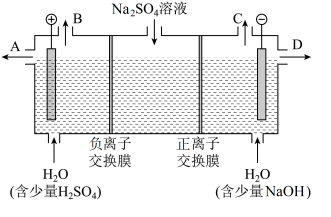
根据如图所示的装置,完成下列各空。
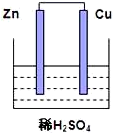
(1)该装置中的总反应式为___________ 。
(2)溶液中的H+移向___________ (填“Cu片”或“Zn片”)
(3)Zn电极的反应式为___________ ,发生 ___________ 反应,(填“氧化”或“还原”)
(4)Cu片为原电池的___________ 极(填“正”或“负”),现象为___________ 。

(1)该装置中的总反应式为
(2)溶液中的H+移向
(3)Zn电极的反应式为
(4)Cu片为原电池的
更新时间:2021-06-08 20:52:51
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】写出下列原电池的电极反应式和总反应的化学方程式。铜片、银片和硝酸银溶液组成的原电池
(1)负极反应式是_______ ;
(2)正极反应式是_______ ;
(3)总反应的化学方程式是_______ 。
(1)负极反应式是
(2)正极反应式是
(3)总反应的化学方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】原电池是化学对人类的一项重大贡献。实验室为研究原电池原理,将a和b用导线连接,设计如图所示装置。
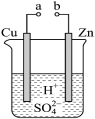
(1)Cu电极为原电池_______ 极(填“正”或“负”),电极反应式为_______ 。
(2)溶液中 移向
移向_______ 极(填“Cu”或“Zn”)。
(3)若工作前两极质量相等,工作一段时间后,导线中通过了1mol 电子,则两极的质量差为_______ g。
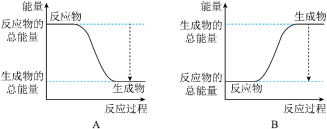
(4)下图能正确表示反应2H2+O2=2H2O中能量变化的是_______ ( 填序号)。

(1)Cu电极为原电池
(2)溶液中
 移向
移向(3)若工作前两极质量相等,工作一段时间后,导线中通过了1mol 电子,则两极的质量差为
(4)下图能正确表示反应2H2+O2=2H2O中能量变化的是

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】电子表和电子计算器的电池常用微型银—锌原电池,其电极分别为Zn和Ag2O,电解质溶液为KOH溶液,负极反应和总反应分别为:Zn+2OH - -2e==ZnO+H2O和Ag2O+Zn==ZnO+2Ag
(1)该原电池工作时负极区溶液的PH值_________ (上升、下降或不变)
(2)该原电池工作时电子由____ (Zn或Ag2O)极经外电路流向_______ (正或负)极。正极上发生的电极反应为__________________________________________________
(1)该原电池工作时负极区溶液的PH值
(2)该原电池工作时电子由
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】常温下,将除去表面氧化膜的Al、Cu片插入电解质A溶液中组成原电池,如图所示:
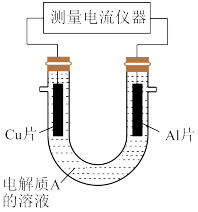
(1)若A为稀盐酸,则Al片作_______ 极,该电极的电极反应式为_______ 。
(2)若A为NaOH,则Al片作_______ 极,该电极的电极反应式为_______ 。
(3)若A为稀HNO3,则Cu片作_______ 极。

(1)若A为稀盐酸,则Al片作
(2)若A为NaOH,则Al片作
(3)若A为稀HNO3,则Cu片作
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势,如图所示:
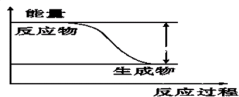
(1)该反应为______ 反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是______ (填字母)。
A.改铁片为铁粉 B.增大压强 C.升高温度 D.将稀硫酸改为98%的浓硫酸
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为____ 极(填“正”或“负”)。铜片上产生的现象为______ ,该极上发生的电极反应为______ 。

(1)该反应为
(2)若要使该反应的反应速率加快,下列措施可行的是
A.改铁片为铁粉 B.增大压强 C.升高温度 D.将稀硫酸改为98%的浓硫酸
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为
您最近一年使用:0次