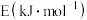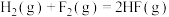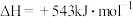根据能量变化示意图,下列说法不正确的是
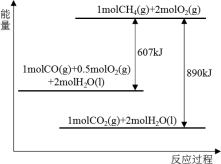

| A.2molCO(g)与1molO2(g)完全反应生成2molCO2(g)时要释放566kJ的能量 |
| B.1molCH4(g)与2molO2(g)具有的总能量高于1molCO2(g)与2molH2O(l) |
| C.1molCH4(g)完全燃烧生成气态水时释放的能量小于890kJ |
| D.16kg液化天然气完全燃烧释放的能量为890000kJ |
更新时间:2021-06-08 20:03:28
|
相似题推荐
【推荐1】下列说法正确的是( )
| A.应用盖斯定律,可计算某些难以直接测量的反应热 |
| B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3kJ·mol-1,则含2molNaOH的稀溶液与一定量的稀硫酸溶液完全反应,其中和热为114.6kJ·mol-1 |
| C.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| D.已知P(白磷,s)=P(红磷,s) ΔH<0,则白磷比红磷稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】2SO2(g)+O2(g)⇌2SO3(g)反应过程中的能量变化如图。下列有关叙述不正确的是
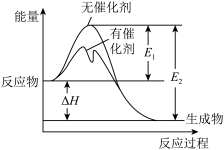

| A.该反应的逆反应为吸热反应,升高温度可提高活化分子的百分数 |
| B.将1molSO2(g)和0.5molO2(g)置于密闭容器中充分反应放热akJ,其热化学方程式为2SO2(g)+O2(g)⇌2SO3(g) ΔH=-2a kJ·mol-l |
| C.该反应中,反应物的总键能小于生成物的总键能 |
| D.ΔH=-(E2-E1),使用催化剂改变活化能,但不改变反应热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关化学反应与能量变化的叙述正确的是
| A.相同条件下,等物质的量的硫蒸气和硫固体分别完全燃烧,前者放出热量更多 |
B.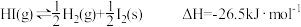 ,则 ,则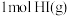 充分分解后放出 充分分解后放出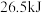 的热量 的热量 |
C.由“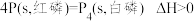 ”可知,白磷比红磷稳定 ”可知,白磷比红磷稳定 |
D.同温同压下,反应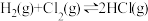 在光照和点燃条件的 在光照和点燃条件的 不同 不同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】 与
与 生成
生成 的反应可以一步完成,也可以分两步完成,各步反应之间的关系如图所示,下列说法不正确的是
的反应可以一步完成,也可以分两步完成,各步反应之间的关系如图所示,下列说法不正确的是

 与
与 生成
生成 的反应可以一步完成,也可以分两步完成,各步反应之间的关系如图所示,下列说法不正确的是
的反应可以一步完成,也可以分两步完成,各步反应之间的关系如图所示,下列说法不正确的是
A. 的燃烧热的 的燃烧热的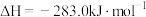 |
B.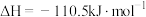 |
C. 金刚石与石墨完全燃烧放出的热量均为 金刚石与石墨完全燃烧放出的热量均为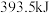 |
D.根据上图推出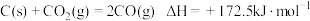 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】肼(N2H4)又称联氨,常用作火箭推进器的燃料。已知:
①N2(g)+O2(g)=2NO(g) ΔH1=+182kJ·mol-1;
②2NO(g) +O2(g)=2NO2(g) ΔH2=-114.3kJ·mol-1;
③2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) ΔH2=-1135.7kJ·mol-1。
下列说法正确的是( )
①N2(g)+O2(g)=2NO(g) ΔH1=+182kJ·mol-1;
②2NO(g) +O2(g)=2NO2(g) ΔH2=-114.3kJ·mol-1;
③2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) ΔH2=-1135.7kJ·mol-1。
下列说法正确的是( )
| A.N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH1=-1068kJ·mol-1 |
B.用铂作电极,以KOH溶液为电解液的肼 空气燃料电池,放电时的负极反应为N2H4-4e-+4OH-=N2+4H2O 空气燃料电池,放电时的负极反应为N2H4-4e-+4OH-=N2+4H2O |
| C.肼与氨类似,溶于水显碱性,可表示为N2H4+H2O=N2H5++OH- |
D.某密闭容器中存在:2NO2(g) N2O4(g),加压 N2O4(g),加压 缩小体积 缩小体积 后颜色先变深后变浅,不能用勒夏特列原理解释 后颜色先变深后变浅,不能用勒夏特列原理解释 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列依据热化学方程式得出的结论正确的是
A.已知 为放热反应,则 为放热反应,则 的能量一定高于 的能量一定高于 的能量 的能量 |
B.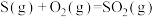  , ,  ,则 ,则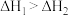 |
C.  , ,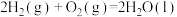  ,则 ,则 |
D.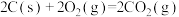  , ,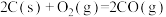  ,则 ,则 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】氢卤酸的能量关系如图所示:下列说法正确的是


A.已知HF气体溶于水放热,则HF的 |
B.相同条件下,HCl的 比HBr的小 比HBr的小 |
C.相同条件下,HCl的( )比HI的大 )比HI的大 |
D.一定条件下,气态原子生成1mol H-X键放出a kJ能量,则该条件下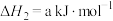 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列焓变比较正确 的是
| A.Na(g)-e-=Na+(g) ΔH1 K(g)-e-=K+(g) ΔH2 ΔH1<ΔH2 |
| B.Cl(g)+e-=Cl-(g) ΔH1 Br(g)+e-=Br-(g) ΔH2 ΔH1<ΔH2 |
| C.NaCl(g)=Na+(g)+Cl-(g) ΔH1 NaBr(g)=Na+(g)+Br-(g) ΔH2 ΔH1<ΔH2 |
| D.H2(g)+Cl2(g)=2HCl(g) ΔH1 H2(g)+Cl2(g)=2HCl(l) ΔH2 ΔH1<ΔH2 |
您最近一年使用:0次

 表示,结合表中信息,下列说法正确的是
表示,结合表中信息,下列说法正确的是