将2.80g含氧化镁的镁条完全溶于50.0mL硫酸溶液后,滴加2.00mol·L-1氢氧化钠溶液,恰好完全沉淀时用去200.0mL。将所得的沉淀灼烧、冷却后称量得固体质量为4.40g。
请计算:
(1)镁条中氧化镁和镁的物质的量之比为n(MgO)︰n(Mg)=___________ 。
(2)上述硫酸的物质的量浓度c(H2SO4)=___________ 。
请计算:
(1)镁条中氧化镁和镁的物质的量之比为n(MgO)︰n(Mg)=
(2)上述硫酸的物质的量浓度c(H2SO4)=
18-19高一下·浙江台州·阶段练习 查看更多[16]
浙江省杭州第十一中学2023-2024学年高一上学期期中考试化学试题(已下线)【定心卷】3.2.2 物质的量在化学方程式计算中的应用随堂练习-人教版2023-2024学年必修第一册(已下线)衔接点20 物质的量浓度-2022年初升高化学无忧衔接?浙江省临海市回浦中学2021-2022学年高一上学期第二次质量抽测(12月)化学试题浙江省台州市路桥区东方理想学校2020-2021学年高一下学期5月月考化学试题(已下线)【浙江新东方】双师296高一下(已下线)【浙江新东方】高三化学20210527-006【2021】【高一下】【期中考】【杭十一中】【高中化学】【杨彦东收集】(已下线)【浙江新东方】高中化学20210304-016(已下线)【浙江新东方】在线化学 (15)浙江省台州市书生中学2020-2021学年高一上学期第三次月考化学试题(已下线)【浙江新东方】双师(39).(已下线)【新东方】高中化学5031人教版(2019)高一必修第一册 第三章 铁 金属材料 第二节 金属材料(已下线)新东方【2019】【高一上】【第一次月考】【RZ】【化学】(已下线)【新东方】2019新中心五地106高中化学浙江省台州市书生中学2018-2019学年高一下学期第一次月考化学试题
更新时间:2021-06-21 22:08:25
|
相似题推荐
计算题
|
较易
(0.85)
解题方法
【推荐1】某温度下22% 硝酸钠溶液150 mL,加入100 g水稀释后溶质质量分数变为14%。
(1)原硝酸钠溶液的质量是__________ 。
(2)原硝酸钠溶液的物质的量浓度是____________ 。
(1)原硝酸钠溶液的质量是
(2)原硝酸钠溶液的物质的量浓度是
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐2】(1)6.20g 白磷(P4)在足量氧气中完全燃烧生成氧化物,反应所消耗的氧气在标准状况下的体积为________________ L.上述燃烧生成氧化物溶有于水配成50.0mLH3PO4溶液,该溶液的物质的量浓度为____________ mol ·L-1
(2)含0.300molH3PO4溶液滴加到含0.500mol Ca(OH)2的悬浮液中,反应恰好完全,生成1种难溶盐和16.2 g水,该难溶盐的化学式可表示为____________ 。
(2)含0.300molH3PO4溶液滴加到含0.500mol Ca(OH)2的悬浮液中,反应恰好完全,生成1种难溶盐和16.2 g水,该难溶盐的化学式可表示为
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐3】物质的量是高中化学中常用的物理量,请完成以下有关其内容的计算:
(1)标准状况下,含有相同氧原子数的CO与CO2的体积之比为____________ 。
(2)等温等压下,等体积的O2和O3所含分子个数比为______________ ,原子个数比为______________ ,质量比为___________ 。
(3)设NA为阿伏加德罗常数的数值,如果a g某气中含有的分子数为b,则c g某气在标准状况下的体积约是___________ 。 (用含NA的式子表示).
(4)配制100mL 1mol•L-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g•mL-1,质量分数为98%)的体积为__________ mL.
(5)100 mL 某Al2(SO4)3溶液中,n(Al3+)=0.20 mol,则其中c(SO )=
)= _________ mol/L。
(6)某氯化镁溶液的密度为1.18g/cm3,其中镁离子的质量分数5.6%,300mL该溶液中Cl-的物质的量等于_________ .
(1)标准状况下,含有相同氧原子数的CO与CO2的体积之比为
(2)等温等压下,等体积的O2和O3所含分子个数比为
(3)设NA为阿伏加德罗常数的数值,如果a g某气中含有的分子数为b,则c g某气在标准状况下的体积约是
(4)配制100mL 1mol•L-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g•mL-1,质量分数为98%)的体积为
(5)100 mL 某Al2(SO4)3溶液中,n(Al3+)=0.20 mol,则其中c(SO
 )=
)= (6)某氯化镁溶液的密度为1.18g/cm3,其中镁离子的质量分数5.6%,300mL该溶液中Cl-的物质的量等于
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】(1)含0.4molAl3+的Al2(SO4)3中所含的 的物质的量是
的物质的量是_______ 。
(2)0.2molNH3与_______ gH2O具有相同的氢原子数。
(3)在同温同压下,同体积的甲烷(CH4)和二氧化碳,原子总数之比为_______ 。
(4)在标准状况下,由CO和CO2组成的混合气体8.96L,质量是16g。此混合物中CO和CO2的物质的量之比是_______ ,混合气体的平均摩尔质量是_______ 。
(5)200mL0.25mol·L-1的NaOH溶液与足量Al完全反应。计算在标准状况下生成H2的体积为_ L
 的物质的量是
的物质的量是(2)0.2molNH3与
(3)在同温同压下,同体积的甲烷(CH4)和二氧化碳,原子总数之比为
(4)在标准状况下,由CO和CO2组成的混合气体8.96L,质量是16g。此混合物中CO和CO2的物质的量之比是
(5)200mL0.25mol·L-1的NaOH溶液与足量Al完全反应。计算在标准状况下生成H2的体积为
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐2】将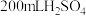 和
和 的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少
的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少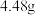 ;向另一份中加入足量
;向另一份中加入足量 溶液,经过滤、洗涤、干燥、称量,得到
溶液,经过滤、洗涤、干燥、称量,得到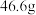 白色沉淀。请计算:
白色沉淀。请计算:
(1)其中一份溶液中加入足量的铁粉发生的反应有两个,写出对应的离子方程式:①___________ 、②___________ 。
(2)原溶液中
___________  ;
;
(3)原溶液中 和
和 的物质的量浓度之比为
的物质的量浓度之比为___________ 。
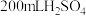 和
和 的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少
的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少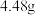 ;向另一份中加入足量
;向另一份中加入足量 溶液,经过滤、洗涤、干燥、称量,得到
溶液,经过滤、洗涤、干燥、称量,得到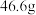 白色沉淀。请计算:
白色沉淀。请计算:(1)其中一份溶液中加入足量的铁粉发生的反应有两个,写出对应的离子方程式:①
(2)原溶液中

 ;
;(3)原溶液中
 和
和 的物质的量浓度之比为
的物质的量浓度之比为
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐3】瑞典皇家科学院宣布,将2007年诺贝尔化学奖授予德国马普学会弗里茨-哈伯(Fritz-Haber)研究所的格哈德·埃特尔(Gerhard Ertl)教授,以表彰他在固体表面化学过程研究领域作出的开拓性成就。合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3。
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4:5,其中Fe2+与Fe3+物质的量之比为_________ 。
(2)当催化剂中Fe2+与Fe3+物质的量之比为1:2时,其催化活性最高,此时铁的氧化物混合物中铁的质量分数为_________ (用小数表示)。
(3)以Fe2O3为原料制备上述催化剂,可向其中加入适量碳粉,发生如下反应:
2Fe2O3+C =4FeO +CO2↑,为制得这种催化活性最高的催化剂,应向480g Fe2O3粉末中加入碳粉的质量为_________ g。
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4:5,其中Fe2+与Fe3+物质的量之比为
(2)当催化剂中Fe2+与Fe3+物质的量之比为1:2时,其催化活性最高,此时铁的氧化物混合物中铁的质量分数为
(3)以Fe2O3为原料制备上述催化剂,可向其中加入适量碳粉,发生如下反应:
2Fe2O3+C =4FeO +CO2↑,为制得这种催化活性最高的催化剂,应向480g Fe2O3粉末中加入碳粉的质量为
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐1】为测定某种铝镁合金中铝的质量分数,探究小组进行了实验:称取质量为20g的合金,加入300g的稀盐酸,合金恰好被溶解,并产生了质量为2g的氢气。以下问题均需要写出计算过程:
(1)铝镁合金中铝的质量分数是多少_______ ?
(2)所用稀盐酸的溶质质量分数是多少_______ ?
(3)若要将反应后的溶液中的溶质全部转变为MgCl2,至少需要加入多少质量的镁_______ ?
(1)铝镁合金中铝的质量分数是多少
(2)所用稀盐酸的溶质质量分数是多少
(3)若要将反应后的溶液中的溶质全部转变为MgCl2,至少需要加入多少质量的镁
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐2】由第IIA族金属单质A和第IIIA族金属单质B组成的混合物1.29g ,用过量的盐酸其完全溶解后生成的氢气在标况下的体积为1.456L.若A和B的原子量之比为8:9,混合物中A和B的原子个数比为2:3,求A、B的的相对原子质量。
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐1】为检验某只含两种元素的固体化合物X的组成,进行如下实验:

请回答下列问题:
(1)固体X的化学式是________ 。
(2)X与盐酸反应的化学方程式是________ 。

请回答下列问题:
(1)固体X的化学式是
(2)X与盐酸反应的化学方程式是
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐2】臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来制取臭氧:3O2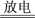 2O3。
2O3。
(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为_______ g·mol-1(保留一位小数)。
(2)将8 L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧为________ L。
(3)在臭氧发生装置中装入氧气100 mL,经反应最后气体体积变为95 mL(体积均在标准状况下测定),则混合气体的密度是____________ g·L-1(保留一位小数)
(4)实验室将氧气和臭氧的混合气体0.896 L(标准状况),通入盛有20.0 g铜粉的反应容器中,充分加热后,粉末的质量最终变为21.6 g。则原混合气中臭氧的体积分数______
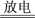 2O3。
2O3。(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为
(2)将8 L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧为
(3)在臭氧发生装置中装入氧气100 mL,经反应最后气体体积变为95 mL(体积均在标准状况下测定),则混合气体的密度是
(4)实验室将氧气和臭氧的混合气体0.896 L(标准状况),通入盛有20.0 g铜粉的反应容器中,充分加热后,粉末的质量最终变为21.6 g。则原混合气中臭氧的体积分数
您最近一年使用:0次
【推荐3】平达喜是常用的中和胃酸的药物,它的化学成分是AlxMgy(OH)zCO3·nH2O,其中氢元素的质量分数为0.040。取该碱式盐3.01g,加入2.0mol/L盐酸使其溶解,当逐滴加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时正好反应完全。若在上述碱式盐溶于盐酸后的溶液中加入过量的氢氧化钠,过滤、洗涤,沉淀物进行干燥后重1.74g。请计算该试样中:
(1)碳酸根的物质的量_____________ ;
(2)镁离子的物质的量_____________ ;
(3)通过计算确定该物质的化学组成为___________ 。
(1)碳酸根的物质的量
(2)镁离子的物质的量
(3)通过计算确定该物质的化学组成为
您最近一年使用:0次



