水是人体最不可缺的物质,已知水的电离方程式:H2O H++OH-。金属钠可以和冷水剧烈反应,完成下列问题:
H++OH-。金属钠可以和冷水剧烈反应,完成下列问题:
(1)写出一绿豆粒大小金属钠投入水中反应的化学方程式,并标出电子转移的方向和数目_____ 。氧化剂是___________ 。
(2)比较金属钠与水、无水乙醇、乙酸溶液反应速率的快慢顺序__________ 。
 H++OH-。金属钠可以和冷水剧烈反应,完成下列问题:
H++OH-。金属钠可以和冷水剧烈反应,完成下列问题:(1)写出一绿豆粒大小金属钠投入水中反应的化学方程式,并标出电子转移的方向和数目
(2)比较金属钠与水、无水乙醇、乙酸溶液反应速率的快慢顺序
更新时间:2021-06-23 16:33:59
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】化学与生活密切相关,回答下列问题:
(1)豆浆中加入适量胆水(含 等)能形成豆腐,是因为胶体遇电解质发生
等)能形成豆腐,是因为胶体遇电解质发生_______ 。
(2)铁与水难反应,但在高温条件下与水蒸气反应,生成的固体物质为_______ (写化学式)。
(3)明矾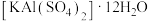 是一种常用净水剂。写出
是一种常用净水剂。写出 溶于水的电离方程式
溶于水的电离方程式_______ 。
(4)“84”消毒液与洁厕灵(主要成分为 )混用会生成有毒的氯气,反应方程式为
)混用会生成有毒的氯气,反应方程式为 。该反应中还原剂是
。该反应中还原剂是_______ ,用双线桥表示该反应中电子转移方向和数目_______ 。
(5)硅胶常用作袋装食品的干燥剂,原因是_______ (用适当的文字描述)。
(1)豆浆中加入适量胆水(含
 等)能形成豆腐,是因为胶体遇电解质发生
等)能形成豆腐,是因为胶体遇电解质发生(2)铁与水难反应,但在高温条件下与水蒸气反应,生成的固体物质为
(3)明矾
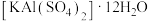 是一种常用净水剂。写出
是一种常用净水剂。写出 溶于水的电离方程式
溶于水的电离方程式(4)“84”消毒液与洁厕灵(主要成分为
 )混用会生成有毒的氯气,反应方程式为
)混用会生成有毒的氯气,反应方程式为 。该反应中还原剂是
。该反应中还原剂是(5)硅胶常用作袋装食品的干燥剂,原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
(1)亚硝酸钠(NaNO2)像食盐一样有咸味,但有很强的毒性,误食NaNO2会使人中毒。
①已知亚硝酸钠能发生如下反应,请将化学方程式配平:____ 。
______NaNO2+______HI=______NO↑+______NaI+______I2+______H2O
②用单线桥法标出该反应中电子转移的方向及数目:____ 。
③被氧化的原子与被还原的原子数目之比为____ 。
④HI在反应中表现的性质是____ (填“氧化性”、“还原性”和“酸性”)。
(2)自来水中的NO 对人类健康会产生危害,碱性条件下用Mg还原NO
对人类健康会产生危害,碱性条件下用Mg还原NO ,主要产物是Mg(OH)2、N2等,写出该反应过程的离子方程式
,主要产物是Mg(OH)2、N2等,写出该反应过程的离子方程式____ 。
(1)亚硝酸钠(NaNO2)像食盐一样有咸味,但有很强的毒性,误食NaNO2会使人中毒。
①已知亚硝酸钠能发生如下反应,请将化学方程式配平:
______NaNO2+______HI=______NO↑+______NaI+______I2+______H2O
②用单线桥法标出该反应中电子转移的方向及数目:
③被氧化的原子与被还原的原子数目之比为
④HI在反应中表现的性质是
(2)自来水中的NO
 对人类健康会产生危害,碱性条件下用Mg还原NO
对人类健康会产生危害,碱性条件下用Mg还原NO ,主要产物是Mg(OH)2、N2等,写出该反应过程的离子方程式
,主要产物是Mg(OH)2、N2等,写出该反应过程的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】氧化还原反应在生产、生活中具有广泛的用途、贯穿古今。
(1)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用右下图表达。

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:________________,其中水为________剂。
(2)过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。关于双氧水,回答下列问题:
①下列反应中,H2O2既体现氧化性又体现还原性的反应是( )
②保存过氧化氢的试剂瓶上最适合贴上的一个标签是( )(填序号)

(3)焊接铜器时,可先用NH4Cl 除去其表面的氧化铜再进行焊接,该反应可表示为:
4CuO + 2NH4Cl △ 3Cu + CuCl2 + N2↑+ 4H2O
①用双线桥标明电子转移的方向和数目。
②该反应中,被氧化的元素是 ,氧化剂是 。
③还原剂与氧化产物的物质的量之比为 。
④反应中若产生0.2 mol的氮气,则有 mol的电子转移。
(1)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用右下图表达。

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:________________,其中水为________剂。
(2)过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。关于双氧水,回答下列问题:
①下列反应中,H2O2既体现氧化性又体现还原性的反应是( )
| A.Na2O2+2HCl═2NaCl+H2O2 | B.Ag2O+H2O2═2Ag+O2↑+H2O |
| C.2H2O2═2H2O +O2↑ | |
| D.3H2O2+Cr2(SO4)3 +10KOH═2K2CrO4+3K2SO4+8H2O | |

(3)焊接铜器时,可先用NH4Cl 除去其表面的氧化铜再进行焊接,该反应可表示为:
4CuO + 2NH4Cl △ 3Cu + CuCl2 + N2↑+ 4H2O
①用双线桥标明电子转移的方向和数目。
②该反应中,被氧化的元素是 ,氧化剂是 。
③还原剂与氧化产物的物质的量之比为 。
④反应中若产生0.2 mol的氮气,则有 mol的电子转移。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】按要求回答下列问题。
(1)写出N2的结构式_____ 。
(2)写出氟的原子结构示意图_____ 。
(3)写出钠与水反应的化学方程式_____ 。
(4)写出Na2SO4的电离方程式_____ 。
(5)用电子式表示MgCl2的形成过程_____ 。
(1)写出N2的结构式
(2)写出氟的原子结构示意图
(3)写出钠与水反应的化学方程式
(4)写出Na2SO4的电离方程式
(5)用电子式表示MgCl2的形成过程
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】补齐物质与其用途的连线,并回答问题。
(1)补齐上图连线_____ 。
(2)上述 的用途,利用了它的
的用途,利用了它的_______ (填“物理”或“化学”)性质。
(3) 可以去除某些有机溶剂中的水分,用化学方程式解释其原因:
可以去除某些有机溶剂中的水分,用化学方程式解释其原因:_______ 。
| 用途 | 物质 |
| A.去除某些有机溶剂中的水分———————————— | a. |
| B.84消毒液的有效成分 | b. |
| C.厨房中的食用碱 | c. |
| D.打印机墨粉中的磁性成分 | d. |
(2)上述
 的用途,利用了它的
的用途,利用了它的(3)
 可以去除某些有机溶剂中的水分,用化学方程式解释其原因:
可以去除某些有机溶剂中的水分,用化学方程式解释其原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】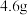 某有机物完全燃烧,得到8.8g二氧化碳和5.4g水。此有机物的蒸气对氢气的相对密度为23,该有机物与金属钠反应放出氢气。其分子式为
某有机物完全燃烧,得到8.8g二氧化碳和5.4g水。此有机物的蒸气对氢气的相对密度为23,该有机物与金属钠反应放出氢气。其分子式为___________ ,结构简式__________ 。
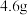 某有机物完全燃烧,得到8.8g二氧化碳和5.4g水。此有机物的蒸气对氢气的相对密度为23,该有机物与金属钠反应放出氢气。其分子式为
某有机物完全燃烧,得到8.8g二氧化碳和5.4g水。此有机物的蒸气对氢气的相对密度为23,该有机物与金属钠反应放出氢气。其分子式为
您最近一年使用:0次
填空题
|
较易
(0.85)
真题
名校
【推荐2】(1)比较给出 能力的相对强弱:
能力的相对强弱:
________  (填“>”“<”或“=”);用一个化学方程式说明
(填“>”“<”或“=”);用一个化学方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱________ 。
(2) 是离子化合物,各原子均满足8电子稳定结构。写出
是离子化合物,各原子均满足8电子稳定结构。写出 的电子式
的电子式________ 。
(3)在常压下,甲醇的沸点(65℃)比甲醛的沸点(-19℃)高。主要原因是________ 。
 能力的相对强弱:
能力的相对强弱:
 (填“>”“<”或“=”);用一个化学方程式说明
(填“>”“<”或“=”);用一个化学方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱(2)
 是离子化合物,各原子均满足8电子稳定结构。写出
是离子化合物,各原子均满足8电子稳定结构。写出 的电子式
的电子式(3)在常压下,甲醇的沸点(65℃)比甲醛的沸点(-19℃)高。主要原因是
您最近一年使用:0次
【推荐1】完成下列问题。
(1)如图所示的乙酸分子结构:
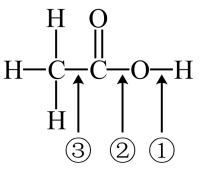
它是一种弱酸, 部分发生电离时断键的位置是_______ (填序号,下同),它跟乙醇发生酯化反应时断键的位置是_______ ,其化学反应式为_______ 。它与Na2CO3反应放出CO2,说明乙酸酸性比碳酸酸性_______ (填“强”或“弱”)。
(2)维生素C的结构简式如图:请回答:

①维生素C的分子式是_______ ,其分子中不含氧的官能团的名称是_______ 。
②维生素C可发生的化学反应有_______ (填序号)。
A. 加成反应 B. 氧化反应 C. 酯化反应
③向维生素C的水溶液中滴加紫色石蕊试液,试液变红,说明此溶液显_______ 性。
(1)如图所示的乙酸分子结构:

它是一种弱酸, 部分发生电离时断键的位置是
(2)维生素C的结构简式如图:请回答:

①维生素C的分子式是
②维生素C可发生的化学反应有
A. 加成反应 B. 氧化反应 C. 酯化反应
③向维生素C的水溶液中滴加紫色石蕊试液,试液变红,说明此溶液显
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】乙烯、苯、乙醇、乙酸是重要的有机化工原料和生活中常见的有机物。
(1)乙烯使酸性KMnO4溶液褪色发生了________ (填“氧化”或“加成”)反应。
(2)苯和浓硝酸在浓硫酸作用下发生反应: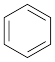 +HNO3
+HNO3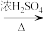
_____ +H2O(请将反应方程式补充完整)。
(3)金属钠和乙醇、乙酸反应能生成_______ (填“H2”或“O2”)
(1)乙烯使酸性KMnO4溶液褪色发生了
(2)苯和浓硝酸在浓硫酸作用下发生反应:
 +HNO3
+HNO3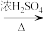
(3)金属钠和乙醇、乙酸反应能生成
您最近一年使用:0次



