氮是自然界中生物体生命活动不可缺少的重要元素,其化合物种类丰富。
Ⅰ.氨是重要的化工原料,实验室可通过图1装置制取。___________ 。
(2)请将图l方框中用试管 收集NH3的装置补充完整___________ 。
(3)图2中,玻璃管内可观察到的现象是___________ (已知:相同条件下,相对分子质量小的气体,运动速率较快)。
(4)图2中,反应的生成物溶于水得到溶液a。取溶液a少许于试管中,___________ (填:操作和现象),则证明溶液a含有 。
。
II.研究氮的循环和转化对生产、生活有重要的价值。某工厂制硝酸的流程如下图所示。___________ (填“i”“ii”或“iii”)。
(6)写出“氧化炉”中反应的化学方程式___________ 。
(7)“吸收塔”排出的尾气中会含有NO、NO2等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。纯碱溶液与NO2反应的原理如下,请将该化学方程式补充完整:Na2CO3 + 2NO2 = NaNO3 +___________ + CO2
Ⅰ.氨是重要的化工原料,实验室可通过图1装置制取。
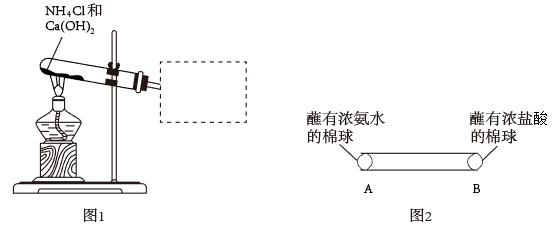
(2)请将图l方框中用
(3)图2中,玻璃管内可观察到的现象是
(4)图2中,反应的生成物溶于水得到溶液a。取溶液a少许于试管中,
 。
。II.研究氮的循环和转化对生产、生活有重要的价值。某工厂制硝酸的流程如下图所示。
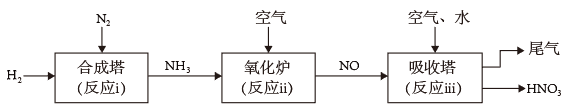
(6)写出“氧化炉”中反应的化学方程式
(7)“吸收塔”排出的尾气中会含有NO、NO2等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。纯碱溶液与NO2反应的原理如下,请将该化学方程式补充完整:Na2CO3 + 2NO2 = NaNO3 +
20-21高一下·北京大兴·期末 查看更多[4]
北京市大兴区2020-2021学年高一下学期期末考试化学试题北京市顺义区杨镇第一中学2021-2022学年高一下学期期中考试化学试题(已下线)高一化学期末押题卷02(“14+5”模式)-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)(已下线)重难点04 硫和氮综合题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)
更新时间:2021-07-06 21:55:39
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】同学们在实验室里用不同的方法分别制取Cu(NO3)2,并在此基础上探究Cu(NO3)2的化学性质。
(1)甲组同学直接用铜屑与稀硝酸反应制取Cu(NO3)2,反应的化学方程式是_____________ 。
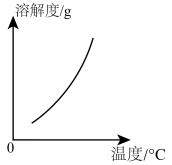
(2)乙组同学查阅了硝酸铜晶体的溶解度曲线(右图),据此设计了以下实验方案,先将铜粉在空气中充分灼烧,再将灼烧后的物质与适量稀HNO3反应,欲从反应后的溶液中得到Cu(NO3)2晶体,依次进行的操作是:蒸发浓缩、____________ 、过滤、洗涤、干燥。乙组同学认为此方案优于甲组的方案,理由之一是__________________________ 。
(3)丙组同学用Cu(NO3)2晶体,探究其热稳定性,实验装置如下所示。(夹持装置和加热仪器未画出)

①充分加热Cu(NO3)2晶体一段时间后,观察到U形管中气体变为红棕色,红棕色气体是____________ 。
②集气瓶最终被水充满,无气体剩余,则晶体分解的生成的气体还有________ 。
③欲证明试管中残留的黑色粉末是CuO[假设Cu(NO3)2晶体已全部分解],实验方案是_________ 。
④由该实验可得出的结论是___________________ 。
(1)甲组同学直接用铜屑与稀硝酸反应制取Cu(NO3)2,反应的化学方程式是

(2)乙组同学查阅了硝酸铜晶体的溶解度曲线(右图),据此设计了以下实验方案,先将铜粉在空气中充分灼烧,再将灼烧后的物质与适量稀HNO3反应,欲从反应后的溶液中得到Cu(NO3)2晶体,依次进行的操作是:蒸发浓缩、
(3)丙组同学用Cu(NO3)2晶体,探究其热稳定性,实验装置如下所示。(夹持装置和加热仪器未画出)

①充分加热Cu(NO3)2晶体一段时间后,观察到U形管中气体变为红棕色,红棕色气体是
②集气瓶最终被水充满,无气体剩余,则晶体分解的生成的气体还有
③欲证明试管中残留的黑色粉末是CuO[假设Cu(NO3)2晶体已全部分解],实验方案是
④由该实验可得出的结论是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示,
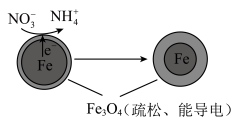
①作负极的物质是____ 。
②正极的电极反应式是____ 。
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
pH=4.5时,NO3-的去除率低。其原因是____ 。
(4)其他条件与(2)相同,经1小时测定NO3-的去除率和pH,结果如下:
与(2)中数据对比,解释(2)中初始pH不同时,NO3-去除率和铁的最终物质形态不同的原因:____ 。
(1)Fe还原水体中NO3-的反应原理如图所示,

①作负极的物质是
②正极的电极反应式是
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
| 初始pH | pH=2.5 | pH=4.5 |
| NO3-的去除率 | 接近100% | <50% |
| 24小时pH | 接近中性 | 接近中性 |
| 铁的最终物质形态 | 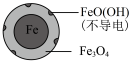 |  |
(4)其他条件与(2)相同,经1小时测定NO3-的去除率和pH,结果如下:
| 初始pH | pH=2.5 | pH=4.5 |
| NO3-的去除率 | 约10% | 约3% |
| 1小时pH | 接近中性 | 接近中性 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某学习小组在实验室研究SO2与Ba(NO3)2溶液的反应:
实验:向盛有2 mL 0.1 mol/L Ba(NO3)2溶液的试管中,缓慢通入SO2气体,试管内有白色沉淀产生,液面上方略显浅棕色。
探究1:白色沉淀产生的原因。
(1) 白色沉淀是___ 。
(2)分析白色沉淀产生的原因,甲同学认为是N O3-氧化了SO2,乙同学认为是溶液中溶解的O2氧化了SO2。
①支持甲同学观点的实验证据是_____________________________________ 。
②依据甲的推断,请写出Ba(NO3)2溶液与SO2反应的离子方程式___________________________________ 。
③乙同学通过下列实验证明了自己的推测正确,请完成实验方案:
探究2:在氧化SO2的过程中,N O3-和O2哪种微粒起了主要作用。
(3) 图1,在无氧条件下,BaCl 2溶液pH下降的原因是______________________________ 。
(4) 图2,BaCl 2溶液中发生反应的离子方程式为_________ 。
(5) 依据上述图象你得出的结论是________ ,说明理由 _________________________
实验:向盛有2 mL 0.1 mol/L Ba(NO3)2溶液的试管中,缓慢通入SO2气体,试管内有白色沉淀产生,液面上方略显浅棕色。
探究1:白色沉淀产生的原因。
(1) 白色沉淀是
(2)分析白色沉淀产生的原因,甲同学认为是N O3-氧化了SO2,乙同学认为是溶液中溶解的O2氧化了SO2。
①支持甲同学观点的实验证据是
②依据甲的推断,请写出Ba(NO3)2溶液与SO2反应的离子方程式
③乙同学通过下列实验证明了自己的推测正确,请完成实验方案:
| 实验操作 | 实验现象 |
| 向2 mL |
探究2:在氧化SO2的过程中,N O3-和O2哪种微粒起了主要作用。
| 实验操作 | 实验数据 |
| 向烧杯中加入煮沸了的0.1 mol/L的BaCl2溶液25 mL,再加入25 mL植物油,冷却至室温,通入SO2,用pH传感器测定溶液pH随时间(t)的变化曲线 | 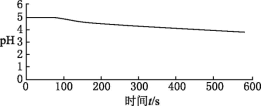 图1:向BaCl2(无氧)溶液中通入SO2 |
| 向烧杯中分别加入25 mL 0.1 mol/L的BaCl2溶液、Ba(NO3)2溶液,通入SO2,用pH传感器分别测定溶液pH随时间(t)变化的曲线。 | 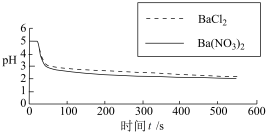 图2:分别向BaCl2、Ba(NO3)2溶液中通入SO2 |
(3) 图1,在无氧条件下,BaCl 2溶液pH下降的原因是
(4) 图2,BaCl 2溶液中发生反应的离子方程式为
(5) 依据上述图象你得出的结论是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】硝酸铵是一种常用的化肥,其工业生产流程如图,请回答下列问题。
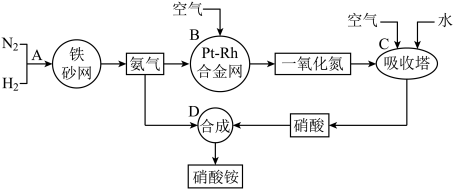
(1)写出反应容器B中发生反应的化学方程式:___ 。
(2)吸收塔C中通入空气的目的是___ (用化学方程式解释);C、D两个反应容器中发生的反应,属于氧化还原反应的是___ (填反应容器代号)。
(3)浓硝酸一般保存在棕色试剂瓶里,并放置在阴凉处,用化学方程式解释原因:___ 。
(4)碳与浓硝酸反应的化学方程式是___ 。

(1)写出反应容器B中发生反应的化学方程式:
(2)吸收塔C中通入空气的目的是
(3)浓硝酸一般保存在棕色试剂瓶里,并放置在阴凉处,用化学方程式解释原因:
(4)碳与浓硝酸反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知固体A是中学常见的矿物,由四种元素组成,现设计如下实验:
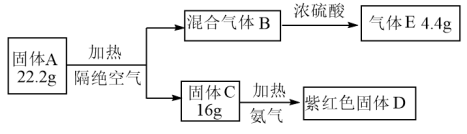
请回答:
(1)固体A的化学式______________ 。
(2)镁能在气体E中燃烧,写出反应的化学方程式____________ 。
(3)写出固体C与氨气反应生成D的化学方程式_________________ 。

请回答:
(1)固体A的化学式
(2)镁能在气体E中燃烧,写出反应的化学方程式
(3)写出固体C与氨气反应生成D的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某小组同学欲探究NH3催化氧化反应,按如图1装置进行实验。
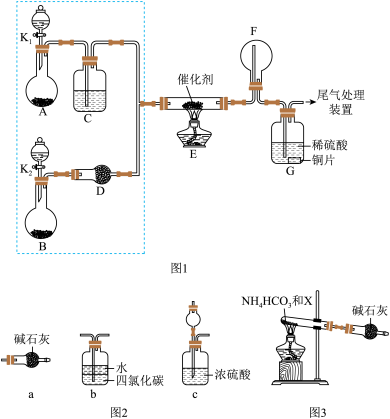
A、B装置可选药品:浓氨水、H2O2、蒸馏水、NaOH固体、MnO2。
(1)B装置中烧瓶内固体名称为___________ 。
(2)NH3催化氧化的化学方程式是___________ 。
(3)甲乙两同学分别按上述装置进行实验,一段时间后,装置G中溶液都变成蓝色。
①甲观察到装置F中有红棕色气体,生成红棕色气体的化学方程式是___________ 。
②乙观察到装置F中只有白烟生成,白烟的成分是(写化学式)___________ 。
③已知酸性条件下的硝酸根有强氧化性,G中生成亿能用排水法收集的无色气体。试根据条件,用离子方程式解释装置G中溶液变成蓝色的原因:___________ 。
(4)为帮助乙实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进。
①甲认为可调节K1和K2控制A、B装置中的产气量,应___________ (填“增加”或“减少”,下同)装置A的产气量,或___________ 装置B中的产气量。
②乙认为可在装置E、F间增加一个装置,该装置可以是图2中___________ 。(填字母)
(5)为实现该反应,也可用图3所示的装置替换上述装置中虚线框部分,化合物X为___________ ,NH4HCO3的作用是___________ 。

A、B装置可选药品:浓氨水、H2O2、蒸馏水、NaOH固体、MnO2。
(1)B装置中烧瓶内固体名称为
(2)NH3催化氧化的化学方程式是
(3)甲乙两同学分别按上述装置进行实验,一段时间后,装置G中溶液都变成蓝色。
①甲观察到装置F中有红棕色气体,生成红棕色气体的化学方程式是
②乙观察到装置F中只有白烟生成,白烟的成分是(写化学式)
③已知酸性条件下的硝酸根有强氧化性,G中生成亿能用排水法收集的无色气体。试根据条件,用离子方程式解释装置G中溶液变成蓝色的原因:
(4)为帮助乙实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进。
①甲认为可调节K1和K2控制A、B装置中的产气量,应
②乙认为可在装置E、F间增加一个装置,该装置可以是图2中
(5)为实现该反应,也可用图3所示的装置替换上述装置中虚线框部分,化合物X为
您最近一年使用:0次



