2007年诺贝尔化学奖授予德国科学家G.Ertl,以表彰他在“固体表面化学过程”研究中做出的贡献。化学工业中广泛使用的负载型催化剂(主要由载体和表面活性组分组成)的制备科学,就是典型的固体表面化学过程的应用。例如,NiO/γ-Al2O3催化剂由γ-Al2O3载体和NiO活性组分组成。研究表明,γ-Al2O3中的O2-具有NaCl晶体中Cl-的堆积方式,γ-Al2O3的主要暴露面为C层或D层(如图1所示),它们的暴露机会均等,分布在该面上的O2-和Al3+如图2所示。
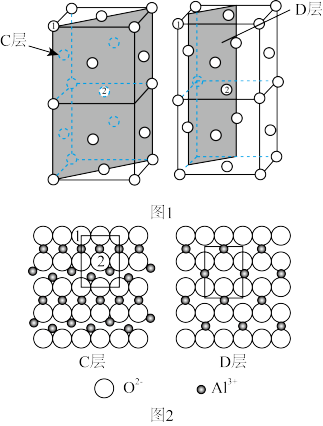
(1)在C层和D层的单位网格(即图2中的方框)内分别有几个处于由体相暴露出来的四面体空隙中的Al3+和八面体空隙中的Al3+_________ 、_______ ?
(2)NiO/γ-Al2O3催化剂中分散在表面的NiO的Ni2+进入能形成表面四面体配位和八面体配位的位置,且与Ni2+相伴的O2-按γ-Al2O3堆积方式外延(假定只形成“单分子层”),请问在C层和D层的单位网格中各能容纳___________ 个Ni2+?
(3)将NiO换为CuO,文献报道Cu2+只能存在于表面的八面体空隙中,如果用氢还原不同配位环境的铜(Cu2+→Cu°),请估计还原温度较低的表面Cu2+分布在C层还是D层中____ ?简述理由____ 。
(4)已知O2-离子半径为0.140nm,试估算CuO/γ-Al2O3催化剂中CuO在γ-Al2O3表面的最大单层分散值(以每100m2的γ-Al2O3载体表面单层分散多少毫摩尔的CuO表示)_____ 。
(5)CuO/γ-Al2O3催化剂可以用于CO的催化氧化:2CO(g)+O2(g)=2CO2(g)。若在p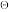 、473K下,有2molCO(g)被完全催化氧化生成CO2(g),请计算此过程中的反应焓变
、473K下,有2molCO(g)被完全催化氧化生成CO2(g),请计算此过程中的反应焓变___________ 。
已知298K下的热力学数据: (CO,g)=-110.5kJ·mol-1,
(CO,g)=-110.5kJ·mol-1, (CO2,g)=-393.5kJ·mol-1,在温度T=298~500K范围内热容Cp,m(CO,g)=29.556J·K-1·mol-1,Cp,m(O2,g)=29.526J·K-1·mol-1,Cp,m(CO2,g)=27.437J·K-1·mol-1。
(CO2,g)=-393.5kJ·mol-1,在温度T=298~500K范围内热容Cp,m(CO,g)=29.556J·K-1·mol-1,Cp,m(O2,g)=29.526J·K-1·mol-1,Cp,m(CO2,g)=27.437J·K-1·mol-1。
(6)CO的低温催化消除通常采用以γ-Al2O3为载体的负载型催化剂,人们对其反应机理已经有了较深入的研究。实验结果表明,CO在催化剂表面与O2反应的可能历程如下:
(1)CO+M CO(ads)
CO(ads)
(2)O2+2M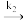 2O(ads)
2O(ads)
(3)CO(ads)+O(ads)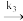 CO2(ads)+M
CO2(ads)+M
(4)CO2(ads) CO2+M
CO2+M
式中M为表面活性位,在该实验条件下M的数量为定值,下标ads表示吸附态。请用稳态近似法推导其速率方程,速率用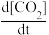 表示
表示____________ 。

(1)在C层和D层的单位网格(即图2中的方框)内分别有几个处于由体相暴露出来的四面体空隙中的Al3+和八面体空隙中的Al3+
(2)NiO/γ-Al2O3催化剂中分散在表面的NiO的Ni2+进入能形成表面四面体配位和八面体配位的位置,且与Ni2+相伴的O2-按γ-Al2O3堆积方式外延(假定只形成“单分子层”),请问在C层和D层的单位网格中各能容纳
(3)将NiO换为CuO,文献报道Cu2+只能存在于表面的八面体空隙中,如果用氢还原不同配位环境的铜(Cu2+→Cu°),请估计还原温度较低的表面Cu2+分布在C层还是D层中
(4)已知O2-离子半径为0.140nm,试估算CuO/γ-Al2O3催化剂中CuO在γ-Al2O3表面的最大单层分散值(以每100m2的γ-Al2O3载体表面单层分散多少毫摩尔的CuO表示)
(5)CuO/γ-Al2O3催化剂可以用于CO的催化氧化:2CO(g)+O2(g)=2CO2(g)。若在p
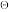 、473K下,有2molCO(g)被完全催化氧化生成CO2(g),请计算此过程中的反应焓变
、473K下,有2molCO(g)被完全催化氧化生成CO2(g),请计算此过程中的反应焓变已知298K下的热力学数据:
 (CO,g)=-110.5kJ·mol-1,
(CO,g)=-110.5kJ·mol-1, (CO2,g)=-393.5kJ·mol-1,在温度T=298~500K范围内热容Cp,m(CO,g)=29.556J·K-1·mol-1,Cp,m(O2,g)=29.526J·K-1·mol-1,Cp,m(CO2,g)=27.437J·K-1·mol-1。
(CO2,g)=-393.5kJ·mol-1,在温度T=298~500K范围内热容Cp,m(CO,g)=29.556J·K-1·mol-1,Cp,m(O2,g)=29.526J·K-1·mol-1,Cp,m(CO2,g)=27.437J·K-1·mol-1。(6)CO的低温催化消除通常采用以γ-Al2O3为载体的负载型催化剂,人们对其反应机理已经有了较深入的研究。实验结果表明,CO在催化剂表面与O2反应的可能历程如下:
(1)CO+M
 CO(ads)
CO(ads)(2)O2+2M
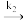 2O(ads)
2O(ads)(3)CO(ads)+O(ads)
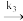 CO2(ads)+M
CO2(ads)+M(4)CO2(ads)
 CO2+M
CO2+M式中M为表面活性位,在该实验条件下M的数量为定值,下标ads表示吸附态。请用稳态近似法推导其速率方程,速率用
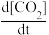 表示
表示
更新时间:2021-07-08 14:37:24
|
相似题推荐
解答题-结构与性质
|
困难
(0.15)
【推荐1】硼氢化钠是一种重要的还原剂,可用于纸张漂白、醛酮的还原及含汞污水的处理等等。近年来,科学家十分关注硼氢化钠用作储氢介质的研究。2005年G.J.Gainsford和T.Kemmitt考查了硼氢化钠的醇解反应,发现它与乙醇反应的产物A是由互相平行的一维链组成的晶体。
(1)写 出硼氢化钠与乙醇反应的化学反应方程式____ 。
(2)根据A中存在的作用力类型说明A属于何种晶体____ 。
(3)画出A 的一维结构示意图,确定A的结构基元,抽出一维点阵____ 。
(4)A中Na的配位数为多少____ ?硼原子采取什么杂化____ ?
(5)硼的一种同素异构体是 由B12(以B为顶点的二十面体)单位和单个B原子组成的晶体,其晶胞参数为a = b = 875.6pm, c = 507.8pm, 晶体密度ρ = 2.310g·cm-3.晶胞沿a、b、c轴的投影图如下:

①计算晶胞中的原子数____ 。
②画出晶胞示意图____ 。
③确定晶体的结构基元、点阵型式及特征对称元素____ 。
(1)写 出硼氢化钠与乙醇反应的化学反应方程式
(2)根据A中存在的作用力类型说明A属于何种晶体
(3)画出A 的一维结构示意图,确定A的结构基元,抽出一维点阵
(4)A中Na的配位数为多少
(5)硼的一种同素异构体是 由B12(以B为顶点的二十面体)单位和单个B原子组成的晶体,其晶胞参数为a = b = 875.6pm, c = 507.8pm, 晶体密度ρ = 2.310g·cm-3.晶胞沿a、b、c轴的投影图如下:

①计算晶胞中的原子数
②画出晶胞示意图
③确定晶体的结构基元、点阵型式及特征对称元素
您最近一年使用:0次
解答题-无机推断题
|
困难
(0.15)
【推荐2】金属M的三氯化物MCl3水溶液中加入锌汞齐后可得还原性溶液A,若将该溶液加入到醋酸钠的饱和溶液中可以得到难溶的红色晶体B。已知MCl3中Cl含量为67.16%,光谱分析表明,B分子呈中心对称,其中M原子的配位数为6(即M原子周围有6个原子与之成键),M原子含量27.64%,碳原子仅存在于醋酸根离子中,碳原子含量25.54%。试问:
(1)金属M的原子量为_______ 。
(2)红色晶体B中M原子和碳原子的个数比为_______ 。
(3)红色晶体B中和M原子配位的除了醋酸根离子还有_______ 。
(4)红色晶体B的分子式为_______ 。
(5)画出红色晶体B的结构图_______ 。
(1)金属M的原子量为
(2)红色晶体B中M原子和碳原子的个数比为
(3)红色晶体B中和M原子配位的除了醋酸根离子还有
(4)红色晶体B的分子式为
(5)画出红色晶体B的结构图
您最近一年使用:0次
【推荐3】回答下列问题:
(1)利用双离子交换膜电解法可以从含硝酸铵的工业废水中生产硝酸和氨。
①阳极室得到的是哪种物质_____ ?写出阳极半反应方程式_____ 。
②阴极室得到的是哪种物质_____ ?写出阴极半反应及获得相应物质的方程式_____ 。
(2)电解乙酸钠水溶液,在阳极收集到X和Y的混合气体。气体通过新制的澄清石灰水,X被完全吸收,得到白色沉淀。纯净的气体Y冷却到90.23 K,析出无色晶体,X-射线衍射表明,该晶体属立方晶系,体心立方点阵,晶胞参数a= 530.4pm,Z=2,密度ρ= 0.69g·cm-3。继续冷却,晶体转化为单斜晶系,a=422.6pm, b=562.3 pm, c= 584.5 pm, β= 90.41°。
①写出X的化学式_____ ;写出X和石灰水反应的方程式_____ 。
②通过计算推出Y的化学式(Y分子中存在三次旋转轴)_____ 。
③写出电解乙酸钠水溶液时阳极半反应的方程式_____ 。
④写出单斜晶系的晶胞中Y分子的数目_____ 。
⑤降温过程中晶体转化为对称性较低的单斜晶体,简述原因_____ 。
(1)利用双离子交换膜电解法可以从含硝酸铵的工业废水中生产硝酸和氨。
①阳极室得到的是哪种物质
②阴极室得到的是哪种物质
(2)电解乙酸钠水溶液,在阳极收集到X和Y的混合气体。气体通过新制的澄清石灰水,X被完全吸收,得到白色沉淀。纯净的气体Y冷却到90.23 K,析出无色晶体,X-射线衍射表明,该晶体属立方晶系,体心立方点阵,晶胞参数a= 530.4pm,Z=2,密度ρ= 0.69g·cm-3。继续冷却,晶体转化为单斜晶系,a=422.6pm, b=562.3 pm, c= 584.5 pm, β= 90.41°。
①写出X的化学式
②通过计算推出Y的化学式(Y分子中存在三次旋转轴)
③写出电解乙酸钠水溶液时阳极半反应的方程式
④写出单斜晶系的晶胞中Y分子的数目
⑤降温过程中晶体转化为对称性较低的单斜晶体,简述原因
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
【推荐1】NO是大气的污染物之一。它催化O3分解,破坏大气臭氧层;在空气中易被氧化为NO2,氮的氧化物参与产生光化学烟雾。空气中NO最高允许含量不超过5mg/L。为此,人们一直在努力寻找高效催化剂,将NO分解为N2和O2。
(1)用热力学理论判断NO在常温常压下能否自发分解_______ (已知N2、NO和O2的解离焓分别为941.7、631.8和493.7kJ/mol)。
(2)有研究者用载负Cu的ZSM-5分子筛作催化剂,对NO的催化分解获得了良好效果。实验发现,高温下,当氧分压很小时,Cu/ZSM-5催化剂对NO的催化分解为一级反应。考查催化剂活性常用如下图所示的固定床反应装置。反应气体(NO)由惰性载气(He)带入催化剂床层,发生催化反应。某试验混合气中NO的体积分数为4.0%,混合气流速为4.0×10cm3/min(已换算成标准状况),673K和723K时,反应20秒后,测得平均每个活性中心上NO分解的分子数分别为1.91和5.03。试求NO在该催化剂上分解反应的活化能_______ 。
(3)在上述条件下,设催化剂表面活性中心(Cu+)含量1.0×10-6mol,试计算NO在723K时分解反应的转化率_______ 。

(4)研究者对NO在该催化剂上的分解反应提出如下反应机理:
NO+M NO-M[1]
NO-M[1]
2NO-M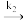 N2+2O-M[2]
N2+2O-M[2]
20-M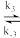 O2+2M(快)[3]
O2+2M(快)[3]
M表示催化剂活性中心,NO为弱吸附,NO-M浓度可忽略。试根据上述机理和M的物料平衡,推导反应的速率方程,并解释当O2分压很低时,总反应表现出一级反应动力学特征_______ 。
(1)用热力学理论判断NO在常温常压下能否自发分解
(2)有研究者用载负Cu的ZSM-5分子筛作催化剂,对NO的催化分解获得了良好效果。实验发现,高温下,当氧分压很小时,Cu/ZSM-5催化剂对NO的催化分解为一级反应。考查催化剂活性常用如下图所示的固定床反应装置。反应气体(NO)由惰性载气(He)带入催化剂床层,发生催化反应。某试验混合气中NO的体积分数为4.0%,混合气流速为4.0×10cm3/min(已换算成标准状况),673K和723K时,反应20秒后,测得平均每个活性中心上NO分解的分子数分别为1.91和5.03。试求NO在该催化剂上分解反应的活化能
(3)在上述条件下,设催化剂表面活性中心(Cu+)含量1.0×10-6mol,试计算NO在723K时分解反应的转化率

(4)研究者对NO在该催化剂上的分解反应提出如下反应机理:
NO+M
 NO-M[1]
NO-M[1]2NO-M
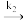 N2+2O-M[2]
N2+2O-M[2]20-M
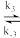 O2+2M(快)[3]
O2+2M(快)[3]M表示催化剂活性中心,NO为弱吸附,NO-M浓度可忽略。试根据上述机理和M的物料平衡,推导反应的速率方程,并解释当O2分压很低时,总反应表现出一级反应动力学特征
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
解题方法
【推荐2】车载甲醇质子交换膜燃料电池(PEMFC)将甲醇蒸气转化为氢气的工艺有2种:
i.水蒸气变换(重整)法;
ii.空气氧化法。
两种工艺都得到副产品CO。
(1)I.分别写出这2种工艺(包括副反应)的化学方程式,通过计算,说明这2种工艺的优缺点________ 。
有关资料(298.15K)列于下表:
(2)II.上述2种工艺产生的少量CO会吸附在燃料电池的Pt或其它贵金属催化剂表面,阻碍H2的吸附和电氧化,引起燃料电池放电性能急剧下降,为此,开发了除去CO的方法。现有一组实验结果(500K)如下:CO(g)+1/2O2(g)→CO2(g)
表中 、
、 ,分别为CO和O2的分压;
,分别为CO和O2的分压; 为以每秒每个催化剂Ru活性位上所消耗的CO分子数表示的2O的氧化速率。
为以每秒每个催化剂Ru活性位上所消耗的CO分子数表示的2O的氧化速率。
①求催化剂Ru上CO氧化反应分别对CO和O2的反应级数(取整数)___ ,写出速率方程___ 。
②固体Ru表面具有吸附气体分子的能力,但是气体分子只有碰到空活性位才可能发生吸附作用。当已吸附分子的热运动的动能足以克服固体引力场的势垒时,才能脱附,重新回到气相。假设CO和O2的吸付与脱附互不影响,并且表面是均匀的,以θ表示气体分子覆盖活性位的百分数(覆盖度),则气体的吸附速率与气体的压力成正比,也与固体表面的空活性位数成正比,研究提出CO在Ru。上的氧化反应的一种机理如下:
CO+M OC-M
OC-M
O2+2M 2O-M
2O-M
OC-M+ O2-M→CO2+
O2-M→CO2+
其中 、
、 分别为CO在Ru的活性位上的吸附速率常数和脱附速率常数,
分别为CO在Ru的活性位上的吸附速率常数和脱附速率常数, ,为O2在Ru的活性位,上的吸附速率常数。M表示Ru催化剂表面上的活性位。CO在Ru表面活性位上的吸附比O2的吸附强得多。
,为O2在Ru的活性位,上的吸附速率常数。M表示Ru催化剂表面上的活性位。CO在Ru表面活性位上的吸附比O2的吸附强得多。
试根据上述反应机理推导CO在催化剂Ru表面上氧化反应的速率方程(不考虑O2的脱附;也不考虑产物CO2的吸附),并与实验结果比较__________ 。
(3)III.有关物质的热力学函数(298.15K)如下:
在373.15K,100kPa下,水的蒸发焓 =40.64kJ·mol-1,在298.15~373.15K间水的等压热容。
=40.64kJ·mol-1,在298.15~373.15K间水的等压热容。
为75.6J·K-1·mol-1,水蒸气的热容为33.9J·K-1·mol-1。
①将上述工艺得到的富氢气体作为质子交换膜燃料电池的燃料。燃料电池的理论效率是指电池所能做的最大电功相对于燃烧反应焓变的效率。在298.15K,100kPa下,当1molH2燃烧分别生成H2O(1)和H2O(g)时,计算燃料电池工作的理论效率_______ ,并通过计算分析两者存在差别的原因_______ 。
②若燃料电池在473.15K、100kPa下工作,其理论效率又为多少_____ (可忽略焓变和熵变随温度的变化)?
③说明(1)和(2)中的同一反应有不同理论效率的原因______ 。
i.水蒸气变换(重整)法;
ii.空气氧化法。
两种工艺都得到副产品CO。
(1)I.分别写出这2种工艺(包括副反应)的化学方程式,通过计算,说明这2种工艺的优缺点
有关资料(298.15K)列于下表:
| 物质 |  /kJ·mol-1 /kJ·mol-1 |  /J·K-1·mol-1 /J·K-1·mol-1 |
| CH3OH(g) CO2(g) CO(g)。 H2O(g) H2(g) | -200.66 -393.51 -110.52 -241.82 0 | 239.81 213.64 197.91 188.83 130.59 |
(2)II.上述2种工艺产生的少量CO会吸附在燃料电池的Pt或其它贵金属催化剂表面,阻碍H2的吸附和电氧化,引起燃料电池放电性能急剧下降,为此,开发了除去CO的方法。现有一组实验结果(500K)如下:CO(g)+1/2O2(g)→CO2(g)
 |  |  /CO分子数(Ru活性位·s-1) /CO分子数(Ru活性位·s-1) |  |  |  /CO分子数(Ru活性位·s-1) /CO分子数(Ru活性位·s-1) |
| 0.005 0.010 0.017 0.048 0.080 | 0.01 0.01 0.01 0.01 0.01 | 20.5 7.0 5.0 2.0 1.1 | 0.01 0.01 0.01 0.01 | 0.010 0.070 0.090 0.12 | 7 50 65 80 |
表中
 、
、 ,分别为CO和O2的分压;
,分别为CO和O2的分压; 为以每秒每个催化剂Ru活性位上所消耗的CO分子数表示的2O的氧化速率。
为以每秒每个催化剂Ru活性位上所消耗的CO分子数表示的2O的氧化速率。①求催化剂Ru上CO氧化反应分别对CO和O2的反应级数(取整数)
②固体Ru表面具有吸附气体分子的能力,但是气体分子只有碰到空活性位才可能发生吸附作用。当已吸附分子的热运动的动能足以克服固体引力场的势垒时,才能脱附,重新回到气相。假设CO和O2的吸付与脱附互不影响,并且表面是均匀的,以θ表示气体分子覆盖活性位的百分数(覆盖度),则气体的吸附速率与气体的压力成正比,也与固体表面的空活性位数成正比,研究提出CO在Ru。上的氧化反应的一种机理如下:
CO+M
 OC-M
OC-MO2+2M
 2O-M
2O-MOC-M+
 O2-M→CO2+
O2-M→CO2+
其中
 、
、 分别为CO在Ru的活性位上的吸附速率常数和脱附速率常数,
分别为CO在Ru的活性位上的吸附速率常数和脱附速率常数, ,为O2在Ru的活性位,上的吸附速率常数。M表示Ru催化剂表面上的活性位。CO在Ru表面活性位上的吸附比O2的吸附强得多。
,为O2在Ru的活性位,上的吸附速率常数。M表示Ru催化剂表面上的活性位。CO在Ru表面活性位上的吸附比O2的吸附强得多。试根据上述反应机理推导CO在催化剂Ru表面上氧化反应的速率方程(不考虑O2的脱附;也不考虑产物CO2的吸附),并与实验结果比较
(3)III.有关物质的热力学函数(298.15K)如下:
| 物质 |  /kJ·mol-1 /kJ·mol-1 |  /J·K-1·mol-1 /J·K-1·mol-1 |
| H2(g) O2(g) H2O(g) H2O(1) | 0 0 -241.82 -285.84 | 130.59 205.03 188.83 69.94 |
在373.15K,100kPa下,水的蒸发焓
 =40.64kJ·mol-1,在298.15~373.15K间水的等压热容。
=40.64kJ·mol-1,在298.15~373.15K间水的等压热容。为75.6J·K-1·mol-1,水蒸气的热容为33.9J·K-1·mol-1。
①将上述工艺得到的富氢气体作为质子交换膜燃料电池的燃料。燃料电池的理论效率是指电池所能做的最大电功相对于燃烧反应焓变的效率。在298.15K,100kPa下,当1molH2燃烧分别生成H2O(1)和H2O(g)时,计算燃料电池工作的理论效率
②若燃料电池在473.15K、100kPa下工作,其理论效率又为多少
③说明(1)和(2)中的同一反应有不同理论效率的原因
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
【推荐1】900K、 下,乙烷脱氢反应的吉布斯自由能变为
下,乙烷脱氢反应的吉布斯自由能变为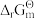 =22.39kJ·mol-1,有关物质的标准摩尔熵数据示于下表。
=22.39kJ·mol-1,有关物质的标准摩尔熵数据示于下表。
(1)写出乙烷脱氢反应的方程式_______ 。
(2)计算900K时乙烷脱氢反应的平衡常数_______ 。
(3)求出900K时乙烯氢化反应的焓变
_______ 。
(4)900K时,乙烷经过脱氢催化剂后反应的平衡组成(体积百分数)是_______ ,平衡时反应体系的总压为101.3kPa。
(5)假设脱氢反应的焓变在600~900K之间时与温度无关,请计算600K时脱氢反应的平衡常数_______ 。
(6)比较600K、900K时脱氢反应平衡常数的数值,并予以简要解释_______ 。
 下,乙烷脱氢反应的吉布斯自由能变为
下,乙烷脱氢反应的吉布斯自由能变为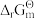 =22.39kJ·mol-1,有关物质的标准摩尔熵数据示于下表。
=22.39kJ·mol-1,有关物质的标准摩尔熵数据示于下表。| 物质 |  /J·mol-1·K-1(900K) /J·mol-1·K-1(900K) |
| H2(g) | 163.0 |
| 乙烷(g) | 319.7 |
| 乙烯(g) | 291.7 |
(2)计算900K时乙烷脱氢反应的平衡常数
(3)求出900K时乙烯氢化反应的焓变

(4)900K时,乙烷经过脱氢催化剂后反应的平衡组成(体积百分数)是
(5)假设脱氢反应的焓变在600~900K之间时与温度无关,请计算600K时脱氢反应的平衡常数
(6)比较600K、900K时脱氢反应平衡常数的数值,并予以简要解释
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
【推荐2】NO是大气的污染物之一。它催化O3分解,破坏大气臭氧层;在空气中易被氧化为NO2,氮的氧化物参与产生光化学烟雾。空气中NO最高允许含量不超过5mg/L。为此,人们一直在努力寻找高效催化剂,将NO分解为N2和O2。
(1)用热力学理论判断NO在常温常压下能否自发分解_______ (已知N2、NO和O2的解离焓分别为941.7、631.8和493.7kJ/mol)。
(2)有研究者用载负Cu的ZSM-5分子筛作催化剂,对NO的催化分解获得了良好效果。实验发现,高温下,当氧分压很小时,Cu/ZSM-5催化剂对NO的催化分解为一级反应。考查催化剂活性常用如下图所示的固定床反应装置。反应气体(NO)由惰性载气(He)带入催化剂床层,发生催化反应。某试验混合气中NO的体积分数为4.0%,混合气流速为4.0×10cm3/min(已换算成标准状况),673K和723K时,反应20秒后,测得平均每个活性中心上NO分解的分子数分别为1.91和5.03。试求NO在该催化剂上分解反应的活化能_______ 。
(3)在上述条件下,设催化剂表面活性中心(Cu+)含量1.0×10-6mol,试计算NO在723K时分解反应的转化率_______ 。

(4)研究者对NO在该催化剂上的分解反应提出如下反应机理:
NO+M NO-M[1]
NO-M[1]
2NO-M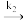 N2+2O-M[2]
N2+2O-M[2]
20-M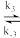 O2+2M(快)[3]
O2+2M(快)[3]
M表示催化剂活性中心,NO为弱吸附,NO-M浓度可忽略。试根据上述机理和M的物料平衡,推导反应的速率方程,并解释当O2分压很低时,总反应表现出一级反应动力学特征_______ 。
(1)用热力学理论判断NO在常温常压下能否自发分解
(2)有研究者用载负Cu的ZSM-5分子筛作催化剂,对NO的催化分解获得了良好效果。实验发现,高温下,当氧分压很小时,Cu/ZSM-5催化剂对NO的催化分解为一级反应。考查催化剂活性常用如下图所示的固定床反应装置。反应气体(NO)由惰性载气(He)带入催化剂床层,发生催化反应。某试验混合气中NO的体积分数为4.0%,混合气流速为4.0×10cm3/min(已换算成标准状况),673K和723K时,反应20秒后,测得平均每个活性中心上NO分解的分子数分别为1.91和5.03。试求NO在该催化剂上分解反应的活化能
(3)在上述条件下,设催化剂表面活性中心(Cu+)含量1.0×10-6mol,试计算NO在723K时分解反应的转化率

(4)研究者对NO在该催化剂上的分解反应提出如下反应机理:
NO+M
 NO-M[1]
NO-M[1]2NO-M
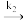 N2+2O-M[2]
N2+2O-M[2]20-M
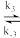 O2+2M(快)[3]
O2+2M(快)[3]M表示催化剂活性中心,NO为弱吸附,NO-M浓度可忽略。试根据上述机理和M的物料平衡,推导反应的速率方程,并解释当O2分压很低时,总反应表现出一级反应动力学特征
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
解题方法
【推荐3】高温条件下反应机理的研究一直是化学反应动力学的基本课题,1956年的诺贝尔化学奖获得者在该领域做出过杰出的贡献。科研工作者研究了1000K下丙酮的热分解反应并提出了如下反应历程:
CH3COCH3 CH3·+CH3CO· (1)Ea(1)=351KJ·mol-1
CH3·+CH3CO· (1)Ea(1)=351KJ·mol-1
CH3CO·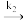 CH3·+CO (2)Ea(2)=42KJ·mol-1
CH3·+CO (2)Ea(2)=42KJ·mol-1
CH3·+CH3COCH3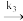 CH4+CH3COCH2· (3)Ea。(3)=63KJ·mol-1
CH4+CH3COCH2· (3)Ea。(3)=63KJ·mol-1
CH3COCH2· CH3·+CH2CO (4)Ea(1)=200KJ·mol-1
CH3·+CH2CO (4)Ea(1)=200KJ·mol-1
CH3·+CH3COCH2· C2H5COCH3 (5)Ea(5)=21KJ·mol-1
C2H5COCH3 (5)Ea(5)=21KJ·mol-1
(1)上述历程是根据两个平行反应而提出的,请写出反应方程式_______ 。
(2)实验测得1000K下热分解反应对丙酮为一级反应,试推出反应的速率方程_______ 。提示:①消耗丙酮的主要基元步骤是反应(3);②可忽略各基元反应指前因子的影响。
(3)根据(2)推出的速率方程,计算表观活化能_______ 。
(4)分解产物中CH4可以和水蒸气反应制备H2:CH4(g)+H2O(g)→3H2(g)+CO(g)。试根据下表数据计算该反应在298K时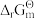 和平衡常数K
和平衡常数K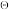 ,并指出平衡常数随温度的变化趋势
,并指出平衡常数随温度的变化趋势_______ 。
相关物质热力学数据(298K)
CH3COCH3
 CH3·+CH3CO· (1)Ea(1)=351KJ·mol-1
CH3·+CH3CO· (1)Ea(1)=351KJ·mol-1CH3CO·
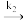 CH3·+CO (2)Ea(2)=42KJ·mol-1
CH3·+CO (2)Ea(2)=42KJ·mol-1CH3·+CH3COCH3
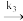 CH4+CH3COCH2· (3)Ea。(3)=63KJ·mol-1
CH4+CH3COCH2· (3)Ea。(3)=63KJ·mol-1CH3COCH2·
 CH3·+CH2CO (4)Ea(1)=200KJ·mol-1
CH3·+CH2CO (4)Ea(1)=200KJ·mol-1CH3·+CH3COCH2·
 C2H5COCH3 (5)Ea(5)=21KJ·mol-1
C2H5COCH3 (5)Ea(5)=21KJ·mol-1(1)上述历程是根据两个平行反应而提出的,请写出反应方程式
(2)实验测得1000K下热分解反应对丙酮为一级反应,试推出反应的速率方程
(3)根据(2)推出的速率方程,计算表观活化能
(4)分解产物中CH4可以和水蒸气反应制备H2:CH4(g)+H2O(g)→3H2(g)+CO(g)。试根据下表数据计算该反应在298K时
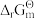 和平衡常数K
和平衡常数K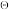 ,并指出平衡常数随温度的变化趋势
,并指出平衡常数随温度的变化趋势相关物质热力学数据(298K)
| 物质 | 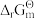 KJ·mol-1 KJ·mol-1 |  /J·mol-1·K-1 /J·mol-1·K-1 |
| CH4(g) | -74.4 | 186.3 |
| H2O(g) | -241.8 | 188.8 |
| H2(g) | 0 | 130.7 |
| CO(g) | -110.5 | 197.7 |
| H2O(1) | -285.8 | 69.9. |
您最近一年使用:0次



