苯胺(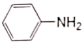 )是重要的化工原料,其制备原理为:2
)是重要的化工原料,其制备原理为:2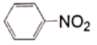 +3Sn+12HCl
+3Sn+12HCl 2
2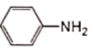 +3SnCl4+4 H2O
+3SnCl4+4 H2O
已知:苯胺类似氨气有碱性,与盐酸反应生成可溶于水的盐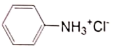 ;部分物质物理性质见下表:
;部分物质物理性质见下表:
回答下列问题:
(1)实验室用苯制取硝基苯的化学方程式为___________ 。
(2)往硝基苯中加入 和足量盐酸充分还原,冷却后,往混合物中加入过量
和足量盐酸充分还原,冷却后,往混合物中加入过量 溶液得碱化液,加
溶液得碱化液,加 溶液的主要目的是析出苯胺,反应的离子方程式为
溶液的主要目的是析出苯胺,反应的离子方程式为___________ 。
(3)分离提纯:
步骤ⅰ.将碱化液蒸馏,收集到苯胺与水的混合物,分液得粗苯胺和水溶液;
步骤ⅱ.步骤ⅰ所得水溶液中加 至饱和,用乙醚萃取得萃取液与粗苯胺合并:
至饱和,用乙醚萃取得萃取液与粗苯胺合并:
步骤ⅲ。合并溶液用干燥剂干燥,过滤,将滤液蒸馏并收集温度 时的馏分得到苯胺。
时的馏分得到苯胺。
①步骤ⅰ蒸馏不需温度计控制温度,试依据收集馏分的特点,分析原因是___________ 。
②步骤ⅱ萃取分液操作过程中要远离明火及热源,原因是___________ 。如果没有步骤ⅱ,苯胺的产率___________ (填“不变”、“增大”或“减小”)。步骤ⅲ中干燥剂可以选用___________ (填序号)
a.浓硫酸 b.五氧化二磷 c. 固体
固体
③步骤ⅲ中蒸馏获得苯胺的温度 的范围为
的范围为___________ 。
(4)二次纯化:
苯胺中混有少量硝基苯杂质,可以采用如下方案除杂提纯:
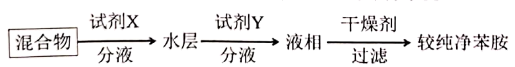
试剂 是
是___________ ,试剂 是
是___________ ,“液相”是___________ (填“水层”或“有机层”)
 )是重要的化工原料,其制备原理为:2
)是重要的化工原料,其制备原理为:2 +3Sn+12HCl
+3Sn+12HCl 2
2 +3SnCl4+4 H2O
+3SnCl4+4 H2O已知:苯胺类似氨气有碱性,与盐酸反应生成可溶于水的盐
 ;部分物质物理性质见下表:
;部分物质物理性质见下表:| 物质 | 熔点/℃ | 沸点/℃ | 溶解性 | 密度/ |
| 苯胺 | 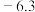 | 184 | 微溶于水,易溶于乙醚 | 1.02 |
| 硝基苯 | 5.7 | 210.9 | 难溶于水,易溶于乙醚 | 1.23 |
| 乙醚 | 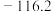 | 34.6 | 微溶于水 | 0.7134 |
(1)实验室用苯制取硝基苯的化学方程式为
(2)往硝基苯中加入
 和足量盐酸充分还原,冷却后,往混合物中加入过量
和足量盐酸充分还原,冷却后,往混合物中加入过量 溶液得碱化液,加
溶液得碱化液,加 溶液的主要目的是析出苯胺,反应的离子方程式为
溶液的主要目的是析出苯胺,反应的离子方程式为(3)分离提纯:
步骤ⅰ.将碱化液蒸馏,收集到苯胺与水的混合物,分液得粗苯胺和水溶液;
步骤ⅱ.步骤ⅰ所得水溶液中加
 至饱和,用乙醚萃取得萃取液与粗苯胺合并:
至饱和,用乙醚萃取得萃取液与粗苯胺合并:步骤ⅲ。合并溶液用干燥剂干燥,过滤,将滤液蒸馏并收集温度
 时的馏分得到苯胺。
时的馏分得到苯胺。①步骤ⅰ蒸馏不需温度计控制温度,试依据收集馏分的特点,分析原因是
②步骤ⅱ萃取分液操作过程中要远离明火及热源,原因是
a.浓硫酸 b.五氧化二磷 c.
 固体
固体③步骤ⅲ中蒸馏获得苯胺的温度
 的范围为
的范围为(4)二次纯化:
苯胺中混有少量硝基苯杂质,可以采用如下方案除杂提纯:

试剂
 是
是 是
是
更新时间:2021-07-09 16:51:52
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】Glaser反应是指端炔烃在催化剂存在下可发生偶联反应,例如: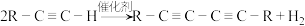
下面是利用Glaser反应制备化合物E的一种合成路线:
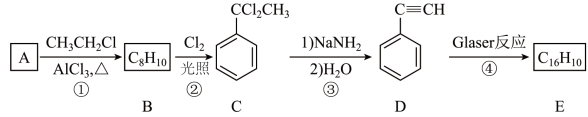
回答下列问题:
(1)最简单的芳香烃 的结构简式为
的结构简式为_______ ,D的化学名称为_______ 。
(2)步骤②的反应化学方程式:_______ 。
(3) 的结构简式为
的结构简式为_______ 。用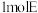 和氢气反应合成
和氢气反应合成 二苯基丁烷,理论上需要消耗氢气
二苯基丁烷,理论上需要消耗氢气_______ mol。
(4)芳香化合物 是
是 的同分异构体,其分子中只有两种不同化学环境的氢原子,数目比为
的同分异构体,其分子中只有两种不同化学环境的氢原子,数目比为 ,符合条件的
,符合条件的 有5种,分别为
有5种,分别为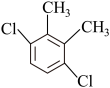 、
、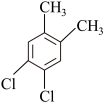 、
、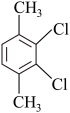 、
、_______ 、_______
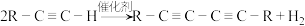
下面是利用Glaser反应制备化合物E的一种合成路线:

回答下列问题:
(1)最简单的芳香烃
 的结构简式为
的结构简式为(2)步骤②的反应化学方程式:
(3)
 的结构简式为
的结构简式为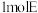 和氢气反应合成
和氢气反应合成 二苯基丁烷,理论上需要消耗氢气
二苯基丁烷,理论上需要消耗氢气(4)芳香化合物
 是
是 的同分异构体,其分子中只有两种不同化学环境的氢原子,数目比为
的同分异构体,其分子中只有两种不同化学环境的氢原子,数目比为 ,符合条件的
,符合条件的 有5种,分别为
有5种,分别为 、
、 、
、 、
、
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐2】苯环上原有的取代基对新导入苯环上的取代基的位置有一定影响,其规律是:
①苯环上新导入的取代基所占的位置主要决定于原有取代基的性质。
②可以把原有取代基分成两类:第一类如:―OH,―X(Cl,Br),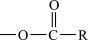 ,—R等,可使新导入的取代基进入苯环的邻位和对位;第二类如—NO2、—SO3H、—CHO等,可使新导入的取代基进入苯环的间位。当第一类和第二类同时存在时,以第一类为准。
,—R等,可使新导入的取代基进入苯环的邻位和对位;第二类如—NO2、—SO3H、—CHO等,可使新导入的取代基进入苯环的间位。当第一类和第二类同时存在时,以第一类为准。
(1)请写出图中第②步反应的化学方程式及C的结构简式。
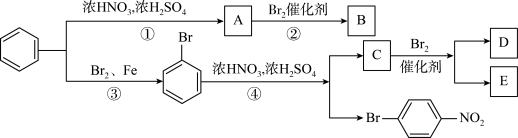
②的化学方程式是____________________ 。
(2)C的结构简式为______________________ 。
(3)写出同分异构体D、E的结构简式:D_________ ;E_________ 。
①苯环上新导入的取代基所占的位置主要决定于原有取代基的性质。
②可以把原有取代基分成两类:第一类如:―OH,―X(Cl,Br),
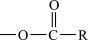 ,—R等,可使新导入的取代基进入苯环的邻位和对位;第二类如—NO2、—SO3H、—CHO等,可使新导入的取代基进入苯环的间位。当第一类和第二类同时存在时,以第一类为准。
,—R等,可使新导入的取代基进入苯环的邻位和对位;第二类如—NO2、—SO3H、—CHO等,可使新导入的取代基进入苯环的间位。当第一类和第二类同时存在时,以第一类为准。(1)请写出图中第②步反应的化学方程式及C的结构简式。

②的化学方程式是
(2)C的结构简式为
(3)写出同分异构体D、E的结构简式:D
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知:R—NO2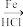 R—NH2,以下是用苯作原料制备一系列化合物的转化关系图:
R—NH2,以下是用苯作原料制备一系列化合物的转化关系图:
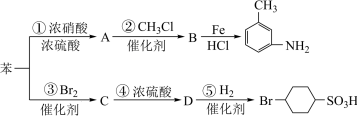
(1)苯转化为A的化学方程式是______________________________________________ 。
(2)B的结构简式为_______________ 。
(3)有机物C的所有原子______ (填“是”或“不是”)在同一平面上。
(4)D分子苯环上的一氯代物有_________ 种。
(5)在上述反应①②③④⑤中,属于取代反应的是_______________________ 。
 R—NH2,以下是用苯作原料制备一系列化合物的转化关系图:
R—NH2,以下是用苯作原料制备一系列化合物的转化关系图:
(1)苯转化为A的化学方程式是
(2)B的结构简式为
(3)有机物C的所有原子
(4)D分子苯环上的一氯代物有
(5)在上述反应①②③④⑤中,属于取代反应的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上用粗CuO制备CuCl2晶体的流程如下:

各种离子相关数据如下:
请回答:
(1)CuO溶于盐酸的离子方程式是_______________ 。
(2)已知NaClO为强氧化剂,能将Fe2+氧化为Fe3+。
① NaClO溶液显_______ 性(填“酸”或“碱”)。你认为用NaClO作氧化剂X是否妥当__________ (填“是”或“否”),理由是__________ 。
②下列另有几种常用的氧化剂,可用作氧化剂X的是__________ 。
a 浓H2SO4 b C12 c H2O2
(3)试剂Y的作用是调节溶液的pH=3.2,将Fe3+转化为Fe(OH)3沉淀,过滤后得到CuCl2溶液。下列试剂中适宜的是___________ 。
a NaOH b Na2CO3 c CuCO3 d CuO
(4)为了得到符合质量标准的CuCl2溶液,必须控制溶液的pH____________ 。

各种离子相关数据如下:
| Fe2+ | Cu2+ | Fe3+ | |
| 开始转化成氢氧化物沉淀时的pH | 7.0 | 4.7 | 1.9 |
| 完全转化成氢氧化物沉淀时的pH | 9.0 | 6.7 | 3.2 |
请回答:
(1)CuO溶于盐酸的离子方程式是
(2)已知NaClO为强氧化剂,能将Fe2+氧化为Fe3+。
① NaClO溶液显
②下列另有几种常用的氧化剂,可用作氧化剂X的是
a 浓H2SO4 b C12 c H2O2
(3)试剂Y的作用是调节溶液的pH=3.2,将Fe3+转化为Fe(OH)3沉淀,过滤后得到CuCl2溶液。下列试剂中适宜的是
a NaOH b Na2CO3 c CuCO3 d CuO
(4)为了得到符合质量标准的CuCl2溶液,必须控制溶液的pH
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某课外研究性学习小组拟用粗盐(含有少量杂质包括:泥沙、CaCl2、MgCl2、Na2SO4)经提纯后,配制0.4mol/L 450mL NaCl溶液.他们设计并实施了如下实验,请根据已学过的知识回答下列问题:
(1)取一定量的粗盐置于烧杯中加适量的水溶解。将配制的粗盐悬浊液过滤后取滤液加入过量的除杂试剂,如果除杂试剂可从下列六种溶液中选择①Na2CO3溶液②KOH溶液③AgNO3溶液④NaOH溶液⑤NaHCO3溶液⑥BaCl2溶液,则正确的试剂和加入的顺序应为:__________ (填选项)
A.①②③ B.②⑥⑤ C.④⑥① D.①④⑥ E.⑥①④ F.⑥②⑤
(2)将所得的悬浊液经过滤后取滤液加入足量的盐酸,充分反应后对混合溶液进行蒸发、过滤、洗涤、干燥操作,得到纯净的NaCl固体,请描述在蒸发操作过程中玻璃棒的作用:_______________________________________________________
(3)利用(2)中所得的NaCl固体继续配制所需溶液.在托盘天平上称量____ g NaCl固体.配制过程中需要使用的玻璃仪器有:烧杯、玻璃棒、_________
和_______________
(4)配制结束后同学们对实验中出现的某些错误操作,对最终配制的溶液浓度的影响进行了分析,则下列错误操作会导致最终配制溶液中NaCl的浓度相比0.4mol/L是偏小的是__________
A.在上述(2)步中没有使用盐酸处理滤液;
B.在上述(3)步中没有对烧杯和玻璃棒进行洗涤;
C.定容时俯视凹液面;
D.上下颠倒摇匀后液面低于刻度线,未及时加水至刻度线。
(1)取一定量的粗盐置于烧杯中加适量的水溶解。将配制的粗盐悬浊液过滤后取滤液加入过量的除杂试剂,如果除杂试剂可从下列六种溶液中选择①Na2CO3溶液②KOH溶液③AgNO3溶液④NaOH溶液⑤NaHCO3溶液⑥BaCl2溶液,则正确的试剂和加入的顺序应为:
A.①②③ B.②⑥⑤ C.④⑥① D.①④⑥ E.⑥①④ F.⑥②⑤
(2)将所得的悬浊液经过滤后取滤液加入足量的盐酸,充分反应后对混合溶液进行蒸发、过滤、洗涤、干燥操作,得到纯净的NaCl固体,请描述在蒸发操作过程中玻璃棒的作用:
(3)利用(2)中所得的NaCl固体继续配制所需溶液.在托盘天平上称量
和
(4)配制结束后同学们对实验中出现的某些错误操作,对最终配制的溶液浓度的影响进行了分析,则下列错误操作会导致最终配制溶液中NaCl的浓度相比0.4mol/L是偏小的是
A.在上述(2)步中没有使用盐酸处理滤液;
B.在上述(3)步中没有对烧杯和玻璃棒进行洗涤;
C.定容时俯视凹液面;
D.上下颠倒摇匀后液面低于刻度线,未及时加水至刻度线。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有KNO3样品(含有少量杂质KCl、K2SO4),选择适当的试剂除去杂质,从而得到纯净的KNO3晶体,相应的实验流程如图所示。
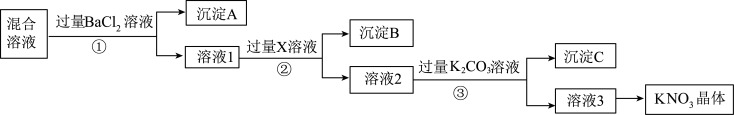
请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X__ ,沉淀C__ 、__ 。
(2)上述实验流程中①②③步均要进行的实验操作是__ (填操作名称)。
(3)生成沉淀A的离子方程式是__ 。
(4)此实验方案存在缺陷,还应__ ,之后若要获得纯净的KNO3晶体,需进行的实验操作是__ 、__ (填操作名称)。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X
(2)上述实验流程中①②③步均要进行的实验操作是
(3)生成沉淀A的离子方程式是
(4)此实验方案存在缺陷,还应
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】间溴苯甲醛常用作医药中间体,实验室以苯甲醛为原料,在无水AlCl3催化下加热制备间溴苯甲醛。
I.催化剂的制备
如图1是实验室制取少量无水AlCl3的相关实验装置。已知无水氯化铝易升华,极易潮解。
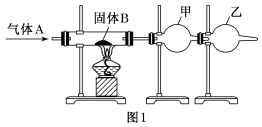
(1)若气体A是Cl2,且由KMnO4和浓盐酸反应制取,该反应的离子方程式为_______ 。
(2)若固体B是AlCl3·6H2O,则气体A是_______ ,通入气体A的目的是_______ 。
(3)若气体A为Cl2,乙中的药品是碱石灰,则碱石灰的作用是___________ 。
II.间溴苯甲醛的制备
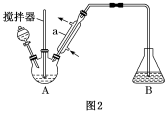
实验所用装置如图2(夹持及加热装置已省略):
已知相关物质的沸点如下表所示:
实验步骤如下:
步骤1:将一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛在三颈烧瓶中充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,维持温度不变,反应一段时间后,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10%NaHCO3溶液洗涤。
步骤3:往洗涤后的有机相中加入适量无水MgSO4固体,放置一段时间后,进行下一操作。
步骤4:减压蒸馏有机相,收集相应馏分。
(4)仪器a的名称为___________ ,本实验需要控制反应温度为60℃,为了更好地控制反应温度,宜采用的加热方式是___________ 。
(5)步骤2分液时有机相处于___________ (填“上层”或“下层”),NaHCO3可以除去有机相中的Br2,反应中1molBr2参与反应,转移1mol电子且产生无色气体,反应的离子方程式为_______ 。
(6)步骤3中将加入无水MgSO4固体的有机相放置一段时间后,进行的下一操作是_______ 。
I.催化剂的制备
如图1是实验室制取少量无水AlCl3的相关实验装置。已知无水氯化铝易升华,极易潮解。

(1)若气体A是Cl2,且由KMnO4和浓盐酸反应制取,该反应的离子方程式为
(2)若固体B是AlCl3·6H2O,则气体A是
(3)若气体A为Cl2,乙中的药品是碱石灰,则碱石灰的作用是
II.间溴苯甲醛的制备
实验所用装置如图2(夹持及加热装置已省略):

已知相关物质的沸点如下表所示:
| 物质 | 沸点/℃ |
| 液溴 | 58.8 |
| 苯甲醛 | 179 |
| 1,2-二氯乙烷 | 83.5 |
| 间溴苯甲醛 | 229 |
步骤1:将一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛在三颈烧瓶中充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,维持温度不变,反应一段时间后,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10%NaHCO3溶液洗涤。
步骤3:往洗涤后的有机相中加入适量无水MgSO4固体,放置一段时间后,进行下一操作。
步骤4:减压蒸馏有机相,收集相应馏分。
(4)仪器a的名称为
(5)步骤2分液时有机相处于
(6)步骤3中将加入无水MgSO4固体的有机相放置一段时间后,进行的下一操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】2-甲基-2-己醇常用于合成洗涤剂、乳化剂等。实验室制备2-甲基-2-己醇的流程如下:
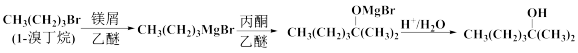
已知:RMgBr化学性质活泼,易与H2O、R'X 等发生反应生成RH、R-R'。
(1)仪器A的名称是___________ 。
(2)引发CH3(CH2)3Br 与镁屑反应可微热或加入米粒大小的碘单质,其中碘的作用可能是_____ ,若镁屑不足,则反应时生成的有机副产物为________ (填结构简式)。
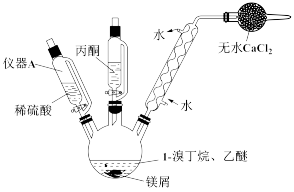
(3) 干燥管中无水氯化钙的作用为__________ 。
(4)加入丙酮及稀硫酸时均需用冰水冷却,这是因为_________ 。
(5)起始加入三颈烧瓶的1-溴丁烷的体积为5 mL,密度为1.28g/mL,最终所得产品的质量为2.71g,则2-甲基-2-己醇的产率为________ 。
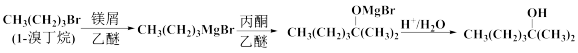
已知:RMgBr化学性质活泼,易与H2O、R'X 等发生反应生成RH、R-R'。
(1)仪器A的名称是
(2)引发CH3(CH2)3Br 与镁屑反应可微热或加入米粒大小的碘单质,其中碘的作用可能是

(3) 干燥管中无水氯化钙的作用为
(4)加入丙酮及稀硫酸时均需用冰水冷却,这是因为
(5)起始加入三颈烧瓶的1-溴丁烷的体积为5 mL,密度为1.28g/mL,最终所得产品的质量为2.71g,则2-甲基-2-己醇的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】实验室由安息香制备二苯乙二酮的反应式如下:
装置示意图所示,实验步骤为:
①在圆底烧瓶中加入10mL冰乙酸、5mL水及9.0gFeCl3∙6H2O,边搅拌边加热,至固体全部溶解。
②停止加热,待沸腾平息后加入2.0g安息香,加热回流45~60min。
③加入50mL水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶1.6g。
回答下列问题:___________ ;其作用是___________ ,冷却水应从___________ (填“a”或“b”)口通入。
(2)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是___________ 。
(3)冷水洗涤固体的目的是为了洗去___________ 。
(4)在本实验中,FeCl3为氧化剂且过量,其还原产物为___________ ;某同学尝试采用少量的FeCl3并通入空气也可制得二苯乙二酮。简述该方案可行的理由___________ 。
(5)若粗品中混有少量未氧化的安息香,可用少量___________ 洗涤的方法除去(填标号)。若要得到更高纯度的产品,可用重结晶的方法进一步提纯。
a.热水 b.乙酸 c.冷水 d.乙醇
(6)本实验的产率最接近于___________ (填标号)。
a.85% b.80% c.75% d.70%
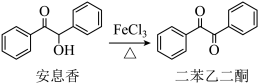
| 物质 | 性状 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 安息香 | 白色固体 | 133 | 344 | 难溶于冷水 溶于热水、乙醇、乙酸 |
| 二苯乙二酮 | 淡黄色固体 | 95 | 347 | 不溶于水 溶于乙醇、苯、乙酸 |
| 冰乙酸 | 无色液体 | 17 | 118 | 与水、乙醇互溶 |
①在圆底烧瓶中加入10mL冰乙酸、5mL水及9.0gFeCl3∙6H2O,边搅拌边加热,至固体全部溶解。
②停止加热,待沸腾平息后加入2.0g安息香,加热回流45~60min。
③加入50mL水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶1.6g。
回答下列问题:
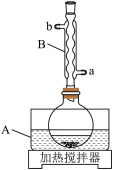
(2)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是
(3)冷水洗涤固体的目的是为了洗去
(4)在本实验中,FeCl3为氧化剂且过量,其还原产物为
(5)若粗品中混有少量未氧化的安息香,可用少量
a.热水 b.乙酸 c.冷水 d.乙醇
(6)本实验的产率最接近于
a.85% b.80% c.75% d.70%
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
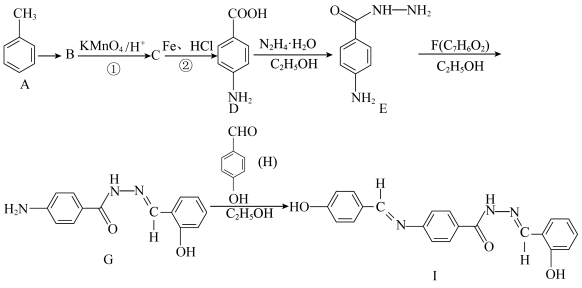
【推荐1】席夫碱化合物具有结构多样、性质稳定的特点,且具有良好的与金属离子配位的能力,因此是一类重要的荧光探针分子。一种合成含席夫碱结构的新型Zn2+荧光探针P1 (化合物Ⅰ)的流程如图所示。请回答下列问题:
已知: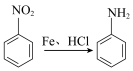 (苯胺易被氧化)。
(苯胺易被氧化)。
(1)A中碳原子的杂化方式为___________ 。
(2)A→B 的反应类型为___________ ,D的名称为___________ 。
(3)反应①和反应②的顺序___________ (填“能”或“否”)调换,说明理由:___________ 。
(4)已知 G→Ⅰ涉及两步反应,第一步是加成反应,第二步是消去反应,写出由 G→Ⅰ的化学方程式:___________ 。
(5)F 的结构简式为___________ 。
(6) 化合物J与H互为同系物,J的相对分子质量比H大28,则满足下列条件的J的芳香族同分异构体有___________ 种,其中核磁共振氢谱有4组峰,且峰面积之比为 6:2:1:1 的结构简式为___________ (任写一种)。
①能够发生银镜反应;
②能够发生水解反应。

已知:
 (苯胺易被氧化)。
(苯胺易被氧化)。(1)A中碳原子的杂化方式为
(2)A→B 的反应类型为
(3)反应①和反应②的顺序
(4)已知 G→Ⅰ涉及两步反应,第一步是加成反应,第二步是消去反应,写出由 G→Ⅰ的化学方程式:
(5)F 的结构简式为
(6) 化合物J与H互为同系物,J的相对分子质量比H大28,则满足下列条件的J的芳香族同分异构体有
①能够发生银镜反应;
②能够发生水解反应。
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】雷诺嗪H是一种抗心绞痛药物,它的一种合成路线如下:
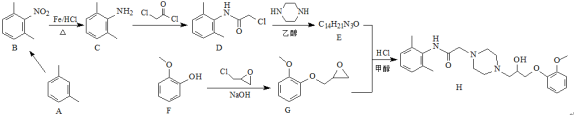
回答下列问题:
(1)F中官能团的名称是___________ 。
(2)B→C的反应类型是___________ ,F→G的反应类型是___________ 。
(3)A→B的反应条件是___________ ;E的结构简式为___________ 。
(4)C→D的化学方程式为___________ 。
(5)同时满足下列三个条件的D的同分异构体有8种。其中氮原子上全部连接饱和碳原子的同分异构体结构简式为___________ 。
①含有苯环②含有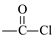 ③核磁共振氢谱有4组峰且峰面积之为1:1:1:3
③核磁共振氢谱有4组峰且峰面积之为1:1:1:3

回答下列问题:
(1)F中官能团的名称是
(2)B→C的反应类型是
(3)A→B的反应条件是
(4)C→D的化学方程式为
(5)同时满足下列三个条件的D的同分异构体有8种。其中氮原子上全部连接饱和碳原子的同分异构体结构简式为
①含有苯环②含有
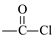 ③核磁共振氢谱有4组峰且峰面积之为1:1:1:3
③核磁共振氢谱有4组峰且峰面积之为1:1:1:3
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:
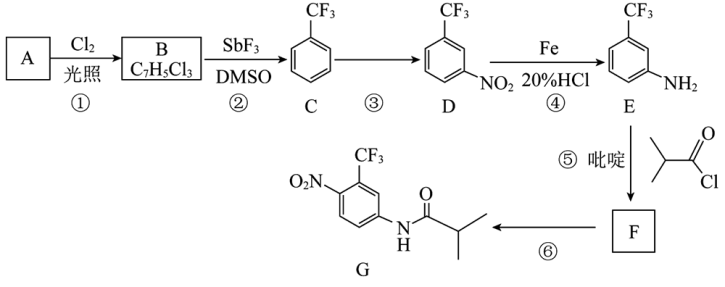
回答下列问题:
(1)A的结构简式为_______ 。C苯环上的一氯代物有几种_______ 。
(2)③的反应试剂和反应条件分别是_______ ,该反应的类型是 _______ 。
(3)⑤的反应方程式为_______ 。吡啶是一种有机碱,其作用是_______ 。
(4)G的分子式为_______ 。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,写出H的一种结构简式_______ 。

回答下列问题:
(1)A的结构简式为
(2)③的反应试剂和反应条件分别是
(3)⑤的反应方程式为
(4)G的分子式为
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,写出H的一种结构简式
您最近一年使用:0次



