W、Q、X、Y、Z属于周期表中前20号元素,且原子序数依次增大。W元素最外层电子数是次外层的3倍,Q是所在周期中原子半径最大的元素,X是地壳中含量最高的金属元素,Y元素最高化合价与最低化合价之和为4,Z和Q同主族。下列判断正确的是
A.原子半径: |
B.简单氢化物的热稳定性: |
C.最高价氧化物对应水化物的碱性: |
| D.Q、Y、X最高价氧化物对应水化物两两之间均能反应 |
更新时间:2021-07-20 09:22:32
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1~36号元素)。对比中学常见元素周期表,思考扇形元素周期表的填充规律,下列说法正确的是


| A.②⑧⑨对应简单离子的半径依次减小 |
| B.⑥的金属性比⑦的金属性弱 |
| C.元素⑩位于常见元素周期表第四周期VIII族 |
| D.①与③④⑤均可形成化合物 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】一种广泛用于锂离子电池的物质。其结构如图所示。X、Y、Z、W为原子序数依次递增的四种短周期元素,Y、W同主族,原子半径r(X)>r(Y)>r(Z)。下列说法正确的是( )

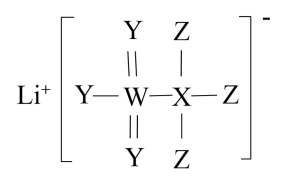

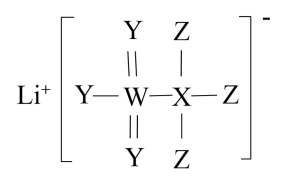
| A.电负性X<Y<Z |
| B.简单氢化物的沸点W>Z>Y>X |
| C.Y、Z、W的单质是相同的晶体类型 |
| D.简单氢化物的热稳定性Y>W>Z |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】我国最早报道的超高温导体中,铊是重要组成之一。已知铊是ⅢA族元素,关于铊的性质判断值得怀疑的是
| A.金属铊可以作为半导体材料 | B.能生成+3价的化合物 |
| C.Tl(OH)3的碱性比Al(OH)3强 | D.Tl(OH)3 与Al(OH)3一样是两性氢氧化物 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】锶(Sr)为第五周期IIA族元素,其化合物六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4,含少量BaSO4)为原料制备,生产流程如下:
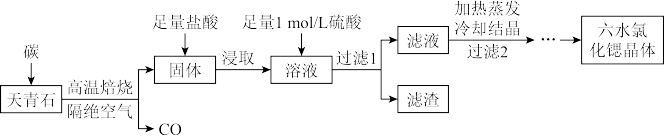
下列叙述不正确的是

下列叙述不正确的是
| A.锶的金属性比钙的强,所以SrSO4的溶解性比CaSO4的强 |
B.高温焙烧时,若0.5molSrSO4完全反应转移了4mol电子,该反应的化学方程式为:SrSO4+4C SrS+4CO SrS+4CO |
| C.加入适量1mol/LH2SO4目的是除去溶液中Ba2+杂质 |
| D.工业上常电解熔融SrCl2制锶单质,则SrCl2·6H2O制取无水SrCl2一定要在无水氯化氢气流中加热SrCl2·6H2O失水恒重 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是周期表中的原子半径最小的元素,Y元素的最高正价与最低负价的绝对值相等,Z的核电荷数是Y的2倍,W的最外层电子数是其最内层电子数的3倍。下列说法不正确的是
| A.原子半径:Z>W>R |
| B.W、R对应的简单氢化物的稳定性前者大于后者 |
| C.W与X、W与Z形成的化合物的化学键类型完全相同 |
| D.电负性R>Y、X |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】 X、Y、Z、M、W为五种短周期元素.X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的一半。下列说法正确的是
| A.原子半径:W>Z>Y>X>M |
| B.将XZ2通入W单质与水反应后的溶液中,一定只生成碳酸钠、碳酸氢钠 |
| C.由X、Y、Z、M四种元素形成的化合物中一定有共价键可能有离子键 |
| D.CaZ2、CaM2、CaZ2等3种化合物中,阳离子和阴离子个数比均为1:2 |
您最近一年使用:0次

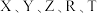 为短周期主族元素,其中R原子的最外层电子数是电子层数的2倍;Y与Z能形成
为短周期主族元素,其中R原子的最外层电子数是电子层数的2倍;Y与Z能形成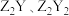 型离子化合物,Y与T同主族。五种元素原子半径与原子序数之间的关系如图所示。下列推断正确的是
型离子化合物,Y与T同主族。五种元素原子半径与原子序数之间的关系如图所示。下列推断正确的是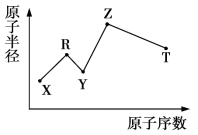
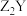 和
和 的阴阳离子个数比相同
的阴阳离子个数比相同

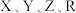 四种元素组成的常见化合物溶液显酸性
四种元素组成的常见化合物溶液显酸性 能级成对电子数与未成对电子数相等;Q电子总数是最外层电子的3倍;R是用量最大使用最广泛的金属。下列说法正确的是
能级成对电子数与未成对电子数相等;Q电子总数是最外层电子的3倍;R是用量最大使用最广泛的金属。下列说法正确的是


