以下12种物质为中学化学中常见的物质:①Cu②FeCl3溶液③NaHSO4固体④SO2⑤石墨⑥C2H5OH⑦CH3COOH⑧氨水⑨NaHCO3⑩NaOH固体。请按下列分类标准回答问题:
(1)能导电的物质是_______ (填序号)
(2)属于电解质的是_______ 。(填序号)
(3)写出③在水溶液中的电离方程式_______ 。
(4)上述物质中有两种物质在水溶液中可发生离子反应:H++OH-=H2O,写出该反应的化学方程式_______ 。
(5)23gC2H5OH的物质的量为_______ ,共含有_______ 个H原子,与_______ molSO2中所含氧原子数相同。
(1)能导电的物质是
(2)属于电解质的是
(3)写出③在水溶液中的电离方程式
(4)上述物质中有两种物质在水溶液中可发生离子反应:H++OH-=H2O,写出该反应的化学方程式
(5)23gC2H5OH的物质的量为
更新时间:2021-07-28 21:28:28
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】现有mgX元素的单质气体 (其摩尔质量为Mg/mol)。若阿伏加德罗常数的数值用NA表示,则:
(其摩尔质量为Mg/mol)。若阿伏加德罗常数的数值用NA表示,则:
(1)该气体的物质的量为___________ mol。
(2)该气体所含原子总数为___________ 。
(3)该气体在标准状况下的体积为___________ L。
(4)该气体全部溶于1L水中(不考虑与水反应,水的密度为1g/cm3),其溶液中溶质的质量分数为___________ 。
(5)X元素的另一单质气体 与
与 的关系是
的关系是___________ 。mg 气体的物质的量为
气体的物质的量为___________ mol,所含原子总数为___________ 。
 (其摩尔质量为Mg/mol)。若阿伏加德罗常数的数值用NA表示,则:
(其摩尔质量为Mg/mol)。若阿伏加德罗常数的数值用NA表示,则:(1)该气体的物质的量为
(2)该气体所含原子总数为
(3)该气体在标准状况下的体积为
(4)该气体全部溶于1L水中(不考虑与水反应,水的密度为1g/cm3),其溶液中溶质的质量分数为
(5)X元素的另一单质气体
 与
与 的关系是
的关系是 气体的物质的量为
气体的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题。
(1)已知硫酸钠晶体(Na2SO4·10H2O)的物质的量为0.5 mol,则所含钠离子的物质的量是___________ ,钠离子的数目是___________ ,所含硫酸根离子的物质的量是___________ 。
(2)18克水的物质的量为___________ ,其中含有H的原子的数目约为多少___________ 。
(1)已知硫酸钠晶体(Na2SO4·10H2O)的物质的量为0.5 mol,则所含钠离子的物质的量是
(2)18克水的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】填空。
(1)4.5gH2O与_____ gH2SO4所含的分子数相等,它们所含氧原子数之比是_______ 。
(2)14g氮气在标准状况下的体积为________ ,含有的原子的数目为_______ 。
(3)现有标况下CO和CO2混合气体6.72L,其质量为10.8g,则此混合气体中,CO和CO2的物质的量之比为______ 。
(4)NO和O2发生反应:2NO+O2=2NO2,现有amolNO和bmolO2充分反应后氮原子与氧原子的个数比为______ 。
(1)4.5gH2O与
(2)14g氮气在标准状况下的体积为
(3)现有标况下CO和CO2混合气体6.72L,其质量为10.8g,则此混合气体中,CO和CO2的物质的量之比为
(4)NO和O2发生反应:2NO+O2=2NO2,现有amolNO和bmolO2充分反应后氮原子与氧原子的个数比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)标准状况下,1.92g某气体的体积为672mL,则此气体的相对分子质量为______ 。
(2)在25℃、101kPa的条件下,相同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为______ 。
(3)两个相同容积的密闭容器X、Y,在25℃下,X中充入agA气体,Y中充入agCH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为______ 。
(1)标准状况下,1.92g某气体的体积为672mL,则此气体的相对分子质量为
(2)在25℃、101kPa的条件下,相同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为
(3)两个相同容积的密闭容器X、Y,在25℃下,X中充入agA气体,Y中充入agCH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】H2O2是重要的化工原料。
(1)H2O2中O元素的化合价为______ 。
(2)①向酸性KMnO4溶液中滴加H2O2溶液,溶液褪色,体现了H2O2的还原性,其中氧化过程是:H2O2→______ (填化学式)。
②向H2SO4酸化的FeSO4溶液中滴加H2O2溶液,溶液变成黄色,体现了H2O2的氧化性,反应的离子方程式是_________ 。
(3)H2O2不稳定易分解。实验室需要448 mL O2(标准状况),则理论上最少需要用30%的H2O2溶液(密度为1.10 g/mL)_______ mL。(计算结果保留一位小数)
(1)H2O2中O元素的化合价为
(2)①向酸性KMnO4溶液中滴加H2O2溶液,溶液褪色,体现了H2O2的还原性,其中氧化过程是:H2O2→
②向H2SO4酸化的FeSO4溶液中滴加H2O2溶液,溶液变成黄色,体现了H2O2的氧化性,反应的离子方程式是
(3)H2O2不稳定易分解。实验室需要448 mL O2(标准状况),则理论上最少需要用30%的H2O2溶液(密度为1.10 g/mL)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据所学知识,回答下列问题:
(1)分类在化学学习中起着非常重要的作用,下列分类标准合理的是___________(填标号)。
(2)现有七种物质:①NaCl溶液 ② ③HClO ④蔗糖 ⑤NaOH固体 ⑥稀硫酸 ⑦氢氧化铁胶体。属于混合物的是
③HClO ④蔗糖 ⑤NaOH固体 ⑥稀硫酸 ⑦氢氧化铁胶体。属于混合物的是___________ (填序号),属于电解质的是___________ (填序号)。制备⑦的化学方程式为___________ 。
(3)化学计量是化学定量研究的基础。
①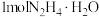 中含有H的个数为
中含有H的个数为___________ 。
② 个
个 分子的物质的量为
分子的物质的量为___________ mol,质量为___________ g。
③等质量的 和
和 ,其物质的量比
,其物质的量比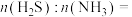
___________ ,标准状况下气体的体积比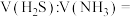
___________ 。
(1)分类在化学学习中起着非常重要的作用,下列分类标准合理的是___________(填标号)。
| A.根据物质溶于水后形成的溶液呈碱性,可将此类物质归类为碱 |
| B.根据物质能否导电,将物质分为电解质和非电解质 |
| C.根据反应中是否有电子的转移,将化学反应分为氧化还原反应和非氧化还原反应 |
| D.根据分散系中分散质粒子的直径大小,将分散系分为溶液、胶体和浊液 |
 ③HClO ④蔗糖 ⑤NaOH固体 ⑥稀硫酸 ⑦氢氧化铁胶体。属于混合物的是
③HClO ④蔗糖 ⑤NaOH固体 ⑥稀硫酸 ⑦氢氧化铁胶体。属于混合物的是(3)化学计量是化学定量研究的基础。
①
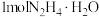 中含有H的个数为
中含有H的个数为②
 个
个 分子的物质的量为
分子的物质的量为③等质量的
 和
和 ,其物质的量比
,其物质的量比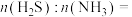
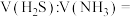
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求回答下列问题:
(1)现有8种物质:A.稀硫酸、B. 溶液、C.CO、D.熔融的
溶液、C.CO、D.熔融的 、E.
、E. 、F.
、F. 胶体、G.
胶体、G. 固体、H.
固体、H. 溶液。
溶液。
①能导电的电解质有___________ (填字母,下同),属于酸性氧化物的有___________ 。
② 溶于水的电离方程式为
溶于水的电离方程式为___________ 。
③实验室用加热饱和 溶液制备
溶液制备 胶体,写出该反应的化学方程式:
胶体,写出该反应的化学方程式:___________ 。
④写出H与足量A反应的化学方程式:___________ 。
(2)甲烷(甲烷中C的化合价为-4)在厌氧氧化菌的作用下,可以和氢氧化铁发生如下反应,配平该离子方程式:________
___________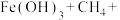 ___________
___________
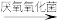 ___________+___________
___________+___________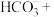 ___________
___________
该反应中的还原剂为___________ (填化学式),被还原的物质与被氧化的物质的物质的量之比为___________ 。
(3)无氧条件下加热蓝铁矿(无杂质),发生反应的化学方程式为 ,蓝铁矿的质量由
,蓝铁矿的质量由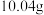 减小到
减小到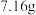 ,则n=
,则n=___________ 。
(1)现有8种物质:A.稀硫酸、B.
 溶液、C.CO、D.熔融的
溶液、C.CO、D.熔融的 、E.
、E. 、F.
、F. 胶体、G.
胶体、G. 固体、H.
固体、H. 溶液。
溶液。①能导电的电解质有
②
 溶于水的电离方程式为
溶于水的电离方程式为③实验室用加热饱和
 溶液制备
溶液制备 胶体,写出该反应的化学方程式:
胶体,写出该反应的化学方程式:④写出H与足量A反应的化学方程式:
(2)甲烷(甲烷中C的化合价为-4)在厌氧氧化菌的作用下,可以和氢氧化铁发生如下反应,配平该离子方程式:
___________
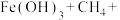 ___________
___________
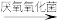 ___________+___________
___________+___________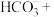 ___________
___________
该反应中的还原剂为
(3)无氧条件下加热蓝铁矿(无杂质),发生反应的化学方程式为
 ,蓝铁矿的质量由
,蓝铁矿的质量由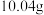 减小到
减小到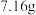 ,则n=
,则n=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在下列物质:A 烧碱 B 硫酸 C 干冰 D 硫酸钡 E 纯碱 F 铁
(1)既不是电解质,也不是非电解质的是_______ 。
(2)纯碱的电离方程式是___________________________ 。
(3)烧碱溶液与稀硫酸混合,发生反应的离子方程式为________________ 。
(4)将干冰升华后所得的气体通入过量烧碱溶液中,发生反应的离子方程式为______ 。
(5)a、b、c、d是Na2CO3、BaCl2、HCl、AgNO3四种溶液中的一种,现将它们两两混合,现象如下表所示:
① b是_________ 用化学式填写)。
② 写出a+c反应的离子方程式_________________ 。
(1)既不是电解质,也不是非电解质的是
(2)纯碱的电离方程式是
(3)烧碱溶液与稀硫酸混合,发生反应的离子方程式为
(4)将干冰升华后所得的气体通入过量烧碱溶液中,发生反应的离子方程式为
(5)a、b、c、d是Na2CO3、BaCl2、HCl、AgNO3四种溶液中的一种,现将它们两两混合,现象如下表所示:
| 反应物 | a+b | c+d | a+d | a+c | b+d |
| 现象 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 无色气体 |
① b是
② 写出a+c反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】有如下物质:①铁丝 ②NaOH溶液 ③ 固体 ④
固体 ④ ⑤酒精 ⑥蒸馏水 ⑦
⑤酒精 ⑥蒸馏水 ⑦ ⑧熔融的
⑧熔融的 ⑨红褐色的氢氧化铁胶体
⑨红褐色的氢氧化铁胶体
(1)以上物质中,属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
(2)已知蒸馏水有非常微弱的导电性,上述物质除⑥外,能导电的是___________ 。
(3)物质③溶于水的电离方程式为___________ 。
(4)向⑨的溶液中逐渐滴加③的溶液,看到的现象是___________ 。
 固体 ④
固体 ④ ⑤酒精 ⑥蒸馏水 ⑦
⑤酒精 ⑥蒸馏水 ⑦ ⑧熔融的
⑧熔融的 ⑨红褐色的氢氧化铁胶体
⑨红褐色的氢氧化铁胶体(1)以上物质中,属于电解质的是
(2)已知蒸馏水有非常微弱的导电性,上述物质除⑥外,能导电的是
(3)物质③溶于水的电离方程式为
(4)向⑨的溶液中逐渐滴加③的溶液,看到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】读题填空
(1)HClO4中Cl的化合价为_______ 价。
(2)写出CuCl2的电离方程式_______ 。
(3)写出Na2SO4与Ba(OH)2反应的离子方程式_______ 。
(4)次磷酸(H3PO2)是一种精细磷化工产品,H3PO2是一元中强酸,NaH2PO2为_______ (填“正盐”或“酸式盐”)。
(5)_______ 是用来区分胶体和溶液的一种常用物理方法。
(1)HClO4中Cl的化合价为
(2)写出CuCl2的电离方程式
(3)写出Na2SO4与Ba(OH)2反应的离子方程式
(4)次磷酸(H3PO2)是一种精细磷化工产品,H3PO2是一元中强酸,NaH2PO2为
(5)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学与生活密切相关,回答下列问题:
(1)豆浆中加入适量胆水(含 等)能形成豆腐,是因为胶体遇电解质发生
等)能形成豆腐,是因为胶体遇电解质发生_____ 。
(2)铁与水难反应,但在高温条件下与水蒸气反应,生成的固体物质为_____ (写化学式)。
(3)明矾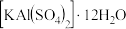 是一种常用净水剂。写出
是一种常用净水剂。写出 溶于水的电离方程式
溶于水的电离方程式_____
(4)“84”消毒液与洁厕灵(主要成分为 )混用会生成有毒的氯气,反应方程式为
)混用会生成有毒的氯气,反应方程式为 。该反应中还原剂是
。该反应中还原剂是_____ ,用双线桥表示该反应中电子转移方向和数目_____
(5)断开1molH-H键、1molN-H键、1molN≡N键分别需要吸收能量为436kJ、391kJ、946kJ,则1molH2与足量N2反应生成NH3需_____ (填“吸收”或“放出”)能量______ kJ。(小数点后保留两位数字),事实上,反应的热量总小于理论值,理由是______ 。
(1)豆浆中加入适量胆水(含
 等)能形成豆腐,是因为胶体遇电解质发生
等)能形成豆腐,是因为胶体遇电解质发生(2)铁与水难反应,但在高温条件下与水蒸气反应,生成的固体物质为
(3)明矾
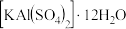 是一种常用净水剂。写出
是一种常用净水剂。写出 溶于水的电离方程式
溶于水的电离方程式(4)“84”消毒液与洁厕灵(主要成分为
 )混用会生成有毒的氯气,反应方程式为
)混用会生成有毒的氯气,反应方程式为 。该反应中还原剂是
。该反应中还原剂是(5)断开1molH-H键、1molN-H键、1molN≡N键分别需要吸收能量为436kJ、391kJ、946kJ,则1molH2与足量N2反应生成NH3需
您最近一年使用:0次



