工业上常用FeSO4溶液处理废水中的重铬酸根离子(Cr2O ),反应原理为:6Fe2++Cr2O
),反应原理为:6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O。处理25.00mL某废水,需消耗15.00mL1.00×10-2mol/LFeSO4溶液(不考虑其他物质与Fe2+反应)。该废水中Cr2O
+14H+=6Fe3++2Cr3++7H2O。处理25.00mL某废水,需消耗15.00mL1.00×10-2mol/LFeSO4溶液(不考虑其他物质与Fe2+反应)。该废水中Cr2O 的物质的量浓度(单位:mol/L)为
的物质的量浓度(单位:mol/L)为
 ),反应原理为:6Fe2++Cr2O
),反应原理为:6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O。处理25.00mL某废水,需消耗15.00mL1.00×10-2mol/LFeSO4溶液(不考虑其他物质与Fe2+反应)。该废水中Cr2O
+14H+=6Fe3++2Cr3++7H2O。处理25.00mL某废水,需消耗15.00mL1.00×10-2mol/LFeSO4溶液(不考虑其他物质与Fe2+反应)。该废水中Cr2O 的物质的量浓度(单位:mol/L)为
的物质的量浓度(单位:mol/L)为| A.1.50×10-4 | B.6.00×10-4 | C.1.00×10-3 | D.3.60×10-3 |
2021高一下·浙江·学业考试 查看更多[11]
四川省眉山市仁寿县2023-2024学年高一上学期1月期末化学试题江西省景德镇一中2022-2023学年高二下学期期中考试(18班)化学试题(已下线)【2022】【高一化学】【期中考】-182浙江省宁波市北仑中学2022-2023学年高一下学期期初返校考试化学(学考)试题(已下线)专题03 物质的量的基本计算-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)上海市民立中学2022-2023学年高一上学期期末考试化学试题上海市曹杨第二中学2022-2023学年高一上学期总结性评价化学试题浙江省丽水外国语学校高中部2021-2022学年高一下学期第一次阶段性考试(3月)化学试题浙江省金华市曙光学校2021-2022学年高一上学期第二次阶段考试化学试题浙江省宁波市三锋教研联盟2021-2022学年高一上学期11月期中考试化学试题2021年7月浙江省普通高中学业水平考试化学试题
更新时间:2021-08-07 21:37:21
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.等质量的质量分数均为4%的氢氧化钠溶液与稀盐酸充分反应后,所得溶液显中性 |
| B.等质量的Al和Mg分别与足量稀硫酸充分反应,生成H2的质量相等 |
| C.等质量的NaHCO3和MgCO3分别与足量稀盐酸充分反应,生成CO2的质量相等 |
| D.等质量的CO和CO2,CO和CO2中氧元素的质量比为1:2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】现向 含有
含有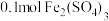 和
和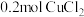 的某混合溶液中加入
的某混合溶液中加入 ,充分反应后(忽略溶液体积变化),下列说法正确的是
,充分反应后(忽略溶液体积变化),下列说法正确的是
 含有
含有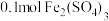 和
和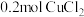 的某混合溶液中加入
的某混合溶液中加入 ,充分反应后(忽略溶液体积变化),下列说法正确的是
,充分反应后(忽略溶液体积变化),下列说法正确的是A.析出 | B.剩余 |
C.溶液中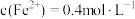 | D.反应后溶液中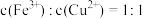 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】当物质的量浓度相同的NaCl、 MgCl2、AlCl3三种溶液中所含Cl-个数比为1:1:1时,这三种溶液的体积比应是
| A.3:2:1 | B.1:2:3 | C.6:3:2 | D.2:3:6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】阿伏加德罗常数的值为NA,下列说法正确的是
| A.在常温常压下,1molHe分子中含有的原子数目为2NA |
| B.常温下,28gN2和CO混合气体中原子个数为NA |
| C.20℃、1.0×105Pa时,同体积的O2与CO2含有相同的氧原子数 |
| D.将NA个NH3溶于1L水中,所得溶液中NH3的物质的量浓度为1mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】水体中过量氨氮(以NH3表示)含量过高会导致水体富营养化。用次氯酸钠除去氨氮的一种原理如图所示。下列说法正确的是

| A.过程①②③均属于氧化还原反应 |
B.该过程的总反应为: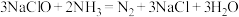 |
| C.过程②中氧化剂与还原剂的个数之比是2:3 |
| D.在较高温度下,氨氮去除率会更好 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知Fe溶于一定浓度HNO3溶液中,反应的离子方程式为aFe+bNO3-+cH+=dFe2++fFe3++gNO↑+hN2O↑+kH2O,方程式中化学计量数均为正整数,则它们之间的关系错误的是
| A.c=4g+10h | B.c-b=2d+3f | C.2d+3f=3g+8h | D.a+c=d+f |
您最近一年使用:0次

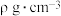 ,质量分数为w%,溶液中含NaCl的质量为m g。则下列表达式正确的是
,质量分数为w%,溶液中含NaCl的质量为m g。则下列表达式正确的是

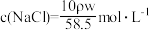
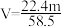
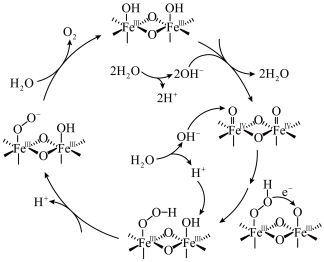
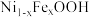 作光催化剂,通过以下转化途径,显著提升光催化水氧化反应速率,为太阳能的高效利用提供了新的策略。下列有关说法正确的是
作光催化剂,通过以下转化途径,显著提升光催化水氧化反应速率,为太阳能的高效利用提供了新的策略。下列有关说法正确的是