下列溶液中,一定能大量共存的离子组是
A.pH=1的溶液中:Na+、Mg2+、SO 、HCO 、HCO |
B.含有大量Fe3+的溶液中:Al3+、Cu2+、Cl-、SO |
C.加入Al能放出H2的溶液中:K+、NH 、NO 、NO 、C1- 、C1- |
D.水电离产生的c(H+)=10-12mol/L-1的溶液:K+、Ba2+、NO 、OH- 、OH- |
2010高二·安徽·竞赛 查看更多[2]
第24届(2010年)全国高中学生化学竞赛(安徽赛区)初赛试题(已下线)3.2.1 水的电离 溶液的酸碱性(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)
更新时间:2021-08-13 10:42:51
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列各组离子在特定条件下一定能够大量共存的是
| A.含有较多Fe3+的溶液:Na+、SO42-、HS-、NH4+ |
| B.c(OH-)=1mol/L的溶液:AlO2-、CH3COO-、K+、Ba2+ |
| C.pH=1的溶液:K+、Fe2+、NO3-、Na+ |
| D.遇Al能放出H2的溶液:HCO3-、K+、Mg2+、Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列各组离子一定能大量共存的是
| A.在含有大量[Al(OH)4]-溶液中NH4+、Na+、Cl-、H+ |
| B.在能使pH试纸变蓝的溶液中Na+、K+、CO32-、NO3- |
| C.在由水电离的OH-浓度为10-13的溶液中NH4+、Na+、SO42-、Cl- |
| D.滴加KSCN显红色的溶液:NH4+、K+、Cl-、I- |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】向一定量的Fe、FeO和 的混合物中加入
的混合物中加入 的稀硝酸,恰好使混合物完全溶解,放出
的稀硝酸,恰好使混合物完全溶解,放出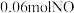 ,往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的原混合物,能得到铁的物质的量为
,往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的原混合物,能得到铁的物质的量为
 的混合物中加入
的混合物中加入 的稀硝酸,恰好使混合物完全溶解,放出
的稀硝酸,恰好使混合物完全溶解,放出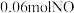 ,往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的原混合物,能得到铁的物质的量为
,往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的原混合物,能得到铁的物质的量为A.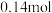 | B. | C.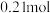 | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】从电子废料(含 、
、 和
和 等)中可回收金,主要流程如下:
等)中可回收金,主要流程如下: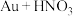 (稀)
(稀)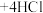 (浓)
(浓)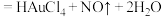
下列说法不正确 的是
 、
、 和
和 等)中可回收金,主要流程如下:
等)中可回收金,主要流程如下:
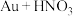 (稀)
(稀)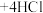 (浓)
(浓)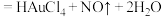
下列说法
A.浓盐酸促进了 和 和 的反应,其原因是降低了 的反应,其原因是降低了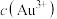 ,增强了 ,增强了 的还原性 的还原性 |
B.以 为电解质进行粗金的电解精炼,可能会有 为电解质进行粗金的电解精炼,可能会有 覆盖在阴极发生针化 覆盖在阴极发生针化 |
C. 可实现析金发生反应: 可实现析金发生反应: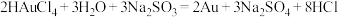 |
D.依据王水溶金原理, 溶液与浓盐酸也可使 溶液与浓盐酸也可使 溶解 溶解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列指定反应的离子方程式正确的是
A.用惰性电极电解CuCl2溶液: 2H2O + Cu2++ 2Cl- Cu(OH)2+ H2↑+ Cl2↑ Cu(OH)2+ H2↑+ Cl2↑ |
B.将少量氯气通入NaHSO3溶液中:HSO + H2O +Cl2=2Cl-+ 3H++SO + H2O +Cl2=2Cl-+ 3H++SO |
C.0.1mol/L AgNO3溶液中加入过量浓氨水:Ag+ + 2NH3·H2O =Ag(NH3)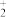 + 2H2O + 2H2O |
D.将NaHSO3溶液滴入Ba(NO3)2溶液产生白色沉淀:2HSO + Ba2+ =H2O+SO2↑+BaSO3↓ + Ba2+ =H2O+SO2↑+BaSO3↓ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 时,苯酚(C6H5OH)的Ka=1.0×10-10,下列说法正确的是
时,苯酚(C6H5OH)的Ka=1.0×10-10,下列说法正确的是
 时,苯酚(C6H5OH)的Ka=1.0×10-10,下列说法正确的是
时,苯酚(C6H5OH)的Ka=1.0×10-10,下列说法正确的是A.相同温度下,等 的 的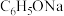 和 和 溶液中, 溶液中,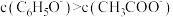 |
B.向C6H5ONa溶液中通入少量CO2,C6H5ONa+CO2+H2O=C6H5OH+CO |
C. 时, 时, 溶液与 溶液与 溶液混合,测得 溶液混合,测得 ,则此时溶液中c(C6H5O-)=c(C6H5OH) ,则此时溶液中c(C6H5O-)=c(C6H5OH) |
D. 时, 时, 的 的 溶液中加少量 溶液中加少量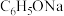 固体,水的电离程度变小 固体,水的电离程度变小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列各组离子在指定溶液中能大量共存的是( )
| A.无色溶液:K+、Na+、Cu2+、OH- |
| B.由水电离出的c(OH-)=10-13mol/L的溶液中:Na+、Ba2+、Cl-、Br- |
C.加入Al能放出H2的溶液中:Cl-、 、 、 、 、 |
D.有较多Fe3+的溶液中:Na+、 、SCN-、 、SCN-、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】不同浓度的CH3COONa溶液和NaHCO3溶液pH-c如图,下列说法错误的是


| A.CH3COONa溶液的pH-c线性关系明显,浓度每增加10倍,pH增加约0.5个单位 |
| B.近似浓度小于0.01mol/L,CH3COONa 溶液的pH小于NaHCO3溶液pH,说明CH3COOH酸性大于H2CO3 |
| C.NaHCO3溶液pH不仅要考虑水解,还要考虑电离 |
| D.同温、同浓度下CH3COONa溶液和NaHCO3溶液pH大小具体视浓度而定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】将硫酸铜的稀溶液放在密闭容器中,缓缓抽取容器中的水蒸气,溶液逐渐失水变成饱和溶液,再继续抽气,则变成各种含水盐,最后变成无水硫酸铜。50°C时,容器中的压强与结晶体水合物和溶液中含水量的关系如图所示。下列说法正确的是
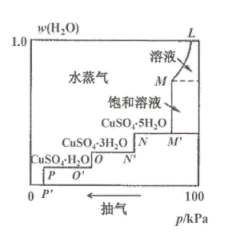
| A.曲线L-M对应溶液中溶质的质量分数不变 |
| B.曲线M -Mˊ对应溶液中无硫酸铜晶体析出 |
| C.曲线Mˊ-N对应体系存在平衡:CuSO4 (饱和溶液)⇌CuSO4·5H2O(s)+ H2O(g) |
| D.当容器中压强低于Pˊ后得到无水硫酸铜 |
您最近一年使用:0次

 、
、 、
、
 、
、 、
、
 、
、 、
、 、
、 的溶液中:
的溶液中: 、
、 、
、 、
、