合成氨对人类生存具有重大意义:
(1)传统工业合成法:反应为N2(g)+3H2(g) 2NH3(g) ∆H。科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)。
2NH3(g) ∆H。科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)。
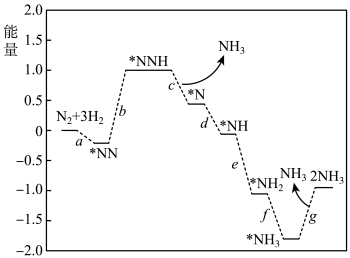
①N2的电子式是___ 。
②写出步骤b的化学方程式___ 。
③由图象可知合成氨反应的∆H__ 0(填“>”、“<”或“=”)。
④工业生产中,除了温度采用400℃—500℃外,促进该反应正向进行的措施是(至少两点)___ 。
(2)电化学制备方法:目前科学家利用生物燃料电池原理(电池工作时MV2+/MV+在电极与酶之间传递电子),研究室温下合成氨并取得初步成果,示意图如图:

①氢化酶区域发生反应的离子方程式是___ 。
②溶液中H+的移动方向是___ (填“向左”或“向右”)。
③下列说法正确的是___ 。
A.该装置可以实现电能转化为化学能
B.电极a是燃料电池的负极
C.该方法相较于传统工业合成方法具有条件温和,对环境友好等优点
(1)传统工业合成法:反应为N2(g)+3H2(g)
 2NH3(g) ∆H。科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)。
2NH3(g) ∆H。科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)。
①N2的电子式是
②写出步骤b的化学方程式
③由图象可知合成氨反应的∆H
④工业生产中,除了温度采用400℃—500℃外,促进该反应正向进行的措施是(至少两点)
(2)电化学制备方法:目前科学家利用生物燃料电池原理(电池工作时MV2+/MV+在电极与酶之间传递电子),研究室温下合成氨并取得初步成果,示意图如图:

①氢化酶区域发生反应的离子方程式是
②溶液中H+的移动方向是
③下列说法正确的是
A.该装置可以实现电能转化为化学能
B.电极a是燃料电池的负极
C.该方法相较于传统工业合成方法具有条件温和,对环境友好等优点
2021·北京延庆·一模 查看更多[1]
更新时间:2021-08-17 18:05:00
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】如图是A→E五种含氮物质相互转化的关系图。其中A、B、C、D常温下都是气体,且B为红棕色气体。
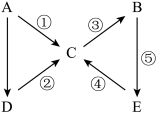
(1)写出下列物质的化学式:
A___ 、B___ 、C___ 、D____ 、E___ 。
(2)写出下面各步反应的化学方程式:
①___ 、②___ 、⑤___ 。

(1)写出下列物质的化学式:
A
(2)写出下面各步反应的化学方程式:
①
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】现有下列4种物质:① NH3、② Na2SiO3、③ Al、④ NaHCO3。其中,能与稀盐酸反应得到胶体的是______ (填序号,下同);与NaOH溶液和稀硫酸均反应生成氢气的是______ ;可以受热分解生成CO2的是______ ;能使湿润的红色石蕊试纸变蓝的气体是______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】化合价和物质分类是认识物质的性质、实现物质之间转化的两个视角。回答下列问题。
(1)现有下列物质:
A.NaOH B.SO3 C.CuSO4 D.Cl2 E.Fe2O3 F.NH3
①上述物质中属于酸性氧化物的是___________ (填字母)。NaOH属于___________ 化合物(填“离子”或“共价”)。
②氮氧化物是大气污染物,若要将NO转化为N2,从性质考虑,以上物质A~F中可以选择与NO反应的是___________ (填字母)。
(2)下图是部分含氯物质的“价-类”二维图。

①e物质的电子式为___________ 。
②过程i、ii、iii的转化中属于氧化还原反应的有过程___________ (填编号)。
③表示b转化为f的离子方程式可以为___________ 。
(1)现有下列物质:
A.NaOH B.SO3 C.CuSO4 D.Cl2 E.Fe2O3 F.NH3
①上述物质中属于酸性氧化物的是
②氮氧化物是大气污染物,若要将NO转化为N2,从性质考虑,以上物质A~F中可以选择与NO反应的是
(2)下图是部分含氯物质的“价-类”二维图。

①e物质的电子式为
②过程i、ii、iii的转化中属于氧化还原反应的有过程
③表示b转化为f的离子方程式可以为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】目前市场上的电池种类繁多,性能也各不相同。
(1)科学家发明了一种以熔融碳酸盐为离子导体的新型燃料电池,工作原理如下图1所示。电池工作时,外电路上电子移动的方向应从电极_______ (填A或B)流向用电器。内电路中阳离子向电极_______ (填A或B)移动,试写出B电极的电极反应式_______ 。

(2)某种燃料电池的工作原理示意如上图2所示(a、b均为石墨电极)。

①假设使用的“燃料”是氢气 ,则b极的电极反应式为
,则b极的电极反应式为_______ 。
②假设使用的“燃料”是甲烷 ,则通入甲烷气体的电极是电池的
,则通入甲烷气体的电极是电池的_______ (填“正”或“负”)极,电池工作一段时间后,电解液的碱性将_______ (填“增强”、“减弱”或“不变”)
③若消耗标准状况下的甲烷 ,假设化学能完全转化为电能,则转移电子的数目为
,假设化学能完全转化为电能,则转移电子的数目为_______ (用 表示)。
表示)。
(1)科学家发明了一种以熔融碳酸盐为离子导体的新型燃料电池,工作原理如下图1所示。电池工作时,外电路上电子移动的方向应从电极

(2)某种燃料电池的工作原理示意如上图2所示(a、b均为石墨电极)。

①假设使用的“燃料”是氢气
 ,则b极的电极反应式为
,则b极的电极反应式为②假设使用的“燃料”是甲烷
 ,则通入甲烷气体的电极是电池的
,则通入甲烷气体的电极是电池的③若消耗标准状况下的甲烷
 ,假设化学能完全转化为电能,则转移电子的数目为
,假设化学能完全转化为电能,则转移电子的数目为 表示)。
表示)。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)写出制取硝基苯的化学反应方程式_________________________________ ;
(2)写出镁铝氢氧化钠原电池的负极电极反应式___________________________ ;
(3)氯气是重要的化工原料,可以用来制备很多化工产品,比如可以制备净水剂高铁酸钾(K2FeO4),写出碱性条件下,由氯化铁制备高铁酸钾的离子方程式___________ ;
写出工业制漂白粉的化学反应方程式__________________________ 。
(2)写出镁铝氢氧化钠原电池的负极电极反应式
(3)氯气是重要的化工原料,可以用来制备很多化工产品,比如可以制备净水剂高铁酸钾(K2FeO4),写出碱性条件下,由氯化铁制备高铁酸钾的离子方程式
写出工业制漂白粉的化学反应方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题
(1)下列物质中可以作为燃料电池的负极反应物的是_______
(2)最新研制的一种新型乙醇电池示意图如图,电池的两极分别充入乙醇和氧气,用磺酸类离子作溶剂。

则电池工作时_______ (选填“a”或“b”)为负极,b 极的电极反应式为_______ 。
(3)欲在某镀件上镀银,在大烧杯中加入电镀液(含AgNO3的溶液)。银片和待镀镀件分别做两极,其中待镀的镀件做_______ 极,接通直流电源后几分钟,就看到镀件的表面镀上了一层银。银电极发生_______ 反应,镀件上发生的电极反应式是:_______ 。
(1)下列物质中可以作为燃料电池的负极反应物的是_______
| A.CH4 | B.H2 | C.CH3OH | D.O2 |

则电池工作时
(3)欲在某镀件上镀银,在大烧杯中加入电镀液(含AgNO3的溶液)。银片和待镀镀件分别做两极,其中待镀的镀件做
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
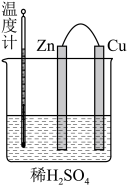
【推荐2】化学电源在生产、生活中有着广泛的应用。回答下列问题:
(1)图中,正极电极反应式:______ ;电子流向:______ (填“ ”或“Cu”,下同)极经导线流入
”或“Cu”,下同)极经导线流入______ 极。
(2)铅蓄电池是常见的二次电池,其工作原理如图所示。放电时总反应为 ,负极电极反应式为
,负极电极反应式为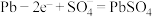 。
。
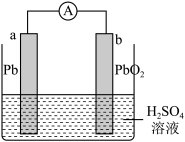
①写出放电时正极的电极反应式:______ ;
②铅蓄电池放电时一段时间,当转移 电子时,负极质量将增大
电子时,负极质量将增大______ g。
(3)金属(M)-空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为 。
。
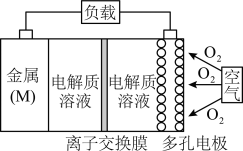
已知:①电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。
②阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。
比䢂Mg、Al、Zn三种金属-空气电池,则Mg、Al、Zn分别作为电极时“理论比能量”由大到小的顺序为______ ,该电池正极的电极反应式为______ ,若为 -空气电池,为防止负极区沉积
-空气电池,为防止负极区沉积 ,宜采用
,宜采用______ (填“阳离子”或“阴离子”)交换膜。
(1)图中,正极电极反应式:
 ”或“Cu”,下同)极经导线流入
”或“Cu”,下同)极经导线流入
(2)铅蓄电池是常见的二次电池,其工作原理如图所示。放电时总反应为
 ,负极电极反应式为
,负极电极反应式为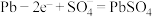 。
。
①写出放电时正极的电极反应式:
②铅蓄电池放电时一段时间,当转移
 电子时,负极质量将增大
电子时,负极质量将增大(3)金属(M)-空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为
 。
。
已知:①电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。
②阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。
比䢂Mg、Al、Zn三种金属-空气电池,则Mg、Al、Zn分别作为电极时“理论比能量”由大到小的顺序为
 -空气电池,为防止负极区沉积
-空气电池,为防止负极区沉积 ,宜采用
,宜采用
您最近一年使用:0次

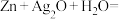
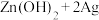 。
。


