(1)写出制取硝基苯的化学反应方程式_________________________________ ;
(2)写出镁铝氢氧化钠原电池的负极电极反应式___________________________ ;
(3)氯气是重要的化工原料,可以用来制备很多化工产品,比如可以制备净水剂高铁酸钾(K2FeO4),写出碱性条件下,由氯化铁制备高铁酸钾的离子方程式___________ ;
写出工业制漂白粉的化学反应方程式__________________________ 。
(2)写出镁铝氢氧化钠原电池的负极电极反应式
(3)氯气是重要的化工原料,可以用来制备很多化工产品,比如可以制备净水剂高铁酸钾(K2FeO4),写出碱性条件下,由氯化铁制备高铁酸钾的离子方程式
写出工业制漂白粉的化学反应方程式
更新时间:2017-06-29 19:29:32
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】钠和氯是海洋中重要的两种元素,其化合物有很多用途。
(1)将水滴入盛有过氧化钠固体的试管中,立即把带火星的木条伸入试管中,发现__ ,用pH试纸检验溶液为碱性,写出过氧化钠固体与水反应的离子方程式__ 。
(2)氯气广泛应用于化工生产中,将氯气通入冷的石灰乳中制得漂白粉,请写出化学方程式___ 。
(1)将水滴入盛有过氧化钠固体的试管中,立即把带火星的木条伸入试管中,发现
(2)氯气广泛应用于化工生产中,将氯气通入冷的石灰乳中制得漂白粉,请写出化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某同学用如下所示装置探究物质的性质。其中气体A的主要成分是氯气,还含有少量水蒸气。请回答下列问题:

(1)该实验观察到的实验现象是___________________________________ 。
(2)浓硫酸的作用是_____________________________________________ 。
(3)该实验设计还存在事故隐患,因此还需增加_________________ 装置。

(1)该实验观察到的实验现象是
(2)浓硫酸的作用是
(3)该实验设计还存在事故隐患,因此还需增加
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为_______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】按要求回答问题:
(1)漂粉精的主要成分:_____ (填化学式);苏打的化学式:_____ 。
(2)氢化钠中氢的化合价_____ ; 的电离方程式
的电离方程式_____ 。
(3)常温下,将氯气通入氢氧化钠溶液中发生反应的离子方程式为_____ 。
(4)过氧化钠与二氧化碳反应的化学方程式为_____ 。
(5)瓦斯中甲烷与氧气的质量比为1:4时极易发生爆炸,此时甲烷和氧气的体积比为_____ 。
(1)漂粉精的主要成分:
(2)氢化钠中氢的化合价
 的电离方程式
的电离方程式(3)常温下,将氯气通入氢氧化钠溶液中发生反应的离子方程式为
(4)过氧化钠与二氧化碳反应的化学方程式为
(5)瓦斯中甲烷与氧气的质量比为1:4时极易发生爆炸,此时甲烷和氧气的体积比为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】按要求填写下列空格
(1)画出Cl的原子结构示意图__________ 。
(2)写出醋酸的电离方程式__________________ 。
(3)写出工业上制取漂白粉的化学方程式__________________ 。
(1)画出Cl的原子结构示意图
(2)写出醋酸的电离方程式
(3)写出工业上制取漂白粉的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】氯气的化学性质
(1)氯气是很活泼的非金属单质,具有强___________ 性。
(2)与金属单质的反应
2Na+Cl2 2NaCl,产生
2NaCl,产生___________ 。
2Fe+3Cl2
___________ ,产生___________ ,加水溶解所得溶液呈___________ 色(Fe3+的颜色)。
Cu+Cl2 CuCl2,产生
CuCl2,产生___________ ,加水溶解所得溶液呈___________ 。
(3)与非金属单质的反应
[实验探究]H2在Cl2中燃烧
(4)与水的反应
①Cl2溶于水,Cl2的水溶液称为。在常温下,溶于水的氯气部分与水反应生成了盐酸和次氯酸,反应的化学方程式为___________ ,离子方程式为___________ 。
从化合价的角度看,该反应中氯元素的化合价既有升高又有降低,故Cl2既是氧化剂又是还原剂。
②氯水的性质
[注意]干燥的氯气不具有漂白性,潮湿的氯气才具有漂白性,实际上起作用的是Cl2与水反应生成的HClO。
③次氯酸的性质
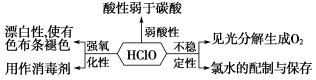
(5)与碱的反应
①化学方程式:Cl2+2NaOH=_________+H2O,_________ ,离子方程式:_________
漂白液的有效成分是_________ 。
②制取漂白粉
2Cl2+2Ca(OH)2=_________+2H2O_________
漂白粉的有效成分是_________ ,其主要成分是CaCl2和Ca(ClO)2。
Cl2与Ca(OH)2反应充分,并使_________ 成为主要成分,则得到漂粉精。
[注意]氯气所发生的反应均为氧化还原反应,反应中氯气通常为氧化剂,但Cl2与碱反应时,Cl2既是氧化剂又是还原剂。
(1)氯气是很活泼的非金属单质,具有强
(2)与金属单质的反应
2Na+Cl2
 2NaCl,产生
2NaCl,产生2Fe+3Cl2

Cu+Cl2
 CuCl2,产生
CuCl2,产生(3)与非金属单质的反应
[实验探究]H2在Cl2中燃烧
| 实验操作 | 实验现象 | 实验结论 |
| 在空气中点燃H2后,把导管缓慢伸入盛满氯气的集气瓶中 | 氢气在氯气中安静地燃烧,发出 | H2+Cl2 2HCl,反应生成的HCl极易溶于水,溶于水得到的溶液即为 2HCl,反应生成的HCl极易溶于水,溶于水得到的溶液即为 |
①Cl2溶于水,Cl2的水溶液称为。在常温下,溶于水的氯气部分与水反应生成了盐酸和次氯酸,反应的化学方程式为
从化合价的角度看,该反应中氯元素的化合价既有升高又有降低,故Cl2既是氧化剂又是还原剂。
②氯水的性质
| 实验操作 | 实验现象 | 结论 |
 | 有色布条 | 干燥的Cl2 |
 | 有色布条 | 氯水有漂白作用,起漂白作用的是HClO |
③次氯酸的性质

(5)与碱的反应
①化学方程式:Cl2+2NaOH=_________+H2O,
漂白液的有效成分是
②制取漂白粉
2Cl2+2Ca(OH)2=_________+2H2O
漂白粉的有效成分是
Cl2与Ca(OH)2反应充分,并使
[注意]氯气所发生的反应均为氧化还原反应,反应中氯气通常为氧化剂,但Cl2与碱反应时,Cl2既是氧化剂又是还原剂。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】从某铝镁合金片上剪下一小块(质量为1.0g),立即投入到盛有10mL10mol/LNaOH溶液的小烧杯中。
(1)自反应开始到反应结束,从小烧杯中可观察到的主要现象。(请依次写出)
(2)开始时产生气泡的速率较慢的原因是________________________________ 。后来的反应速率相当快的原因是___________________________________ 。
(3)写出所形成的原电池的负极材料名称:________________________________
电极反应式:____________________________________
(4)欲利用该反应来测定合金中铝的含量,还应测定的数据:_______________________ (请逐一写出)
(1)自反应开始到反应结束,从小烧杯中可观察到的主要现象。(请依次写出)
(2)开始时产生气泡的速率较慢的原因是
(3)写出所形成的原电池的负极材料名称:
电极反应式:
(4)欲利用该反应来测定合金中铝的含量,还应测定的数据:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】利用反应Cu+2FeCl3=CuCl2+2FeCl2设计成如图所示原电池,回答下列问题:

(1)写出电极反应式:正极___________________ ;负极_________________ 。
(2)图中X溶液是____________ ,Y溶液是____________ 。
(3)原电池工作时,盐桥中的________ (填“阳”或“阴”)离子向X溶液方向移动。
(4)X溶液中石墨电极上发生____________ (填“氧化”或“还原”)反应

(1)写出电极反应式:正极
(2)图中X溶液是
(3)原电池工作时,盐桥中的
(4)X溶液中石墨电极上发生
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】燃料电池是利用燃料与氧气反应从而将化学能转化为电能的装置。

以葡萄糖为燃料的微生物燃料电池结构示意图如上图所示。
(1)A为生物燃料电池的_______ (填“正”或“负”)极,正极反应式为_______ 。
(2)放电过程中,H+由_______ 极区向_______ 极区迁移(填“正”或“负”)。
(3)在电池反应中,每消耗1mol氧气,理论上生成标准状况下二氧化碳的体积是_______ 。
(4)电子由电极_______ 通过用电器流向电极_______ (填“A”或“B”)。

以葡萄糖为燃料的微生物燃料电池结构示意图如上图所示。
(1)A为生物燃料电池的
(2)放电过程中,H+由
(3)在电池反应中,每消耗1mol氧气,理论上生成标准状况下二氧化碳的体积是
(4)电子由电极
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】完成原电池问题。
Ⅰ.有甲、乙两位同学均想利用原电池反应检测金属的活动性,两人均使用相同镁片与铝片作电极,甲同学将电极放入2 mol/L H2SO4 溶液中,乙同学将电极放入2 mol/L的NaOH溶液中,如图所示。

请回答:
(1)写出甲池中正极的电极反应式:_________________________________ 。
(2)写出乙池中负极的电极反应式和总反应的离子方程式:
负极:_________________________________________________ ;
总反应:_______________________________________________ 。
(3)如果甲、乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出_______ 活动性更强,而乙会判断出________ 活动性更强(填写元素符号)。
(4)由此实验,可得到如下哪些正确结论?_________ (填写字母序号)。
a.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
b.镁的金属性不一定比铝的金属性强
c.该实验说明金属活动性顺序已过时,已没有实用价值
d.上述实验反过来证明了“直接利用金属活动性顺序判断原电池中的正负极”的做法是“不可靠”的
Ⅱ.市场上出售的“热敷袋”其主要成分是铁屑、炭粉、木屑和少量氯化钠、水等。“热敷袋”启用之前用塑料袋使其与空气隔绝,启用时,打开塑料袋轻轻揉搓就会放出热量。使用完后,会发现有大量铁锈存在。“热敷袋”放出的热量是利用了_____________________________________ 而放出热量。
Ⅰ.有甲、乙两位同学均想利用原电池反应检测金属的活动性,两人均使用相同镁片与铝片作电极,甲同学将电极放入2 mol/L H2SO4 溶液中,乙同学将电极放入2 mol/L的NaOH溶液中,如图所示。

请回答:
(1)写出甲池中正极的电极反应式:
(2)写出乙池中负极的电极反应式和总反应的离子方程式:
负极:
总反应:
(3)如果甲、乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出
(4)由此实验,可得到如下哪些正确结论?
a.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
b.镁的金属性不一定比铝的金属性强
c.该实验说明金属活动性顺序已过时,已没有实用价值
d.上述实验反过来证明了“直接利用金属活动性顺序判断原电池中的正负极”的做法是“不可靠”的
Ⅱ.市场上出售的“热敷袋”其主要成分是铁屑、炭粉、木屑和少量氯化钠、水等。“热敷袋”启用之前用塑料袋使其与空气隔绝,启用时,打开塑料袋轻轻揉搓就会放出热量。使用完后,会发现有大量铁锈存在。“热敷袋”放出的热量是利用了
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】人们应用原电池原理制作了多种电池,以满足不同的需要。请根据题中提供的信息,填写空格。
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为:___ 。当线路中转移0.4mol电子时,则被腐蚀铜的质量为:____ g。(已知:铜的相对原子量是64)
(2)将铝片和铜片用导线相连,一组插入溶液氢氧化钠中,一组插入浓硝酸中,分别形成了原电池,在这两个原电池中,负极分别为____ 。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(3)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

该酸式氢氧燃料电池的负极电极反应式是____ ,正极电极反应式是____ ,电池工作一段时间后电解质溶液pH___ (填“增大”“减小”或“不变”)。
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为:
(2)将铝片和铜片用导线相连,一组插入溶液氢氧化钠中,一组插入浓硝酸中,分别形成了原电池,在这两个原电池中,负极分别为
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(3)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

该酸式氢氧燃料电池的负极电极反应式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】某兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下系列实验,实验结果记录如下:
注:①实验均为常温下完成;②电流计指针偏转方向为正极方向。试根据表中实验现象完成下列问题:
(1)实验1、2中Al所作的电极(指正极或负极)______ (填“相同”或“不同”)。
(2)对实验3完成下列填空:
①Al为______ 极,电极反应式为______ 。
②石墨为______ 极,电极反应式为______ 。
③电池总反应式为______
(3)实验4中Al作______ 极,理由是______ 。
(4)解释实验5中电流计偏向Al的原因______ 。
(5)根据实验结果总结出影响铝在电池中作正极或负极的因素有______ 。
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | NaOH溶液 | 偏向Mg |
| 5 | Al、Cu | 浓硝酸 | 偏向Al |
注:①实验均为常温下完成;②电流计指针偏转方向为正极方向。试根据表中实验现象完成下列问题:
(1)实验1、2中Al所作的电极(指正极或负极)
(2)对实验3完成下列填空:
①Al为
②石墨为
③电池总反应式为
(3)实验4中Al作
(4)解释实验5中电流计偏向Al的原因
(5)根据实验结果总结出影响铝在电池中作正极或负极的因素有
您最近一年使用:0次



