二硫化钨(WS2,WS2中W的化合价为+4)可用作润滑剂及石油化工领域中的催化剂。由钨铁矿(其主要成分是FeWO4,还含少量Al2O3)制备二硫化钨的工艺流程如下:
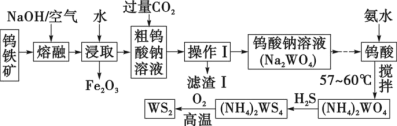
(1)写出FeWO4在碱熔过程中发生反应的化学方程式:___________ 。
(2)滤渣Ⅰ中主要成分的形成可用离子方程式表示为___________ 。

(1)写出FeWO4在碱熔过程中发生反应的化学方程式:
(2)滤渣Ⅰ中主要成分的形成可用离子方程式表示为
2021高三·全国·专题练习 查看更多[1]
(已下线)专题讲座(二)陌生化学方程式书写(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)
更新时间:2021-08-20 09:13:37
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】三氧化二砷(As2O3)可用于治疗急性早幼粒白血病。利用某酸性含砷废水(含 、H+、
、H+、 )可提取三氧化二砷,提取工艺流程如图所示:
)可提取三氧化二砷,提取工艺流程如图所示:

已知:①As2O3+6NaOH=2Na3AsO3+3H2O;
②As2S3易溶于过量的Na2S溶液中,加入FeSO4的目的是除去过量的S2-。
请回答下列问题:
(1)基态As原子的价层电子排布式为___________ 。
(2)操作M的名称是___________ ,滤液N中含有的阳离子有Fe2+、H+、___________ 。
(3)“焙烧”操作中,As2S3参与反应的化学方程式为___________ 。
(4)“碱浸”的目的是___________ 。
(5)“氧化”中发生反应的离子方程式为___________ 。
(6)砷化镓(GaAs)可由(CH3)3Ga和AsH3在700°C制得。已知GaAs的熔点为1238°C,其晶胞结构如图所示,该晶体的类型为___________ 。若阿伏加德罗常数的值为NA,GaAs的密度为ρg·cm-3,摩尔质量为Mg·mol-1,则GaAs的晶胞边长为___________ pm。

 、H+、
、H+、 )可提取三氧化二砷,提取工艺流程如图所示:
)可提取三氧化二砷,提取工艺流程如图所示:
已知:①As2O3+6NaOH=2Na3AsO3+3H2O;
②As2S3易溶于过量的Na2S溶液中,加入FeSO4的目的是除去过量的S2-。
请回答下列问题:
(1)基态As原子的价层电子排布式为
(2)操作M的名称是
(3)“焙烧”操作中,As2S3参与反应的化学方程式为
(4)“碱浸”的目的是
(5)“氧化”中发生反应的离子方程式为
(6)砷化镓(GaAs)可由(CH3)3Ga和AsH3在700°C制得。已知GaAs的熔点为1238°C,其晶胞结构如图所示,该晶体的类型为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、CaCl2、NaCl中的几种物质组成。某同学为了鉴别它们,做了如下实验:
①将固体混合物溶于水,搅拌后得到无色透明溶液;
②在①所得的溶液中滴加Ba(NO3)2溶液,有白色沉淀生成,并继续滴加至沉淀完全;
③过滤,然后向所得白色沉淀中加入过量稀硝酸,沉淀部分溶解。
根据该同学的实验结果回答下列问题:
(1)原混合物中肯定有___________ ,肯定没有___________ ,可能含有___________ 。
(2)写出上述实验过程中白色沉淀部分溶解发生反应的离子方程式:___________ 。
(3)要检验可能含有的物质可采用的方法是___________ 。
①将固体混合物溶于水,搅拌后得到无色透明溶液;
②在①所得的溶液中滴加Ba(NO3)2溶液,有白色沉淀生成,并继续滴加至沉淀完全;
③过滤,然后向所得白色沉淀中加入过量稀硝酸,沉淀部分溶解。
根据该同学的实验结果回答下列问题:
(1)原混合物中肯定有
(2)写出上述实验过程中白色沉淀部分溶解发生反应的离子方程式:
(3)要检验可能含有的物质可采用的方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】金属镓被称为“电子工业脊梁”,氮化镓应用于5G技术中。利用粉煤灰(主要成分为 、
、 、
、 ,还有少量
,还有少量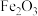 等杂质)制备氮化镓流程如下:
等杂质)制备氮化镓流程如下:
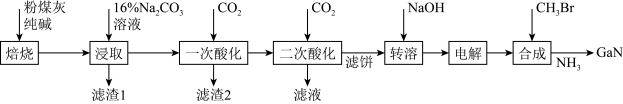
已知:①镓性质与铝相似,金属活动性介于锌和铁之间;②常温下,相关元素可溶性组分物质的量浓度c与 的关系如图1所示。当溶液中可溶组分浓度c≤10-5mol/L时,可认为已除尽。
的关系如图1所示。当溶液中可溶组分浓度c≤10-5mol/L时,可认为已除尽。
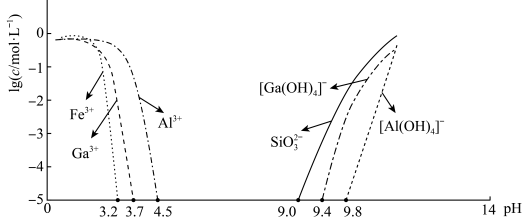
回答下列问题:
(1)“焙烧”的目的是将 转化为
转化为 ,该过程还产生
,该过程还产生_______ 。(填物质名称)
(2)“滤渣1”主要成分为_______ 。
(3)“二次酸化”中 与少量
与少量 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(4)“电解”可得金属 ,写出阴极电极反应式
,写出阴极电极反应式_______ 。
(5)常温下,反应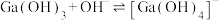 的平衡常数
的平衡常数 的值为
的值为_______ 。
(6)取a克 样品溶于足量的热
样品溶于足量的热 溶液中,用
溶液中,用 溶液将产生的
溶液将产生的 完全吸收,用
完全吸收,用 的盐酸滳定,消耗盐酸
的盐酸滳定,消耗盐酸 ,则样品的纯度是
,则样品的纯度是_______ 。(已知: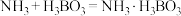 ;
;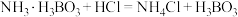 )
)
(7)若 晶胞(如图2)边长为
晶胞(如图2)边长为 ,则
,则 原子与
原子与 原子的最短核间距为
原子的最短核间距为_______  。
。
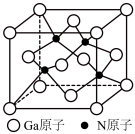
图 2
 、
、 、
、 ,还有少量
,还有少量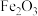 等杂质)制备氮化镓流程如下:
等杂质)制备氮化镓流程如下:
已知:①镓性质与铝相似,金属活动性介于锌和铁之间;②常温下,相关元素可溶性组分物质的量浓度c与
 的关系如图1所示。当溶液中可溶组分浓度c≤10-5mol/L时,可认为已除尽。
的关系如图1所示。当溶液中可溶组分浓度c≤10-5mol/L时,可认为已除尽。
回答下列问题:
(1)“焙烧”的目的是将
 转化为
转化为 ,该过程还产生
,该过程还产生(2)“滤渣1”主要成分为
(3)“二次酸化”中
 与少量
与少量 发生反应的离子方程式为
发生反应的离子方程式为(4)“电解”可得金属
 ,写出阴极电极反应式
,写出阴极电极反应式(5)常温下,反应
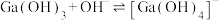 的平衡常数
的平衡常数 的值为
的值为(6)取a克
 样品溶于足量的热
样品溶于足量的热 溶液中,用
溶液中,用 溶液将产生的
溶液将产生的 完全吸收,用
完全吸收,用 的盐酸滳定,消耗盐酸
的盐酸滳定,消耗盐酸 ,则样品的纯度是
,则样品的纯度是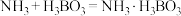 ;
;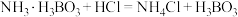 )
)(7)若
 晶胞(如图2)边长为
晶胞(如图2)边长为 ,则
,则 原子与
原子与 原子的最短核间距为
原子的最短核间距为 。
。
图 2
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】以高硫铝土矿(主要成分为 、
、 ,还含有少量
,还含有少量 )为原料,生产氧化铝并获得
)为原料,生产氧化铝并获得 的部分工艺流程如下,下列叙述不正确的是
的部分工艺流程如下,下列叙述不正确的是

(1)高硫铝土矿中 为
为___________ (填“酸性”、“碱性”或“两性”)氧化物。
(2)写出“碱浸”过程的离子方程式:___________
(3)焙烧过程中加入 的目的是:
的目的是:___________
(4)向滤液中通入过量___________ 、过滤、洗涤、___________ 可制得
(5)隔绝空气焙烧过程发生反应的化学方程式为:___________
(6)“烧渣分离”中可以选用___________
(7)用该方法分离出的 中可能含有少量
中可能含有少量 ,为了测定
,为了测定 的纯度,进行了如下实验:称取
的纯度,进行了如下实验:称取
 样品于装置中,高温灼烧,直至质量不再改变,称其质量为
样品于装置中,高温灼烧,直至质量不再改变,称其质量为
 ,则样品中
,则样品中 的纯度为:
的纯度为:___________ (已知 在高温下会转化为
在高温下会转化为 )
)
 、
、 ,还含有少量
,还含有少量 )为原料,生产氧化铝并获得
)为原料,生产氧化铝并获得 的部分工艺流程如下,下列叙述不正确的是
的部分工艺流程如下,下列叙述不正确的是
(1)高硫铝土矿中
 为
为(2)写出“碱浸”过程的离子方程式:
(3)焙烧过程中加入
 的目的是:
的目的是:(4)向滤液中通入过量

(5)隔绝空气焙烧过程发生反应的化学方程式为:
(6)“烧渣分离”中可以选用___________
| A.磁选法 | B.酸浸法 | C.碱浸法 | D.热还原法 |
 中可能含有少量
中可能含有少量 ,为了测定
,为了测定 的纯度,进行了如下实验:称取
的纯度,进行了如下实验:称取
 样品于装置中,高温灼烧,直至质量不再改变,称其质量为
样品于装置中,高温灼烧,直至质量不再改变,称其质量为
 ,则样品中
,则样品中 的纯度为:
的纯度为: 在高温下会转化为
在高温下会转化为 )
)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】MgO、Al2O3都是常用的耐火材料,某研究小组取100 kg含60%Al的报废汽车的镁铝合金材料来制备MgO、Al2O3,其工艺流程如图所示。

请回答下列问题:
(1)下列对合金材料的说法正确的是________ (填字母)。
A.利用生铁制造运—20飞机发动机
B.用镁铝合金制造运—20飞机座椅
C.用不锈钢制造运—20飞机电器线路的导线
D.用普通钢制造运—20飞机灭火器的外壳
(2)物质甲是________ ,产品A是________ 。
(3)操作①、②所需的玻璃仪器是_________________________________ 。
(4)足量物质乙与溶液A发生反应的离子方程式为__________________________________ 。
(5)某同学提出可由溶液B的溶质经过转化得到物质甲,写出相应的化学方程式_____________________________________________________________ 。

请回答下列问题:
(1)下列对合金材料的说法正确的是
A.利用生铁制造运—20飞机发动机
B.用镁铝合金制造运—20飞机座椅
C.用不锈钢制造运—20飞机电器线路的导线
D.用普通钢制造运—20飞机灭火器的外壳
(2)物质甲是
(3)操作①、②所需的玻璃仪器是
(4)足量物质乙与溶液A发生反应的离子方程式为
(5)某同学提出可由溶液B的溶质经过转化得到物质甲,写出相应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】从铝土矿(主要成分是 ,含
,含 、
、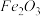 、MgO等杂质)中提取Al2O3的两种工艺品流程如下:
、MgO等杂质)中提取Al2O3的两种工艺品流程如下:

请回答下列问题:
(1)写出相应物质的的化学式:固体A__________ ,固体N__________ ,
滤液D中溶质为_____________ 。
(2)流程甲加入盐酸后生成Al3+的离子方程式为____________________________________________ 。
(3)流程乙加入烧碱后生成水玻璃溶液的化学方程式为______________________________________________________________________ 。
 ,含
,含 、
、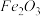 、MgO等杂质)中提取Al2O3的两种工艺品流程如下:
、MgO等杂质)中提取Al2O3的两种工艺品流程如下:
请回答下列问题:
(1)写出相应物质的的化学式:固体A
滤液D中溶质为
(2)流程甲加入盐酸后生成Al3+的离子方程式为
(3)流程乙加入烧碱后生成水玻璃溶液的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】高锰酸钾生产过程中产生的废锰渣(主要成分为 、
、 和
和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:
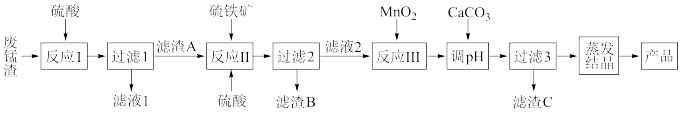
已知:①硫铁矿的主要成分为下 (杂质不参与反应);
(杂质不参与反应);
② 为肉色。
为肉色。
回答下列问题:
(1)为了提高“反应I”的速率,可采取的措施有___________ (写两种即可)。
(2)“反应II”的离子方程式为___________ ,“滤渣B”的主要成分为过量的 和
和___________ (填化学式)。
(3)“反应III”中氧化剂和还原剂物质的量之比为___________ 。
(4)检验“滤液1”中是否含有 的方法是
的方法是___________ 。
(5)取 固体样品,溶于适量水中,加硫酸酸化,用过量
固体样品,溶于适量水中,加硫酸酸化,用过量 (难溶于水)将其完全氧化为
(难溶于水)将其完全氧化为 ,过滤,洗涤液并入滤液后,加入
,过滤,洗涤液并入滤液后,加入 固体,充分反应后,用
固体,充分反应后,用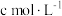 的
的 标准溶液滴定剩余的
标准溶液滴定剩余的 溶液,用去
溶液,用去 。
。
①达到滴定终点的现象是___________ 。
②样品中 的质量分数为
的质量分数为___________ (用含m、a、c、V的代数式表示)。
 、
、 和
和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:
已知:①硫铁矿的主要成分为下
 (杂质不参与反应);
(杂质不参与反应);②
 为肉色。
为肉色。回答下列问题:
(1)为了提高“反应I”的速率,可采取的措施有
(2)“反应II”的离子方程式为
 和
和(3)“反应III”中氧化剂和还原剂物质的量之比为
(4)检验“滤液1”中是否含有
 的方法是
的方法是(5)取
 固体样品,溶于适量水中,加硫酸酸化,用过量
固体样品,溶于适量水中,加硫酸酸化,用过量 (难溶于水)将其完全氧化为
(难溶于水)将其完全氧化为 ,过滤,洗涤液并入滤液后,加入
,过滤,洗涤液并入滤液后,加入 固体,充分反应后,用
固体,充分反应后,用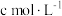 的
的 标准溶液滴定剩余的
标准溶液滴定剩余的 溶液,用去
溶液,用去 。
。①达到滴定终点的现象是
②样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】以冶炼铝的废弃物铝灰为原料制取超细α-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为 (含少量杂质
(含少量杂质 ),其制备实验流程如下:
),其制备实验流程如下:_________ 。
(2)“滤渣”与 溶液反应的化学方程式是
溶液反应的化学方程式是_________ 。
(3) 的结构式是
的结构式是_________ ,加 的作用是
的作用是_________ 。
(4)“沉铁”中加入的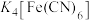 中铁元素的化合价是
中铁元素的化合价是_________ ,发生反应的离子方程式是_________ 。
(5)“操作”的具体步骤是_________ 、_________ 过滤、洗涤、干燥、煅烧。
 (含少量杂质
(含少量杂质 ),其制备实验流程如下:
),其制备实验流程如下:
(2)“滤渣”与
 溶液反应的化学方程式是
溶液反应的化学方程式是(3)
 的结构式是
的结构式是 的作用是
的作用是(4)“沉铁”中加入的
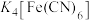 中铁元素的化合价是
中铁元素的化合价是(5)“操作”的具体步骤是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。
Ⅰ:黑木耳中含有比较丰富的铁元素,某研学小组测定其含量。
(1)【铁元素的分离】在坩埚中高温灼烧黑木耳,使之完全灰化。用足量的酸充分溶解,过滤,滤液中铁元素的存在形式是 、
、_______ 。
(2)【铁元素含量测定】研学小组提出如下测量方案。
ⅰ.沉淀法:向(1)滤液中加入足量 溶液,过滤、洗涤沉淀、充分加热至恒重、称量。请评价该测量方案是否可行
溶液,过滤、洗涤沉淀、充分加热至恒重、称量。请评价该测量方案是否可行_______ ,理由是_______ 。
ⅱ.比色法:流程如下。

①溶液 的颜色是
的颜色是_______ 。
②溶液颜色越深,光的透过能力越差,即透光率越小,含铁量越_______ (填“高”或“低”。)
③若不加 ,测出黑木耳中铁元素的含量将
,测出黑木耳中铁元素的含量将_______ (填“偏大”或“偏小”)。
Ⅱ:在肺部,血红蛋白中的亚铁血红素与 结合,把
结合,把 送到各个组织器官。
送到各个组织器官。
(3)已知葡萄糖的分子式是 。铁元素参与人体内的呼吸作用示意图如下图(部分中间产物已略去)。
。铁元素参与人体内的呼吸作用示意图如下图(部分中间产物已略去)。

①反应中起催化作用的物质是_______ 和 。
。
②具有还原性的酶是_______ 。
③该过程总反应的化学方程式是_______ 。
Ⅰ:黑木耳中含有比较丰富的铁元素,某研学小组测定其含量。
(1)【铁元素的分离】在坩埚中高温灼烧黑木耳,使之完全灰化。用足量的酸充分溶解,过滤,滤液中铁元素的存在形式是
 、
、(2)【铁元素含量测定】研学小组提出如下测量方案。
ⅰ.沉淀法:向(1)滤液中加入足量
 溶液,过滤、洗涤沉淀、充分加热至恒重、称量。请评价该测量方案是否可行
溶液,过滤、洗涤沉淀、充分加热至恒重、称量。请评价该测量方案是否可行ⅱ.比色法:流程如下。

①溶液
 的颜色是
的颜色是②溶液颜色越深,光的透过能力越差,即透光率越小,含铁量越
③若不加
 ,测出黑木耳中铁元素的含量将
,测出黑木耳中铁元素的含量将Ⅱ:在肺部,血红蛋白中的亚铁血红素与
 结合,把
结合,把 送到各个组织器官。
送到各个组织器官。(3)已知葡萄糖的分子式是
 。铁元素参与人体内的呼吸作用示意图如下图(部分中间产物已略去)。
。铁元素参与人体内的呼吸作用示意图如下图(部分中间产物已略去)。
①反应中起催化作用的物质是
 。
。②具有还原性的酶是
③该过程总反应的化学方程式是
您最近一年使用:0次



