下列关于硫及其化合物的叙述正确的是
| A.试管内壁残留的硫可用酒精洗涤 | B.SO2使溴水褪色体现SO2的漂白性 |
| C.SO2的水溶液长期放置,酸性会增强 | D.浓硫酸在空气中敞口放置,质量会减小 |
更新时间:2021-08-23 20:58:27
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】用NaOH溶液清洗试管壁上的硫,发生反应S + NaOH—Na2SO3 + Na2S + H2O(未配平),下列说法错误的是
| A.清洗之后的废液一定呈碱性 |
| B.也可以用CS2清洗试管壁上的硫 |
| C.生成的Na2SO3 和Na2S的物质的量之比为1 : 2 |
| D.氧化产物是Na2S |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】短周期元素X、Y、Z、W的原子序数依次增大。已知:X和Y均满足最高正化合价与最低负化合价代数和为零;Z的气态氢化物与最高价氧化物的水溶液能反应生成盐;实验室试管里残留有W单质,可以用Y和W形成的某种液态化合物清洗。下列说法正确的是
| A.ZX5是一种共价化合物,与水反应会发生氧化还原反应生成X2 |
| B.Z元素氢化物的熔沸点高于Y元素氢化物的熔沸点 |
| C.W的气态氢化物有剧毒,2003年12月23日重庆开县天然气井喷事故造成大量人员伤亡 |
| D.X、Z和氧三种元素组成的化合物对水的电离一定是抑制作用 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某消毒液的主要成分为NaClO,还含有一定量的NaOH。下列用来解释事实的方程式中,不合理的是(已知:饱和NaClO溶液的pH约为11)( )
| A.该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-=ClO-+Cl-+H2O |
| B.该消毒液中通入SO2气体可以增强漂白效果 |
| C.该消毒液与洁厕灵(主成分为HCl)混用,产生有毒Cl2:2H++Cl-+ClO-=Cl2↑+H2O |
| D.该消毒液加白醋生成HClO,可增强漂白作用CH3COOH+ClO-=HClO+CH3COO- |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向溴水中通入SO2气体 | 溶液褪色 | SO2具有漂白性 |
| B | 向淀粉水解液中加入NaOH溶液至碱性,再加入新制Cu(OH)2,煮沸 | 有砖红色沉淀生成 | 淀粉已水解 |
| C | 向某钠盐X的溶液中先滴加稀盐酸,无现象,再滴加BaCl2溶液 | 出现白色沉淀 | X一定是Na2SO4 |
| D | BaSO4固体加入饱和Na2CO3溶液中,过滤,向滤渣中加入盐酸 | 有气体生成 | Ksp(BaSO4)>Ksp(BaCO3) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】二氧化硫测量计工作的反应原理为:SO2+Br2+2H2O=H2SO4+2HBr,设NA为阿伏加德罗常数的值。下列有关说法正确的是
| A.2.24 LSO2参与反应破坏水中氢氧键数目为0.4 NA |
| B.反应生成0.1 mol H2SO4时,溶液中含有阳、阴离子数目为0.3 NA |
| C.在常温常压下16 g液态溴中原子数目为0.2 NA |
| D.反应生成0.2 mol H+,转移电子数目为0.2 NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】硫及其化合物在生产生活中具有广泛应用。由自然界的硫磺和金属硫化物矿通过化学反应可得到 ,
, 催化氧化生成
催化氧化生成 ,其热化学方程式为
,其热化学方程式为
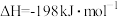 。燃煤、金属冶炼和硫酸生产等产生的尾气中都含有
。燃煤、金属冶炼和硫酸生产等产生的尾气中都含有 ,用
,用 等碱性溶液吸收尾气中的
等碱性溶液吸收尾气中的 ,可得到
,可得到 、
、 等化工产品。下列硫及其化合物的性质与用途具有对应关系的是
等化工产品。下列硫及其化合物的性质与用途具有对应关系的是
 ,
, 催化氧化生成
催化氧化生成 ,其热化学方程式为
,其热化学方程式为
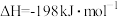 。燃煤、金属冶炼和硫酸生产等产生的尾气中都含有
。燃煤、金属冶炼和硫酸生产等产生的尾气中都含有 ,用
,用 等碱性溶液吸收尾气中的
等碱性溶液吸收尾气中的 ,可得到
,可得到 、
、 等化工产品。下列硫及其化合物的性质与用途具有对应关系的是
等化工产品。下列硫及其化合物的性质与用途具有对应关系的是A. 有氧化性,可用于生产 有氧化性,可用于生产 | B. 溶液显碱性,可用于吸收少量 溶液显碱性,可用于吸收少量 |
C. 有还原性,可用于纸浆漂白 有还原性,可用于纸浆漂白 | D.浓 有脱水性,可用作干燥剂 有脱水性,可用作干燥剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关试剂的保存与处理,说法正确的是( )
| A.氯气与铁不反应,因此液氯保存在钢瓶中 |
| B.金属钠保存在煤油中,金属钠着火可用二氧化碳灭火器灭火 |
| C.常温下,铁遇浓硫酸不反应,用钢瓶贮存与运输浓硫酸 |
| D.盛放浓硫酸与浓盐酸的试剂瓶敞口放置,浓度均会变低 |
您最近一年使用:0次



