盖斯定律的内容
大量实验证明,一个化学反应,不管是_____ 完成的还是____ 完成的,其反应热是_____ 的。换句话说,化学反应的反应热只与反应体系的_____ 和___ 有关,而与反应的____ 无关。
大量实验证明,一个化学反应,不管是
20-21高二·全国·课前预习 查看更多[2]
更新时间:2021-09-03 19:21:34
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】煤作为燃料,可以有下列两种途径(把煤看成由碳组成):
途径Ⅰ:C(s)+O2(g)= CO2(g) ΔH=-a kJ·mol-1
途径Ⅱ:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+b kJ·mol-1
2CO(g)+O2(g)=2CO2(g) ΔH=-c kJ·mol-1
2H2(g)+O2(g)=2H2O(g) ΔH=-d kJ·mol-1
试回答下列问题:
(1)燃烧等质量的煤,途径Ⅰ放出的热量____ 途径Ⅱ放出的热量(填“大于”、“小于”或“等于”)。
(2)b的数学关系式是______________ (用a、c、d表示)。
(3)由于制取水煤气反应中,反应物具有的总能量________ (填“大于”、“小于”或“等于”)生成物所具有的总能量,在反应时,反应物需要______ (填“吸收”或“放出”)能量才能转化为生成物。
(4)简述煤通过途径Ⅱ作为燃料的意义___________________________________ 。
途径Ⅰ:C(s)+O2(g)= CO2(g) ΔH=-a kJ·mol-1
途径Ⅱ:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+b kJ·mol-1
2CO(g)+O2(g)=2CO2(g) ΔH=-c kJ·mol-1
2H2(g)+O2(g)=2H2O(g) ΔH=-d kJ·mol-1
试回答下列问题:
(1)燃烧等质量的煤,途径Ⅰ放出的热量
(2)b的数学关系式是
(3)由于制取水煤气反应中,反应物具有的总能量
(4)简述煤通过途径Ⅱ作为燃料的意义
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】与研究物质变化一样,研究化学反应中的能量变化同样具有重要意义。
I. 的有效回收利用能缓解能源危机。
的有效回收利用能缓解能源危机。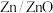 热化学循环还原
热化学循环还原 制
制 的原理如下图所示。
的原理如下图所示。
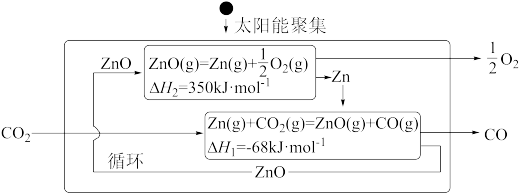
(1)从循环结果看,能量转化的主要方式是_______ 。
(2)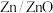 在反应中循环使用,其作用是
在反应中循环使用,其作用是_______ 。
II.已知二甲醚( ,常温下呈气态)、
,常温下呈气态)、 的燃烧热分别为1455
的燃烧热分别为1455 、286
、286 。
。
(3)请写出表示二甲醚燃烧热的热化学方程式_______ 。
(4)利用二甲醚可制取 ,总反应为
,总反应为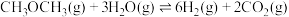 。已知
。已知
 ,则总反应的
,则总反应的
_______ 。总反应能自发进行的条件是_______ 。
(5)二甲醚制 的总反应分两步完成:
的总反应分两步完成:
二甲醚水解: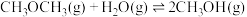 活化能
活化能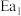
甲醇与水蒸气重整: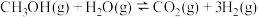 活化能
活化能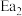
已知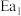 远小于
远小于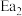 。在恒温恒容容器内,二甲醚与水按1∶3投料进行制氢,请在图中画出甲醇(
。在恒温恒容容器内,二甲醚与水按1∶3投料进行制氢,请在图中画出甲醇( )浓度随时间变化的曲线图
)浓度随时间变化的曲线图_______ 。

I.
 的有效回收利用能缓解能源危机。
的有效回收利用能缓解能源危机。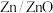 热化学循环还原
热化学循环还原 制
制 的原理如下图所示。
的原理如下图所示。
(1)从循环结果看,能量转化的主要方式是
(2)
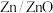 在反应中循环使用,其作用是
在反应中循环使用,其作用是II.已知二甲醚(
 ,常温下呈气态)、
,常温下呈气态)、 的燃烧热分别为1455
的燃烧热分别为1455 、286
、286 。
。(3)请写出表示二甲醚燃烧热的热化学方程式
(4)利用二甲醚可制取
 ,总反应为
,总反应为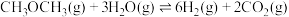 。已知
。已知
 ,则总反应的
,则总反应的
(5)二甲醚制
 的总反应分两步完成:
的总反应分两步完成:二甲醚水解:
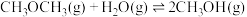 活化能
活化能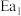
甲醇与水蒸气重整:
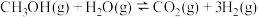 活化能
活化能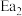
已知
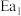 远小于
远小于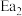 。在恒温恒容容器内,二甲醚与水按1∶3投料进行制氢,请在图中画出甲醇(
。在恒温恒容容器内,二甲醚与水按1∶3投料进行制氢,请在图中画出甲醇( )浓度随时间变化的曲线图
)浓度随时间变化的曲线图
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知下列热化学方程式:
① H2(g)+ O2(g)=H2O(l) ΔH =―285kJ/mol
O2(g)=H2O(l) ΔH =―285kJ/mol
② H2(g)+ O2(g)=H2O(g) ΔH =―241.8kJ/mol
O2(g)=H2O(g) ΔH =―241.8kJ/mol
③ C(s)+ O2(g)=CO(g) ΔH =―110.4 kJ/mol
O2(g)=CO(g) ΔH =―110.4 kJ/mol
④ C(s)+ O2(g)=CO2(g) ΔH =―393.5 kJ/mol
回答下列各问:
(1)上述反应中属于放热反应的是___________ 。
(2)C的燃烧热为_________________ 。
(3)燃烧10g H2生成液态水,放出的热量为_____________________ 。
(4)CO燃烧的热化学方程式为______________________ 。
(5)为了控制温室效应,各国科学家提出了不少设想。有人根据液态CO2密度大于海水密度的事实,设想将CO2液化后,送入深海海底,以减少大气中的CO2。为使CO2液化,可采取的措施________ 。
a 减压、升温 b 增压、降温
c 减压、降温 d 增压、升温
① H2(g)+
 O2(g)=H2O(l) ΔH =―285kJ/mol
O2(g)=H2O(l) ΔH =―285kJ/mol② H2(g)+
 O2(g)=H2O(g) ΔH =―241.8kJ/mol
O2(g)=H2O(g) ΔH =―241.8kJ/mol③ C(s)+
 O2(g)=CO(g) ΔH =―110.4 kJ/mol
O2(g)=CO(g) ΔH =―110.4 kJ/mol④ C(s)+ O2(g)=CO2(g) ΔH =―393.5 kJ/mol
回答下列各问:
(1)上述反应中属于放热反应的是
(2)C的燃烧热为
(3)燃烧10g H2生成液态水,放出的热量为
(4)CO燃烧的热化学方程式为
(5)为了控制温室效应,各国科学家提出了不少设想。有人根据液态CO2密度大于海水密度的事实,设想将CO2液化后,送入深海海底,以减少大气中的CO2。为使CO2液化,可采取的措施
a 减压、升温 b 增压、降温
c 减压、降温 d 增压、升温
您最近一年使用:0次



