已知在常温常压下:
①2CH3OH(l)+2O2(g)═2CO(g)+4H2O(g) △H=﹣akJ•mol﹣1
②2CO(g)+O2(g)═2CO2(g) △H=﹣bkJ•mol﹣1
③H2O(g)═H2O(l) △H=﹣ckJ•mol﹣1
则表示CH3OH(l)燃烧热的热化学方程式为_______ 。
①2CH3OH(l)+2O2(g)═2CO(g)+4H2O(g) △H=﹣akJ•mol﹣1
②2CO(g)+O2(g)═2CO2(g) △H=﹣bkJ•mol﹣1
③H2O(g)═H2O(l) △H=﹣ckJ•mol﹣1
则表示CH3OH(l)燃烧热的热化学方程式为
更新时间:2021-09-18 12:37:24
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】2007年诺贝尔化学奖授予德国科学家格哈德·埃特尔,以表彰他在表面化学研究领域作出的开拓性贡献。

(1)某校化学研究性学习小组的同学在技术人员的指导下,按下列流程探究不同催化剂对NH3还原NO反应的催化性能。
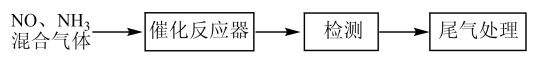
若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体通过滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。为比较不同催化剂的催化性能,需要测量并记录的数据是___ 。
(2)在汽车的排气管上安装“催化转化器”(用铂、钯合金作催化剂),它的作用是使CO、NO反应生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧。
①写出CO与NO反应的化学方程式:___ ,该反应作氧化剂的物质是__ 。
②用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);ΔH1=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);ΔH2
若1molCH4还原NO2至N2,整个过程中放出的热量为867kJ,则ΔH2=___ 。
(3)有人认为:该研究可以使氨的合成反应,在铁催化剂表面进行时的效率大大提高,从而使原料的转化率大大提高。请你应用化学基本理论对此观点进行评价:___ 。

(1)某校化学研究性学习小组的同学在技术人员的指导下,按下列流程探究不同催化剂对NH3还原NO反应的催化性能。

若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体通过滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。为比较不同催化剂的催化性能,需要测量并记录的数据是
(2)在汽车的排气管上安装“催化转化器”(用铂、钯合金作催化剂),它的作用是使CO、NO反应生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧。
①写出CO与NO反应的化学方程式:
②用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);ΔH1=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);ΔH2
若1molCH4还原NO2至N2,整个过程中放出的热量为867kJ,则ΔH2=
(3)有人认为:该研究可以使氨的合成反应,在铁催化剂表面进行时的效率大大提高,从而使原料的转化率大大提高。请你应用化学基本理论对此观点进行评价:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用___________ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面___________ (填字母)反应释放的热量加热食物。
A.生石灰和水 B.浓硫酸和水
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料: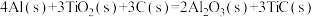
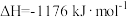 ,则反应过程中,每转移1mol电子放出的热量为
,则反应过程中,每转移1mol电子放出的热量为___________ 。
(4)肼可作为火箭发动机的燃料,与氧化剂 反应生成N2和水蒸气。
反应生成N2和水蒸气。
已知:①
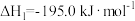
②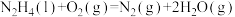
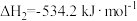
③
 ?
?
根据①与②的数据,计算 =
=___________ 。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(2)“即热饭盒”给人们生活带来方便,它可利用下面
A.生石灰和水 B.浓硫酸和水
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料:
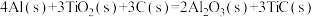
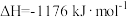 ,则反应过程中,每转移1mol电子放出的热量为
,则反应过程中,每转移1mol电子放出的热量为(4)肼可作为火箭发动机的燃料,与氧化剂
 反应生成N2和水蒸气。
反应生成N2和水蒸气。已知:①

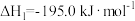
②
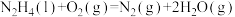
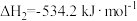
③

 ?
?根据①与②的数据,计算
 =
=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】根据实验数据写出下列反应能表现燃烧热的热化学方程式:
(1)沼气是一种能源,它的主要成分是CH4。0.5 mol CH4完全燃烧生成CO2和液态H2O时,放出445 kJ热量__________________________________ 。
(2)18 g葡萄糖固体(C6H12O6)与适量O2反应,生成CO2和液态水,放出280.4 kJ热量__________________________________ 。
(3)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和H2O(l)。已知室温下2 g SiH4自燃放出热量89.2 kJ__________________________________ 。
(1)沼气是一种能源,它的主要成分是CH4。0.5 mol CH4完全燃烧生成CO2和液态H2O时,放出445 kJ热量
(2)18 g葡萄糖固体(C6H12O6)与适量O2反应,生成CO2和液态水,放出280.4 kJ热量
(3)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和H2O(l)。已知室温下2 g SiH4自燃放出热量89.2 kJ
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】 时,
时, 燃烧生成
燃烧生成 放热
放热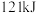 ,
,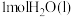 蒸发吸热
蒸发吸热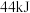 ,表示
,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为_______ 。
 时,
时, 燃烧生成
燃烧生成 放热
放热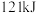 ,
,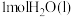 蒸发吸热
蒸发吸热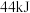 ,表示
,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】东京奥运会火炬传递的火炬样式采用樱花形状。奥运会火炬常用的燃料为丙烷(C3H8)、丁烷(C4H10)等。已知:
(1)写出丙烷燃烧热的热化学方程式:___________ 。
(2)下列有关说法不正确的是___________ (填字母)。
A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.异丁烷分子中的碳氢键比正丁烷多
C.正丁烷比异丁烷稳定
(3)现有3 mol由甲烷和乙烷组成的混合气体,完全燃烧放出的热量是3340 kJ,则该混合气体中甲烷和乙烷的物质的量之比是___________ 。
| 化合物 | 甲烷CH4 | 乙烷C2H6 | 丙烷C3H8 | 正丁烷CH3CH2CH2CH3 | 异丁烷CH3CH(CH3)2 |
| 燃烧热kJ·mol-1 | 890 | 1560 | 2220 | 2878 | 2870 |
(2)下列有关说法不正确的是
A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.异丁烷分子中的碳氢键比正丁烷多
C.正丁烷比异丁烷稳定
(3)现有3 mol由甲烷和乙烷组成的混合气体,完全燃烧放出的热量是3340 kJ,则该混合气体中甲烷和乙烷的物质的量之比是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】氯及其化合物在生活和生产中应用广泛。已知:
Cl2(g)+2NaOH(aq)=NaCl(aq)+NaClO(aq)+H2O(l) △H1=-102 kJ∙mol−1
3Cl2(g) + 6NaOH(aq)=5NaCl(aq)+NaClO3(aq) + 3H2O(1) △H2=-422 kJ∙mol−1
(1)写出在溶液中NaClO分解生成NaClO3的热化学方程式_______________ 。
(2)有研究表明,生成NaClO3的反应分两步进行:
I.2ClO-=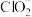 +Cl-;II.
+Cl-;II. +ClO-=
+ClO-=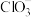 +Cl-
+Cl-
常温下,反应II能快速进行,但氯气与NaOH溶液反应很难得到NaClO3,试用碰撞理论解释其原因:________________________ 。
Cl2(g)+2NaOH(aq)=NaCl(aq)+NaClO(aq)+H2O(l) △H1=-102 kJ∙mol−1
3Cl2(g) + 6NaOH(aq)=5NaCl(aq)+NaClO3(aq) + 3H2O(1) △H2=-422 kJ∙mol−1
(1)写出在溶液中NaClO分解生成NaClO3的热化学方程式
(2)有研究表明,生成NaClO3的反应分两步进行:
I.2ClO-=
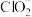 +Cl-;II.
+Cl-;II. +ClO-=
+ClO-=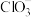 +Cl-
+Cl-常温下,反应II能快速进行,但氯气与NaOH溶液反应很难得到NaClO3,试用碰撞理论解释其原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知某反应器中存在如下反应:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1
ii.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2
iii.CH4(g)=C(s)+2H2(g) ΔH3
……
ⅲ为积炭反应,利用ΔH1和ΔH2计算ΔH3时,还需要利用_______ 反应的ΔH。
i.CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1
ii.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2
iii.CH4(g)=C(s)+2H2(g) ΔH3
……
ⅲ为积炭反应,利用ΔH1和ΔH2计算ΔH3时,还需要利用
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(1)已知拆开1mol H—H键、1mol N—H键、1mol N≡N键需要的能量分别是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为_____________________ 。
(2)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
①2O2(g)+N2(g)=N2O4(l) ΔH1 ②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=-1048.9kJ/mol
上述反应热效应之间的关系式为ΔH4=____________________________________ 。
(2)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
①2O2(g)+N2(g)=N2O4(l) ΔH1 ②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=-1048.9kJ/mol
上述反应热效应之间的关系式为ΔH4=
您最近一年使用:0次

 、
、 为原料生产尿素[
为原料生产尿素[ ]的反应历程与能量变化示意图如下:
]的反应历程与能量变化示意图如下:
 。(用
。(用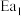 、
、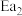 、
、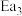 、
、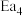 表示,下同)
表示,下同)

