如图为原电池装置示意图。

请回答下列问题:
(1)若A为Zn片,B为石墨棒,电解质溶液为稀硫酸,则A电极是原电池的___ 极,写出正极的电极反应式:___ 。
(2)若A为铜片,B为银片,电解质溶液为AgNO3溶液,则银片为___ (填“正”或“负”)极,写出电极反应式:负极___ ,正极___ 。
(3)若A、B均为铂片,电解质溶液为KOH溶液,分别从A、B两极通H2、O2,该电池为氢氧燃烧电池,则其负极的电极反应式为___ 。

请回答下列问题:
(1)若A为Zn片,B为石墨棒,电解质溶液为稀硫酸,则A电极是原电池的
(2)若A为铜片,B为银片,电解质溶液为AgNO3溶液,则银片为
(3)若A、B均为铂片,电解质溶液为KOH溶液,分别从A、B两极通H2、O2,该电池为氢氧燃烧电池,则其负极的电极反应式为
更新时间:2021-09-22 16:23:25
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】如图所示的原电池:当电解质溶液为稀H2SO4时,回答下列问题:
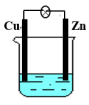
(1)Zn电极是___________ (填“正”或“负”)极,其电极反应为___________ ,该反应是___________ (填“氧化”或“还原”,下同)反应;
(2)Cu电极是___________ 极,其电极反应为___________ ,该反应是___________ 反应。
(3)装置中锌的作用是___________ ,稀硫酸的作用是___________
A.电极材料 B.电极反应物
C.电子导体 D.离子导体

(1)Zn电极是
(2)Cu电极是
(3)装置中锌的作用是
A.电极材料 B.电极反应物
C.电子导体 D.离子导体
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】锌锰干电池是生活中常见的一种一次电池,其构造如图所示。
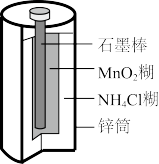
(1)锌筒上发生反应的电极反应式是_______ ,从氧化还原反应的角度分析,该电极上发生的反应属于_______ 反应。
(2)石墨棒是电池的_______ 极(填“正”或“负”)。
(3)该电池在工作过程中,外电路中电子的流动方向是_______ 。

(1)锌筒上发生反应的电极反应式是
(2)石墨棒是电池的
(3)该电池在工作过程中,外电路中电子的流动方向是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】完成下列问题
(1)与MnO2—Zn电池类似,K2FeO4—Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为___________ ,该电池总反应的离子方程式为___________ 。
(2)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是___________ 。
(1)与MnO2—Zn电池类似,K2FeO4—Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为
(2)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】Ⅰ.依据氧化还原反应2Fe3+(aq)+Cu(s)=Cu2+(aq)+2Fe2+(aq)设计的原电池如图所示。请回答下列问题:
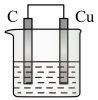
(1)电解质溶液是____________ (填化学式)溶液。
(2)Cu电极上发生的电极反应为_________ 。
(3)石墨电极上发生反应的类型为__________ (填“氧化”或“还原”)反应。
(4)当有0.05mol电子通过外电路时,两极材料的质量变化相差______ g。
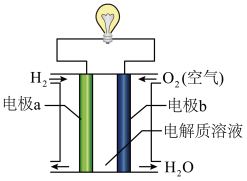
Ⅱ.某种氢氧燃料电池是用稀硫酸作电解质溶液,其装置如图。电子从a极____ (填“流入”或“流出”),电极b的电极反应式为____ 。

(1)电解质溶液是
(2)Cu电极上发生的电极反应为
(3)石墨电极上发生反应的类型为
(4)当有0.05mol电子通过外电路时,两极材料的质量变化相差
Ⅱ.某种氢氧燃料电池是用稀硫酸作电解质溶液,其装置如图。电子从a极

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】I.已知:①2Cu2S(s)+3O2(g)=2Cu2O(s)+2SO2(g) ΔH=−768.2 kJ∙mol−1
②2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g) ΔH=+116.0 kJ∙mol−1
(1)则Cu2S(s)+O2(g)=2Cu(s)+SO2(g) ΔH=_______ 。
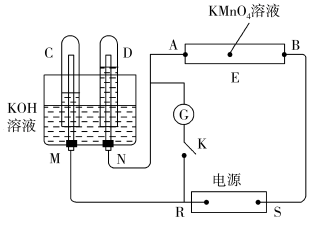
II.如图所示,E为浸过含酚酞的Na2SO4溶液的滤纸;A、B均为铂片,压在滤纸两端;R、S为电源的电极;M、N是用多微孔的Ni制成的电极,在碱溶液中可视为惰性电极:G为电流计;K为开关;C、D和电解池中都充满浓KOH溶液。若在滤纸中央滴一滴紫色的KMnO4溶液,将开关K打开,接通电源一段时间后,C、D中有气体产生。
回答下列问题:
(2)R为_______ (填“正”或“负”)极。
(3)通电一段时间后,M极附近溶液的pH_______ (填“变大”、“变小”或“不变”);B极区的电极反应式为_______ 。
(4)滤纸上的紫色点向_______ (填“A”或“B”)方向移动。
(5)通电一段时间后,C、D中的气体产生到一定量时,切断外电源并接通开关K,C、D中的气体逐渐减少,C中的电极反应式为_______ 。
②2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g) ΔH=+116.0 kJ∙mol−1
(1)则Cu2S(s)+O2(g)=2Cu(s)+SO2(g) ΔH=
II.如图所示,E为浸过含酚酞的Na2SO4溶液的滤纸;A、B均为铂片,压在滤纸两端;R、S为电源的电极;M、N是用多微孔的Ni制成的电极,在碱溶液中可视为惰性电极:G为电流计;K为开关;C、D和电解池中都充满浓KOH溶液。若在滤纸中央滴一滴紫色的KMnO4溶液,将开关K打开,接通电源一段时间后,C、D中有气体产生。

回答下列问题:
(2)R为
(3)通电一段时间后,M极附近溶液的pH
(4)滤纸上的紫色点向
(5)通电一段时间后,C、D中的气体产生到一定量时,切断外电源并接通开关K,C、D中的气体逐渐减少,C中的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】Ⅰ.下图为氢氧燃料电池原理示意图,按下图的提示,回答以下问题:
(1)若电解质溶液为KOH溶液,则写出电极反应式: 极
极 ____________ , 极
极 _______________ 。
(2)若电解质溶液为稀H2SO4,则写出电极反应式: 极
极 _____________ , 极
极 _______________ 。

Ⅱ.氨基甲酸铵分解反应为NH2COONH4(s) 2NH3(g)+CO2(g),在体积不变的密闭容器中发生反应,可以判断该反应已经达到平衡的是
2NH3(g)+CO2(g),在体积不变的密闭容器中发生反应,可以判断该反应已经达到平衡的是__________ 。
A.密闭容器中氨气的体积分数不变 B.1molNH2COONH4分解同时有44gCO2消耗
C.密闭容器中混合气体的密度不变 D.
(1)若电解质溶液为KOH溶液,则写出电极反应式:
 极
极  极
极 (2)若电解质溶液为稀H2SO4,则写出电极反应式:
 极
极  极
极 
Ⅱ.氨基甲酸铵分解反应为NH2COONH4(s)
 2NH3(g)+CO2(g),在体积不变的密闭容器中发生反应,可以判断该反应已经达到平衡的是
2NH3(g)+CO2(g),在体积不变的密闭容器中发生反应,可以判断该反应已经达到平衡的是A.密闭容器中氨气的体积分数不变 B.1molNH2COONH4分解同时有44gCO2消耗
C.密闭容器中混合气体的密度不变 D.

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
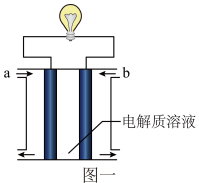
【推荐2】图一所示是一个燃料电池的示意图,a、b表示通入的气体,当此燃料电池工作时:_______ 。(设气体为同温、同压)
(2)如果a极通入CH4,b极通入O2,NaOH溶液作电解质溶液,则通CH4的电极上的电极反应为:________ 。
(3)如果a极通入乙烯,b极通入O2,H2SO4溶液作电解质溶液,则通乙烯的电极上的电极反应为:_________ 。
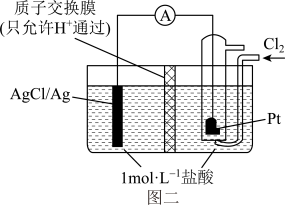
(4)某原电池装置初始状态如图二所示,交换膜两侧的溶液体积均为2L,该电池总反应为_______ ,当电路中转移1mol电子时,共有_______ mol离子通过交换膜,交换膜右侧溶液中c(HCl)=_______ mol•L-1(忽略溶液体积变化和Cl2溶于水)。
(2)如果a极通入CH4,b极通入O2,NaOH溶液作电解质溶液,则通CH4的电极上的电极反应为:
(3)如果a极通入乙烯,b极通入O2,H2SO4溶液作电解质溶液,则通乙烯的电极上的电极反应为:
(4)某原电池装置初始状态如图二所示,交换膜两侧的溶液体积均为2L,该电池总反应为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】积极发展清洁能源,推动经济社会绿色低碳转型,已经成为国际社会应对全球气候变化的普遍共识。
(1)甲醇 是一种重要的清洁燃料。甲醇燃烧时,能量的主要转化形式是
是一种重要的清洁燃料。甲醇燃烧时,能量的主要转化形式是____________ 转化为___________ ;其燃烧反应中反应物的总能量_____________ (填“大于”“小于”或“等于”)生成物的总能量。
(2)氢能是最理想的清洁能源。某氢能源公交车使用的燃料电池结构示意图(质子交换膜传导 )如图。
)如图。__________ 反应, 由
由_______ (填“M”或“N”,下同)极移向_________ 极。
②该电池工作时,M极的电极反应式为________________________________ 。
③与传统的发动机供能相比,氢能源供能的优点是_____________________ (任写一点)。
④每转移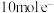 ,消耗氢气的质量为
,消耗氢气的质量为___________  。
。
(1)甲醇
 是一种重要的清洁燃料。甲醇燃烧时,能量的主要转化形式是
是一种重要的清洁燃料。甲醇燃烧时,能量的主要转化形式是(2)氢能是最理想的清洁能源。某氢能源公交车使用的燃料电池结构示意图(质子交换膜传导
 )如图。
)如图。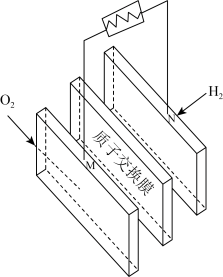
 由
由②该电池工作时,M极的电极反应式为
③与传统的发动机供能相比,氢能源供能的优点是
④每转移
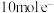 ,消耗氢气的质量为
,消耗氢气的质量为 。
。
您最近一年使用:0次



