回答下列问题
I.写出下列物质的电离方程式
(1)HCl_______
(2)HClO_______
(3)NaOH_______
(4)NaCl_______
II.配平下列氧化还原方程式:
(5)_______ClO2+_______I-=_______ClO +_______I2
+_______I2_______
(6)_______H2O2+_______H++_______Fe2+=_______Fe3++_______H2O_______
(7)_______MnO +_______H++_______Cl-=_______Mn2++_______Cl2↑+_______H2O
+_______H++_______Cl-=_______Mn2++_______Cl2↑+_______H2O_______
I.写出下列物质的电离方程式
(1)HCl
(2)HClO
(3)NaOH
(4)NaCl
II.配平下列氧化还原方程式:
(5)_______ClO2+_______I-=_______ClO
 +_______I2
+_______I2(6)_______H2O2+_______H++_______Fe2+=_______Fe3++_______H2O
(7)_______MnO
 +_______H++_______Cl-=_______Mn2++_______Cl2↑+_______H2O
+_______H++_______Cl-=_______Mn2++_______Cl2↑+_______H2O
更新时间:2021-10-02 16:42:59
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有下列8种物质:①石墨;②氯化氢气体;③酒精;④铝;⑤二氧化碳;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧氯化银固体。
(1)属于电解质的是:______ 。
(2)属于非电解质的是:______ ;
(3)其中能导电的是:______ ;
(4)⑥在水溶液中的电离方程式为____ 。
(5)上述8种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为___ 。
(1)属于电解质的是:
(2)属于非电解质的是:
(3)其中能导电的是:
(4)⑥在水溶液中的电离方程式为
(5)上述8种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.写出下列反应的离子方程式:
(1)硫酸铜溶液和氢氧化钡溶液混合___________ 。
(2)向足量澄清石灰水中通入二氧化碳___________ 。
(3)稀 与
与 溶液的离子方程式:
溶液的离子方程式:___________ 。
(4)向澄清石灰水中滴加足量的碳酸氢钠溶液:___________ 。
(5)写出稀氢氧化钠溶液与氯化铵溶液的离子方程式:___________ 。
II.
(6)写出下列物质的电离方程式:
 :
:___________ ;
 :
:___________ ;
 :
:___________ 。
(1)硫酸铜溶液和氢氧化钡溶液混合
(2)向足量澄清石灰水中通入二氧化碳
(3)稀
 与
与 溶液的离子方程式:
溶液的离子方程式:(4)向澄清石灰水中滴加足量的碳酸氢钠溶液:
(5)写出稀氢氧化钠溶液与氯化铵溶液的离子方程式:
II.
(6)写出下列物质的电离方程式:
 :
: :
: :
:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】“分类”的思想在化学学习及化学学科发展中起着重要作用。现有下列物质:
① 固体 ②熔融
固体 ②熔融 ③淀粉溶液 ④液态氯化氢 ⑤
③淀粉溶液 ④液态氯化氢 ⑤ 溶液 ⑥
溶液 ⑥ ⑦金属铜 ⑧
⑦金属铜 ⑧ ⑨酒精 ⑩
⑨酒精 ⑩
回答下列问题:
(1)以上物质中属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
(2)②熔融 能导电,其电离方程式为
能导电,其电离方程式为___________ 。
(3)③淀粉溶液,⑤ 溶液二者如果混合,可采用
溶液二者如果混合,可采用___________ 方法分离。
(4)⑧ 与水的反应属于氧化还原反应,化学方程式为
与水的反应属于氧化还原反应,化学方程式为___________ ,每当有 参与反应,转移电子数为
参与反应,转移电子数为___________ (设 为阿伏伽德罗常数的值)。
为阿伏伽德罗常数的值)。
(5)已知⑨ (亚磷酸)与足量
(亚磷酸)与足量 溶液反应的化学方程式为
溶液反应的化学方程式为 ,
, 属于
属于___________ (填“正盐”或“酸式盐”)。
①
 固体 ②熔融
固体 ②熔融 ③淀粉溶液 ④液态氯化氢 ⑤
③淀粉溶液 ④液态氯化氢 ⑤ 溶液 ⑥
溶液 ⑥ ⑦金属铜 ⑧
⑦金属铜 ⑧ ⑨酒精 ⑩
⑨酒精 ⑩
回答下列问题:
(1)以上物质中属于电解质的是
(2)②熔融
 能导电,其电离方程式为
能导电,其电离方程式为(3)③淀粉溶液,⑤
 溶液二者如果混合,可采用
溶液二者如果混合,可采用(4)⑧
 与水的反应属于氧化还原反应,化学方程式为
与水的反应属于氧化还原反应,化学方程式为 参与反应,转移电子数为
参与反应,转移电子数为 为阿伏伽德罗常数的值)。
为阿伏伽德罗常数的值)。(5)已知⑨
 (亚磷酸)与足量
(亚磷酸)与足量 溶液反应的化学方程式为
溶液反应的化学方程式为 ,
, 属于
属于
您最近半年使用:0次
【推荐1】Ⅰ高铁酸钠 )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法是用次氯酸钠氧化氯化铁溶液,离子方程式如下(未配平)
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法是用次氯酸钠氧化氯化铁溶液,离子方程式如下(未配平)



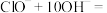




 _______
_______
(1)完成上述离子方程式并进行配平_______ ;
(2)反应中 是
是_______ (填“还原产物”或“氧化产物”)。
Ⅱ.火药是中国的“四大发明”之一。黑火药在发生爆炸时,发生如下反应: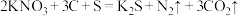 。
。
(3)用双线桥表示以上反应的电子转移数目和方向_______ ;
(4)其中被还原的元素是_______ (填元素名称)。
 )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法是用次氯酸钠氧化氯化铁溶液,离子方程式如下(未配平)
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法是用次氯酸钠氧化氯化铁溶液,离子方程式如下(未配平)


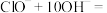




 _______
_______(1)完成上述离子方程式并进行配平
(2)反应中
 是
是Ⅱ.火药是中国的“四大发明”之一。黑火药在发生爆炸时,发生如下反应:
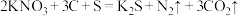 。
。(3)用双线桥表示以上反应的电子转移数目和方向
(4)其中被还原的元素是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】书写下列方程式
(1)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2气体,还生成CO2和KHSO4等物质。写出该反应的化学方程式___________ 。
(2)Pb与C同主族,化合价有+2价和+4价,PbO与PbO2是铅的两种常见氧化物,已知PbO2具有强氧化性,与浓盐酸共热可生成一种黄绿色气体。试写出Pb3O4与浓盐酸反应的化学方程式___________ 。
(3)I2在KOH溶液中反应,产物之一是KIO3,该过程的离子反应方程式为___________ 。
(4)在碱性条件下,Cl2可将废水中的CN—氧化为无毒的CO2、N2,该过程的离子反应方程式为___________ 。
(5)在酸性条件下,向含铬废水中加入FeSO4,可将Cr2O 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为___________ 。
(1)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2气体,还生成CO2和KHSO4等物质。写出该反应的化学方程式
(2)Pb与C同主族,化合价有+2价和+4价,PbO与PbO2是铅的两种常见氧化物,已知PbO2具有强氧化性,与浓盐酸共热可生成一种黄绿色气体。试写出Pb3O4与浓盐酸反应的化学方程式
(3)I2在KOH溶液中反应,产物之一是KIO3,该过程的离子反应方程式为
(4)在碱性条件下,Cl2可将废水中的CN—氧化为无毒的CO2、N2,该过程的离子反应方程式为
(5)在酸性条件下,向含铬废水中加入FeSO4,可将Cr2O
 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】阅读下面科普信息,回答问题:
一个体重50 kg的健康人含铁2 g,这2 g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是____
A.Fe
B.Fe2+
C.Fe3+
(2)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有________ 性。
(3)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了______ 性。
(4)钒性能优良,用途广泛,有金属“维生素”之称。将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应的化学方程式是________ 。
(5)V2O5能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与Na2SO3溶液反应被吸收,则 、Cl-、VO2+还原性由大到小的顺序是
、Cl-、VO2+还原性由大到小的顺序是________ 。
(6)在20.00 mL 0.1 mol.L-1 溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是
溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是 ________ 。
a.VO2+ b. c. V2+ d.V
c. V2+ d.V
一个体重50 kg的健康人含铁2 g,这2 g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.Fe
B.Fe2+
C.Fe3+
(2)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(3)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
(4)钒性能优良,用途广泛,有金属“维生素”之称。将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应的化学方程式是
(5)V2O5能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与Na2SO3溶液反应被吸收,则
 、Cl-、VO2+还原性由大到小的顺序是
、Cl-、VO2+还原性由大到小的顺序是(6)在20.00 mL 0.1 mol.L-1
 溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是
溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是 a.VO2+ b.
 c. V2+ d.V
c. V2+ d.V
您最近半年使用:0次



