已知热化学方程式2SO2(g)+O2(g)2SO3(g)ΔH=-QkJ/mol(Q>0),则下列说法正确的是
| A.降低温度,平衡正向移动,方程式中的Q值增大 |
| B.若该反应放热QkJ,则此过程中有2molSO2(g)被氧化 |
| C.将2molSO3(g)置于一密闭容器中充分反应,需吸收QkJ的热量 |
| D.2molSO2、1molO2分子中的键能总和大于2molSO3分子中的键能 |
19-20高二上·广东广州·期末 查看更多[9]
浙江省精诚联盟2022-2023学年高二上学期10月联考化学试题山东省青岛市第十九中学2021-2022学年高二上学期10月月考化学试题(已下线)必考点03 化学平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)江西省九江市第三中学2021-2022学年高二上学期第一次月考化学试卷河北深州市长江中学2021-2022学年高二上学期10月月考化学(理)试题内蒙古北京四中呼和浩特分校2021-2022学年高二上学期第一次月考化学试题江西省南昌市南昌大学附属中学 2021-2022学年高二上学期第一次月考化学试卷河北省迁安市2020-2021学年高二上学期期末考试化学试题广东省广州市执信中学(广雅,执信,二中联考)2019-2020学年高二上学期期末考试化学试题
更新时间:2021-10-11 16:29:33
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】反应N2+3H2=2NH3的能量变化如图,其热化学方程式正确的是


| A.N2(g)+3H2(g)=2NH3(l)ΔH=+(b+c-a)kJ·mol-1 |
| B.N2(g)+3H2(g)=2NH3(g) ΔH=+2(b-a)kJ·mol-1 |
| C.N2(g)+3H2(g)=2NH3(l) ΔH=-2(b+c-a)kJ·mol-1 |
| D.N2(g)+3H2(g)=2NH3(g)ΔH=+(a+b)kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某化学反应的反应过程中的能量变化如图所示,下列说法正确的是


| A.该反应必须在加热条件下才能进行 |
| B.该反应过程中,反应物断键所吸收的总能量大于生成物成键所放出的总能量 |
| C.甲烷燃烧过程中的能量变化与图中趋势一致 |
| D.该反应为放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】2021年10月,神舟十三号载人飞船成功发射。载人飞船中通过如下过程实现O2再生:
①CO2(g)+4H2(g)=CH4(g)+2H2O(l) ΔH1=-252.9 kJ·mol-1
②2H2O(1)=2H2(g)+O2(g) ΔH2=+571.6 kJ·mol-1
下列说法错误的是
①CO2(g)+4H2(g)=CH4(g)+2H2O(l) ΔH1=-252.9 kJ·mol-1
②2H2O(1)=2H2(g)+O2(g) ΔH2=+571.6 kJ·mol-1
下列说法错误的是
| A.H2的燃烧热ΔH = -285.8 kJ·mol-1 |
| B.反应2H2(g)+O2(g)=2H2O(g)的 ΔH<-571.6 kJ·mol-1 |
| C.反应2H2(g)+O2(g)=2H2O(l) 常温下能自发进行 |
| D.反应CH4(g)+2O2(g)=CO2(g)+2H2O(l)的 ΔH=-890.3 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】部分物质的燃烧热如下表,下列关于CH4和水蒸气反应得到H2和CO的热化学方程式正确的是
注:1 mol H2O(g)转变成1 mol H2O(l)时放热44.0 kJ。
| 物质 | 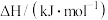 |
| H2 | -285.8 |
| CO | -283.0 |
| CH4 | -890.0 |
A. |
B. |
C.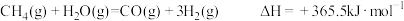 |
D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关说法正确的是
A.常温下,向 溶液中加入少量盐酸,溶液中 溶液中加入少量盐酸,溶液中 的值增大 的值增大 |
B.反应 常温下能自发进行,则该反应的 常温下能自发进行,则该反应的 |
C.一定条件下, 碘蒸气和 碘蒸气和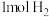 充分混合反应生成HI并放热 充分混合反应生成HI并放热 ,则该反应的热化学方程式为: ,则该反应的热化学方程式为: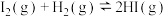 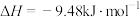 |
D.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 不同 不同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】充分燃烧一定量的丁烷(C4H10)气体放出的热量为Q。完全吸收它生成的CO2气体生成正盐,需5 mol·L-1的NaOH溶液100 mL,则丁烷的燃烧热为( )
| A.16Q | B.8Q | C.4Q | D.2Q |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在新型催化剂 作用下,
作用下, 氧化
氧化 可获得Cl2:
可获得Cl2: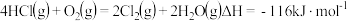 。关于反应
。关于反应 ,下列说法正确的是
,下列说法正确的是
 作用下,
作用下, 氧化
氧化 可获得Cl2:
可获得Cl2: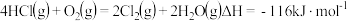 。关于反应
。关于反应 ,下列说法正确的是
,下列说法正确的是A.反应活化能: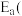 正 正 逆 逆 |
B.每生成标准状况下22.4L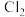 ,放出 ,放出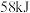 的热量 的热量 |
C.使用高效催化剂,可使平衡时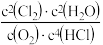 的值增大 的值增大 |
D.断裂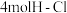 键的同时,有 键的同时,有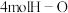 键生成,说明该反应达到平衡状态 键生成,说明该反应达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】阿伏伽德罗常数的值约6.02×1023mol-1,下列叙述中错误的是
①12.4g白磷晶体中含有的P-P键数是0.6×6.02×1023
②电解精炼铜时转移了6.02×1023个电子,阳极溶解32g铜
③7.8gNa2S和Na2O2的混合物中含有阴离子数大于0.1×6.02×1023
④2molSO2和1molO2混合在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数大于2×6.02×1023
⑤6.8g熔融的KHSO4中含有0.1NA个阳离子
⑥1.00molNaCl中,所有Na+的最外层电子总数为10×6.02×1023
①12.4g白磷晶体中含有的P-P键数是0.6×6.02×1023
②电解精炼铜时转移了6.02×1023个电子,阳极溶解32g铜
③7.8gNa2S和Na2O2的混合物中含有阴离子数大于0.1×6.02×1023
④2molSO2和1molO2混合在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数大于2×6.02×1023
⑤6.8g熔融的KHSO4中含有0.1NA个阳离子
⑥1.00molNaCl中,所有Na+的最外层电子总数为10×6.02×1023
| A.①②③④ | B.③④⑤⑥ | C.②③⑤⑥ | D.③④⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知2SO2(g)+O2(g)⇌2SO3(g)+QkJ•mol-1(Q>0)。下列说法正确的是( )
| A.相同条件下,2molSO2(g)和1molO2(g)所具有的能量小于2molSO3(g)所具有的能量 |
| B.将2molSO2(g)和1molO2(g)充分反应后可放出的热量为QkJ |
| C.增大压强或升高温度,该平衡都向逆反应方向移动 |
| D.若充分反应后放热QkJ,则此过程中有2molSO2(g)被氧化 |
您最近一年使用:0次

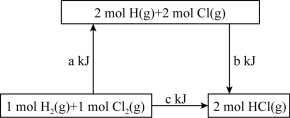
 和1mol
和1mol 反应生成2mol
反应生成2mol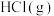 放出ckJ的热量
放出ckJ的热量 键需要吸收bkJ能量
键需要吸收bkJ能量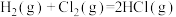 ,反应物的总能量小于生成物的总能量
,反应物的总能量小于生成物的总能量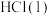 分解成lmol
分解成lmol 体积,且C(s)+
体积,且C(s)+ Z(g)。下列说法正确的是
Z(g)。下列说法正确的是

