天然气作为民生工程受到人们普遍关注。已知天然气不完全燃烧的化学方程式为3O2(g)+2CH4(g)=2CO(g)+4H2O(g) ∆H(单位:kJ/mol)。且O=O键的键能为a kJ/mol,C—H键的键能为b kJ/mol,C≡O的键能为c kJ/mol,O-H键的键能为d kJ/mol,则甲烷不完全燃烧的∆H为
| A.3a+8b-2c-8d | B.3a+8b-2c-4d |
| C.2c+8d-3a-4b | D.2c+8d-3a-8b |
更新时间:2021-10-13 23:20:36
|
相似题推荐
【推荐1】工业上,在一定条件下利用乙烯和水蒸气反应制备乙醇。化学原理:CH2=CH2(g)+H2O(g)=CH3CH2OH(g) ΔH。已知几种共价键的键能如下表所示:
下列说法中错误的是
| 化学键 | C-H | C=C | H-O | C-C | C-O |
| 键能/(kJ•mol-1) | 413 | 615 | 463 | 348 | 351 |
| A.上述合成乙醇的反应是加成反应 |
| B.碳碳双键的键能小于碳碳单键键能的2倍 |
C.上述反应式中,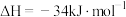 |
| D.相同时间段内,反应中用三种物质表示的反应速率不相等 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法正确的是
| A.氢氧燃料电池工作时化学能全部转化电能 |
| B.氢氧燃料电池的负极反应为O2+4H++4e-=2H2O |
| C.氢氧燃料电池放电过程中消耗11.2LH2,转移的电子数目为6.02×1023 |
| D.反应2H2(g)+O2(g)=2H2O(g)的ΔH可通过下式估算:ΔH=反应中断裂旧共价键的键能之和-反应中形成新共价键的键能之和 |
您最近一年使用:0次



