回答下列问题
(1)在101kPa时,4.0g硫粉在氧气中完全燃烧生成二氧化硫,放出27kJ的热量,硫的燃烧热为___________ ,硫燃烧的热化学方程式为___________ 。
(2)在101kPa时,氢气在1.00mol氧气中完全燃烧,生成2.00mol液态水,放出571.6kJ的热量,氢气的燃烧热为___________ ,表示氢气燃烧热的热化学方程式为___________ 。
(3)将煤转化为水煤气的主要化学反应为C(s)+H2O(g) CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1;H2(g)+
CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1;H2(g)+ O2(g)=H2O(g) ΔH=-242.0kJ·mol-1;CO(g)+
O2(g)=H2O(g) ΔH=-242.0kJ·mol-1;CO(g)+ O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
请回答:根据以上数据,写出C(s)与水蒸气反应的热化学反应方程式:___________ 。
(4)比较下列各组热化学方程式中ΔH的大小关系。
①S(s)+O2(g)=SO2(g) ΔH1 S(g)+O2(g)=SO2(g) ΔH2 ΔH1___________ ΔH2
②CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1 CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH2 ΔH1___________ ΔH2
(1)在101kPa时,4.0g硫粉在氧气中完全燃烧生成二氧化硫,放出27kJ的热量,硫的燃烧热为
(2)在101kPa时,氢气在1.00mol氧气中完全燃烧,生成2.00mol液态水,放出571.6kJ的热量,氢气的燃烧热为
(3)将煤转化为水煤气的主要化学反应为C(s)+H2O(g)
 CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1;H2(g)+
CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1;H2(g)+ O2(g)=H2O(g) ΔH=-242.0kJ·mol-1;CO(g)+
O2(g)=H2O(g) ΔH=-242.0kJ·mol-1;CO(g)+ O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0kJ·mol-1请回答:根据以上数据,写出C(s)与水蒸气反应的热化学反应方程式:
(4)比较下列各组热化学方程式中ΔH的大小关系。
①S(s)+O2(g)=SO2(g) ΔH1 S(g)+O2(g)=SO2(g) ΔH2 ΔH1
②CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1 CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH2 ΔH1
更新时间:2021-10-18 22:19:33
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知下列热化学方程式:
①H2(g)+ O2(g)=H2O(l) △H=-285.8 kJ·mol-1
O2(g)=H2O(l) △H=-285.8 kJ·mol-1
②H2O(g)=H2(g)+ O2(g) △H=+241.8 kJ·mol-1
O2(g) △H=+241.8 kJ·mol-1
③C(s)+ O2(g)= CO(g) △H=-110.5 kJ·mol-1
O2(g)= CO(g) △H=-110.5 kJ·mol-1
④CO2(g)=C(s)+O2(g) △H=+393.5 kJ·mol-1
回答下列问题:
(1)上述反应中属于放热反应的是_________________________ 。
(2)H2的燃烧热为____________ ,C的燃烧热为_____________ 。
(3)CO燃烧时的热化学反应方程式为______________________________ 。
①H2(g)+
 O2(g)=H2O(l) △H=-285.8 kJ·mol-1
O2(g)=H2O(l) △H=-285.8 kJ·mol-1 ②H2O(g)=H2(g)+
 O2(g) △H=+241.8 kJ·mol-1
O2(g) △H=+241.8 kJ·mol-1③C(s)+
 O2(g)= CO(g) △H=-110.5 kJ·mol-1
O2(g)= CO(g) △H=-110.5 kJ·mol-1④CO2(g)=C(s)+O2(g) △H=+393.5 kJ·mol-1
回答下列问题:
(1)上述反应中属于放热反应的是
(2)H2的燃烧热为
(3)CO燃烧时的热化学反应方程式为
您最近一年使用:0次
【推荐2】请根据学过的知识回答下列问题:
(1)
 完全燃烧生成液态水时放出341.7kJ热量,则表示
完全燃烧生成液态水时放出341.7kJ热量,则表示 燃烧热的热化学方程
燃烧热的热化学方程___________ 。
(2)已知: 键的键能是
键的键能是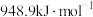 ,
, 键的键能是
键的键能是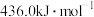 ,
, 键的键能是
键的键能是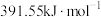 ,则
,则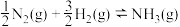

___________ 。
(3)已知:①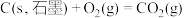

②

③

则298K时反应 的焓变:
的焓变:
___________ 。
(4)已知常温时红磷比白磷稳定,比较下列反应中 的大小:
的大小:
___________  。
。
①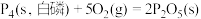

②

(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和
 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为___________ 。
(6)如图所示,某反应在不同条件下的反应历程分别为a、b。
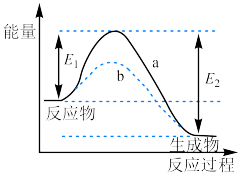
据图可判断出反应物的总键能___________ (填“>”“<”或“=”,下同)生成物的总键能,反应历程a、b的反应热___________ (填“相同”或“不相同”)。
(1)

 完全燃烧生成液态水时放出341.7kJ热量,则表示
完全燃烧生成液态水时放出341.7kJ热量,则表示 燃烧热的热化学方程
燃烧热的热化学方程(2)已知:
 键的键能是
键的键能是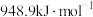 ,
, 键的键能是
键的键能是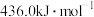 ,
, 键的键能是
键的键能是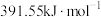 ,则
,则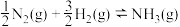

(3)已知:①
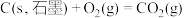

②


③


则298K时反应
 的焓变:
的焓变:
(4)已知常温时红磷比白磷稳定,比较下列反应中
 的大小:
的大小:
 。
。①
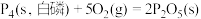

②


(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和

 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为(6)如图所示,某反应在不同条件下的反应历程分别为a、b。

据图可判断出反应物的总键能
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】我国对能源的需求量巨大,其中化石能源占比依然较高,因此发展新型清洁能源意义深远。甲醇汽油是将传统汽油与甲醇混合形成的一种新型燃料,煤可作为甲醇的生产原料。
(1)甲醇的合成可以来源于煤的气化和液化,已知该过程涉及以下反应:
Ⅰ.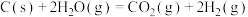

Ⅱ.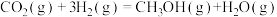

Ⅲ.

Ⅳ.
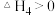

________ 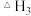 ,反应Ⅱ
,反应Ⅱ
________ 0,反应Ⅳ
________ 0(填序号)。
A.大于 B.小于 C.等于
(2)随着温度的变化,反应的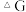 (自由能变化,也在变化,下图中可对应于步骤1的是
(自由能变化,也在变化,下图中可对应于步骤1的是________ 。

(3)汽油的主要成分之一是辛烷[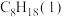 ]。已知:25℃、
]。已知:25℃、 时
时 完全燃烧生成气态二氧化碳和液态水,在该弹式热量计中完全燃烧,可以使得2kg的水升高66K(忽略弹式热量计自身部件吸热)。则
完全燃烧生成气态二氧化碳和液态水,在该弹式热量计中完全燃烧,可以使得2kg的水升高66K(忽略弹式热量计自身部件吸热)。则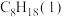 的燃烧热
的燃烧热
______ 。【已知:水的比热容是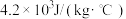 】
】
(1)甲醇的合成可以来源于煤的气化和液化,已知该过程涉及以下反应:
Ⅰ.
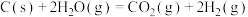

Ⅱ.
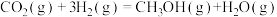

Ⅲ.


Ⅳ.

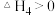

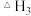 ,反应Ⅱ
,反应Ⅱ

A.大于 B.小于 C.等于
(2)随着温度的变化,反应的
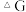 (自由能变化,也在变化,下图中可对应于步骤1的是
(自由能变化,也在变化,下图中可对应于步骤1的是
(3)汽油的主要成分之一是辛烷[
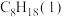 ]。已知:25℃、
]。已知:25℃、 时
时 完全燃烧生成气态二氧化碳和液态水,在该弹式热量计中完全燃烧,可以使得2kg的水升高66K(忽略弹式热量计自身部件吸热)。则
完全燃烧生成气态二氧化碳和液态水,在该弹式热量计中完全燃烧,可以使得2kg的水升高66K(忽略弹式热量计自身部件吸热)。则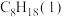 的燃烧热
的燃烧热
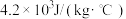 】
】
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】把煤作为燃料可通过下列两种途径:
途径Ⅰ:C(s)+O2(g)=CO2(g);ΔH1=-393.15kJ·mol-1 ①
途径Ⅱ:先制成水煤气:C(s)+H2O(g)=CO(g) +H2(g);ΔH2 ②
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g);ΔH3=-566kJ·mol-1 ③
2H2(g)+O2(g)=2H2O(g);ΔH4=-484kJ·mol-1 ④
请回答下列问题:
(1)途径Ⅰ放出的热量理论上_______ (填“大于”“等于”或“小于”)途径Ⅱ放出的热量。
(2)ΔH2=______ 。
(3)煤燃烧的烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减 少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为NO(g)+O3(g)=NO2(g)+O2(g) ΔH1=-200.9kJ·mol-1,NO(g)+ O2(g)=NO2(g) ΔH2=-58.2kJ·mol-1,SO2(g)+O3(g)=SO3(g)+O2(g) ΔH3=-241.6kJ·mol-1,则反应3NO(g)+O3(g)=3NO2(g)的ΔH=
O2(g)=NO2(g) ΔH2=-58.2kJ·mol-1,SO2(g)+O3(g)=SO3(g)+O2(g) ΔH3=-241.6kJ·mol-1,则反应3NO(g)+O3(g)=3NO2(g)的ΔH=________ 。
(4)在标准状况下的11.2L甲烷完全燃烧生成CO2和液态水放出444.8kJ热量(298K),能表示其燃烧热的热化学方程式是________ ;已知断裂1mol下列化学键需要吸收的能量分别为:C=O:745kJ;O=O键:496kJ;C-H键:414kJ,则断裂1molH-O键需要吸收的能量为_______ 。
途径Ⅰ:C(s)+O2(g)=CO2(g);ΔH1=-393.15kJ·mol-1 ①
途径Ⅱ:先制成水煤气:C(s)+H2O(g)=CO(g) +H2(g);ΔH2 ②
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g);ΔH3=-566kJ·mol-1 ③
2H2(g)+O2(g)=2H2O(g);ΔH4=-484kJ·mol-1 ④
请回答下列问题:
(1)途径Ⅰ放出的热量理论上
(2)ΔH2=
(3)煤燃烧的烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减 少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为NO(g)+O3(g)=NO2(g)+O2(g) ΔH1=-200.9kJ·mol-1,NO(g)+
 O2(g)=NO2(g) ΔH2=-58.2kJ·mol-1,SO2(g)+O3(g)=SO3(g)+O2(g) ΔH3=-241.6kJ·mol-1,则反应3NO(g)+O3(g)=3NO2(g)的ΔH=
O2(g)=NO2(g) ΔH2=-58.2kJ·mol-1,SO2(g)+O3(g)=SO3(g)+O2(g) ΔH3=-241.6kJ·mol-1,则反应3NO(g)+O3(g)=3NO2(g)的ΔH=(4)在标准状况下的11.2L甲烷完全燃烧生成CO2和液态水放出444.8kJ热量(298K),能表示其燃烧热的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列问题。
(1)0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水放出649.5kJ热量,其热化学方程式为:_______ ;又已知H2O(l)=H2O(g) ΔH=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量是_______ kJ。
(2)1mol氧气与足量氢气反应生成水蒸气放热483.6kJ,写出该反应的热化学方程式:_______ 。若1g水蒸气转化成液态水放热2.444kJ,写出表示氢气燃烧热的热化学方程式:_______ 。
(3)含11.2gKOH的稀溶液与1L0.1mol·L-1的H2SO4溶液反应放出11.46kJ的热量,该离子反应的热化学方程式为_______ ,则KOH与H2SO4反应的中和热为_______ 。
(4)已知:①C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3=141kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=_______ 。
(1)0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水放出649.5kJ热量,其热化学方程式为:
(2)1mol氧气与足量氢气反应生成水蒸气放热483.6kJ,写出该反应的热化学方程式:
(3)含11.2gKOH的稀溶液与1L0.1mol·L-1的H2SO4溶液反应放出11.46kJ的热量,该离子反应的热化学方程式为
(4)已知:①C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3=141kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求回答下列问题:
(1)下列变化属于吸热反应的是______ (填序号)。
①钠与冷水的反应 ②氢氧化钡晶体与氯化铵固体的反应 ③蓝矾失水变为白色粉末 ④干冰升华
⑤ 固体溶于水
固体溶于水
(2)强酸与强碱的稀溶液发生中和反应生成1mol 时的反应热
时的反应热 。若用一定浓度的稀硫酸与含10gNaOH的稀碱溶液完全反应,反应放出的热量为
。若用一定浓度的稀硫酸与含10gNaOH的稀碱溶液完全反应,反应放出的热量为______ 。(结果保留小数点后一位)
(3)已知1g 完全燃烧生成液态水时放出热量142.9kJ,则氢气的燃烧热为
完全燃烧生成液态水时放出热量142.9kJ,则氢气的燃烧热为______ ,试写出该反应的热化学方程式为______ 。
(4)试比较反应热的大小:
①



则
______  (填“>”或“<”,下同)。
(填“>”或“<”,下同)。
②已知常温时红磷比白磷稳定。
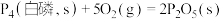

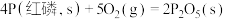

则
______  。
。
(5)已知:25℃、101kPa时,
①

②

③
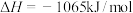
则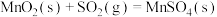

______ 。
(1)下列变化属于吸热反应的是
①钠与冷水的反应 ②氢氧化钡晶体与氯化铵固体的反应 ③蓝矾失水变为白色粉末 ④干冰升华
⑤
 固体溶于水
固体溶于水(2)强酸与强碱的稀溶液发生中和反应生成1mol
 时的反应热
时的反应热 。若用一定浓度的稀硫酸与含10gNaOH的稀碱溶液完全反应,反应放出的热量为
。若用一定浓度的稀硫酸与含10gNaOH的稀碱溶液完全反应,反应放出的热量为(3)已知1g
 完全燃烧生成液态水时放出热量142.9kJ,则氢气的燃烧热为
完全燃烧生成液态水时放出热量142.9kJ,则氢气的燃烧热为(4)试比较反应热的大小:
①




则

 (填“>”或“<”,下同)。
(填“>”或“<”,下同)。②已知常温时红磷比白磷稳定。
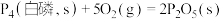

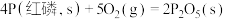

则

 。
。(5)已知:25℃、101kPa时,
①


②


③

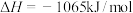
则
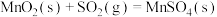

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)在1200℃时,天然气脱硫工艺中会发生下列反应:
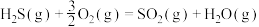







则用 、
、 、
、 来表示
来表示 的表达式为
的表达式为___________ 。
(2)已知甲烷能催化还原 ,得到氮气、二氧化碳和水蒸气,且知反应消耗1.6g甲烷时,放出热量86.7kJ,写出甲烷催化还原
,得到氮气、二氧化碳和水蒸气,且知反应消耗1.6g甲烷时,放出热量86.7kJ,写出甲烷催化还原 的热化学方程式
的热化学方程式________ 。
(3)已知:

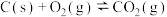
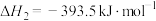
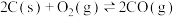

若某反应的平衡常数表达式为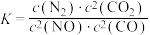 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式_______ 。
(4)利用如图所示装置测定中和热的实验步骤如下:

步骤一:用量筒量取50mL 0.50 盐酸倒入内筒中,测出盐酸温度;
盐酸倒入内筒中,测出盐酸温度;
步骤二:用另一量筒量取50mL 0.55 NaOH溶液,并用同一温度计测出其温度;
NaOH溶液,并用同一温度计测出其温度;
步骤三:将NaOH溶液倒入内筒中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
①假设盐酸和氢氧化钠溶液的密度都是1 ,又知中和反应后生成溶液的比热容c=4.18
,又知中和反应后生成溶液的比热容c=4.18 。为了计算中和热,某学生实验记录数据如下:
。为了计算中和热,某学生实验记录数据如下:
已知在上述实验中生成 的物质的量为0.025mol,依据该学生的实验数据计算,该实验测得的中和热ΔH=
的物质的量为0.025mol,依据该学生的实验数据计算,该实验测得的中和热ΔH=________ (结果保留一位小数)[ 已知热量计算公式为 ] 。
] 。
②该同学通过实验测出的中和热与理论值(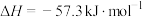 )有偏差,造成这一结果可能的原因是
)有偏差,造成这一结果可能的原因是________ 。
A.实验装置保温、隔热效果差
B.用测量盐酸的温度计直接测定NaOH溶液的温度
C.将NaOH溶液一次性迅速倒入量热计内筒中,并立即盖上杯盖
③现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1L 1 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为________ 。
(1)在1200℃时,天然气脱硫工艺中会发生下列反应:
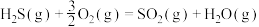







则用
 、
、 、
、 来表示
来表示 的表达式为
的表达式为(2)已知甲烷能催化还原
 ,得到氮气、二氧化碳和水蒸气,且知反应消耗1.6g甲烷时,放出热量86.7kJ,写出甲烷催化还原
,得到氮气、二氧化碳和水蒸气,且知反应消耗1.6g甲烷时,放出热量86.7kJ,写出甲烷催化还原 的热化学方程式
的热化学方程式(3)已知:


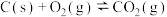
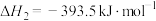
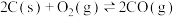

若某反应的平衡常数表达式为
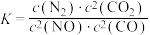 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式(4)利用如图所示装置测定中和热的实验步骤如下:

步骤一:用量筒量取50mL 0.50
 盐酸倒入内筒中,测出盐酸温度;
盐酸倒入内筒中,测出盐酸温度;步骤二:用另一量筒量取50mL 0.55
 NaOH溶液,并用同一温度计测出其温度;
NaOH溶液,并用同一温度计测出其温度;步骤三:将NaOH溶液倒入内筒中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
①假设盐酸和氢氧化钠溶液的密度都是1
 ,又知中和反应后生成溶液的比热容c=4.18
,又知中和反应后生成溶液的比热容c=4.18 。为了计算中和热,某学生实验记录数据如下:
。为了计算中和热,某学生实验记录数据如下:| 实验序号 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | ||
| 盐酸 | 氢氧化钠溶液 | 平均值 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 20.05 | 23.2 |
| 2 | 20.2 | 20.4 | 20.3 | 23.4 |
| 3 | 20.5 | 20.6 | 20.55 | 23.6 |
 的物质的量为0.025mol,依据该学生的实验数据计算,该实验测得的中和热ΔH=
的物质的量为0.025mol,依据该学生的实验数据计算,该实验测得的中和热ΔH= ] 。
] 。②该同学通过实验测出的中和热与理论值(
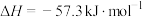 )有偏差,造成这一结果可能的原因是
)有偏差,造成这一结果可能的原因是A.实验装置保温、隔热效果差
B.用测量盐酸的温度计直接测定NaOH溶液的温度
C.将NaOH溶液一次性迅速倒入量热计内筒中,并立即盖上杯盖
③现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1L 1
 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】作为一种绿色消毒剂,H2O2在公共卫生事业中发挥了重要的作用。已知反应:H2O2(l)=H2O(1)+ O2(g) ΔH=-98kJ·mol-1 K=2.88×1020,纯H2O2可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下,H2O2剧烈分解:H2O2(l)=H2O(g)+
O2(g) ΔH=-98kJ·mol-1 K=2.88×1020,纯H2O2可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下,H2O2剧烈分解:H2O2(l)=H2O(g)+ O2(g),放出大量气体,驱动火箭升空。每消耗34gH2O2,理论上
O2(g),放出大量气体,驱动火箭升空。每消耗34gH2O2,理论上___________ (填“放出”或“吸收”)热量___________ 98kJ(填“大于”、“小于”或“等于”)。
 O2(g) ΔH=-98kJ·mol-1 K=2.88×1020,纯H2O2可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下,H2O2剧烈分解:H2O2(l)=H2O(g)+
O2(g) ΔH=-98kJ·mol-1 K=2.88×1020,纯H2O2可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下,H2O2剧烈分解:H2O2(l)=H2O(g)+ O2(g),放出大量气体,驱动火箭升空。每消耗34gH2O2,理论上
O2(g),放出大量气体,驱动火箭升空。每消耗34gH2O2,理论上
您最近一年使用:0次

 汽化时吸收的热量为
汽化时吸收的热量为 ,
, 的燃烧热为
的燃烧热为 ,请写出
,请写出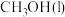 燃烧热的热化学方程式
燃烧热的热化学方程式

