向 FeI2、FeBr2 的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。已知:2Fe2++Br2=2Fe3++2Br-,2Fe3++2I-=2Fe2++I2.下列有关说法不正确的是
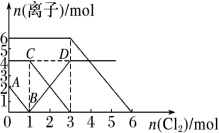

| A.线段 BD 表示 Fe3+物质的量的变化 |
| B.当通入 2 mol Cl2 时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
| C.原混合溶液中 FeI2 的物质的量为 2 mol |
| D.原溶液中,n(Fe2+)∶n(I-)∶n(Br-)=2∶3∶1 |
21-22高三上·山东菏泽·阶段练习 查看更多[2]
更新时间:2021-10-19 23:56:14
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列离子方程式正确的是
A.铁跟稀硫酸反应: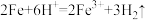 |
B.澄清石灰水跟盐酸反应: |
C.在硫酸铜溶液中加入氢氧化钡溶液: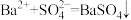 |
D.碳酸钙中加入盐酸: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某矿石的主要成分为 ,还含有
,还含有 、
、 、
、 、
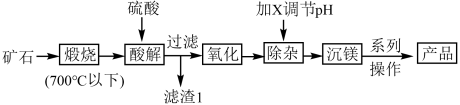
、 及少量其它杂质。某工厂采用该矿石为主要原料生产碱式碳酸镁,流程如下(已知:温度低于700℃时,
及少量其它杂质。某工厂采用该矿石为主要原料生产碱式碳酸镁,流程如下(已知:温度低于700℃时, 不会与
不会与 等反应)。下列有关说法不正确的是
等反应)。下列有关说法不正确的是
 ,还含有
,还含有 、
、 、
、 、
、 及少量其它杂质。某工厂采用该矿石为主要原料生产碱式碳酸镁,流程如下(已知:温度低于700℃时,
及少量其它杂质。某工厂采用该矿石为主要原料生产碱式碳酸镁,流程如下(已知:温度低于700℃时, 不会与
不会与 等反应)。下列有关说法不正确的是
等反应)。下列有关说法不正确的是
A.煅烧过程所发生的主要化学反应方程式为: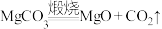 |
B.滤渣1的成分是 和 和 |
C.氧化步骤发生反应的离子方程式可以是: |
| D.加X调pH的X是氢氧化钠 |
您最近一年使用:0次
【推荐1】在MgCl2、KCl、K2SO4三种盐的混合溶液中,若K+、Cl-各为3 mol,Mg2+为1 mol,则 的物质的量为
的物质的量为
 的物质的量为
的物质的量为| A.0.5 mol | B.1 mol | C.1.5 mol | D.2 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某盐溶液滴入氯水无明显现象,再滴入硝酸酸化的硝酸钡,有白色沉淀生成,则某盐可能是
A. | B. | C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知如下反应:①Cl2+2Br﹣=2C1﹣+Br2②2Fe2++Br2=2Fe3++2Br﹣③2Fe3++2I﹣=2Fe2++I2,则有关离子的还原性由强到弱的顺序为
| A.I﹣>Fe2+>Br﹣>Cl﹣ | B.Fe2+>Br﹣>Cl﹣>I﹣ |
| C.Br﹣>Cl﹣>Fe2+>I﹣ | D.Fe2+>I﹣>Br﹣>Cl﹣ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】利用 KMnO4溶液和浓HCl在常温下反应即可制备Cl2,反应方程式2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。相关说法正确的是
| A.由该反应可知氧化性强弱为:KMnO4>Cl2 |
| B.反应中每生成5mol Cl2,则有16mol HCl被氧化 |
| C.该反应中MnCl2是氧化产物,Cl2是还原产物 |
| D.该反应生成11.2L的Cl2,转移电子一定为1mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】有3.92 g铁的氧化物,用足量的CO在高温下将其还原,把生成的全部CO2通入到足量的澄清的石灰水中得到7.0 g固体沉淀物,这种铁的氧化物为
| A.Fe3O4 | B.FeO | C.Fe2O3 | D.Fe5O7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】从高砷烟尘(主要成分为As2O3、As2O5和Pb5O8,As2O3、As2O5均为酸性氧化物)中回收制备砷酸钠晶体的工艺流程如下:
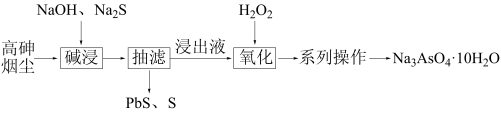
下列说法错误的是

下列说法错误的是
| A.“碱浸”时,Pb5O8发生的反应中氧化产物与还原产物的物质的量之比为1:1 |
| B.为加快“氧化”时的反应速率,可将溶液加热至沸腾 |
| C.浸出液“氧化”过程中,溶液的碱性逐渐减弱 |
| D.“系列操作”包括:蒸发浓缩、冷却结晶、过滤、洗涤、干燥等 |
您最近一年使用:0次


 溶液
溶液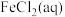

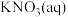



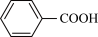 >CH3COOH
>CH3COOH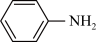
 催化
催化 和
和 制备双氧水和水的过程,如图所示。
制备双氧水和水的过程,如图所示。
 和
和 时转移电子数之比为1:1
时转移电子数之比为1:1


