回答下列问题
(1)一种燃料电池中发生的化学反应为:在酸性溶液中甲醇(CH3OH)与氧作用生成水和二氧化碳。该电池负极发生的反应是___________ 。
(2)要实现铁上镀银,则阳极为___________ ,电极反应式为___________ ,阴极为___________ ,电极反应式为___________ ,电镀液为___________ 。
(3)电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
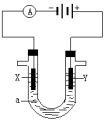
①若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,则电解池中X极上的电极反应为___________ ,在X极附近观察到的现象是 :___________ 。
②Y电极上的电极反应式是___________ ,检验该电极反应产物的方法是 :___________ 。
③如果用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是___________ ,电极反应式是___________ ,Y电极的材料是___________ ,电极反应式是___________ 。(假设粗铜中含铁、锌、银、金)
(4)铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:Pb+PbO2+4H++2
 2PbSO4+2H2O请回答下列问题(不考虑氢、氧的氧化还原):
2PbSO4+2H2O请回答下列问题(不考虑氢、氧的氧化还原):
放电时:正极的电极反应式是___________ ;电解液中H2SO4的浓度将变___________ ;当外电路通过1 mol电子时,理论上负极板的质量增加___________ g.充电时:阴极的电极反应式是___________ 。
(1)一种燃料电池中发生的化学反应为:在酸性溶液中甲醇(CH3OH)与氧作用生成水和二氧化碳。该电池负极发生的反应是
(2)要实现铁上镀银,则阳极为
(3)电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

①若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,则电解池中X极上的电极反应为
②Y电极上的电极反应式是
③如果用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是
(4)铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:Pb+PbO2+4H++2

 2PbSO4+2H2O请回答下列问题(不考虑氢、氧的氧化还原):
2PbSO4+2H2O请回答下列问题(不考虑氢、氧的氧化还原):放电时:正极的电极反应式是
21-22高二上·新疆哈密·阶段练习 查看更多[2]
更新时间:2021-10-28 21:57:29
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,其电极反应正极:______ ,负极:______ ,该电池总反应的离子方程式为______ .
(2)如果把“碱性电池”改为“酸性电池”,其电极反应正极:______ ,负极:______ ,该电池总反应的离子方程式为______ .
(2)如果把“碱性电池”改为“酸性电池”,其电极反应正极:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图所示,水槽中试管内有一枚铁钉,放置数天观察:

(1)铁钉在逐渐生锈。
(2)若试管内液面上升,发生___ 腐蚀,正极反应式:___ 。
(3)若试管内液面下降,正极反应式:___ 。

(1)铁钉在逐渐生锈。
(2)若试管内液面上升,发生
(3)若试管内液面下降,正极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ、火力发电厂释放出大量氮氧化合物(NOx)、SO2和CO2等气体会造成环境问题。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+ 4NO2(g)=4NO(g)+ CO2(g)+ 2H2O(g) △H1=-574 kJ/mol
CH4(g)+ 4NO(g)=2N2(g)+ CO2(g)+ 2H2O(g) △H2=-1160 kJ/mol
甲烷直接将NO2还原为N2的热化学方程式为__________________________ 。
(2)脱碳。将CO2转化为甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H3
CH3OH(g)+H2O(g)△H3

在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2进行反应。测得CO2和CH3OH(g)浓度随时间变化如图所示。回答:0~10 min内,氢气的平均反应速率为___ mol/(L·S);第10 min后,保持温度不变,向该密闭容器中再充入1 mol CO2(g)和1 mol H2O(g),则平衡_________ (填“正向”、“逆向”或“不”)移动。
Ⅱ、如下图所示C、D、E、F、X、Y都是惰性电极。将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色。

(1)若用甲醇、空气燃料电池作电源,电解质为KOH溶液,则A极的电极反应式为_________________________
(2)欲用(丙)装置给铜镀银,银应该是_____ 电极(填G或H)
(3)(丁)装置中Y极附近红褐色变_______ (填深或浅)
(4)通电一段时间后,C、D、E、F电极均有单质生成,其物质的量之比为_____________
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+ 4NO2(g)=4NO(g)+ CO2(g)+ 2H2O(g) △H1=-574 kJ/mol
CH4(g)+ 4NO(g)=2N2(g)+ CO2(g)+ 2H2O(g) △H2=-1160 kJ/mol
甲烷直接将NO2还原为N2的热化学方程式为
(2)脱碳。将CO2转化为甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H3
CH3OH(g)+H2O(g)△H3
在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2进行反应。测得CO2和CH3OH(g)浓度随时间变化如图所示。回答:0~10 min内,氢气的平均反应速率为
Ⅱ、如下图所示C、D、E、F、X、Y都是惰性电极。将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色。

(1)若用甲醇、空气燃料电池作电源,电解质为KOH溶液,则A极的电极反应式为
(2)欲用(丙)装置给铜镀银,银应该是
(3)(丁)装置中Y极附近红褐色变
(4)通电一段时间后,C、D、E、F电极均有单质生成,其物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】阳离子交换膜法电解饱和食盐水具有综合能耗低、环境污染小等优点。生产流程如图:

(1)电解饱和食盐水的化学方程式为_______ 。结合电极反应式说明生成溶液a的原理_______ 。
(2)电解结束后,能够脱去阳极液中游离氯的试剂或方法是_______ (填字母序号)。
a.Na2SO4 b.Na2SO3 c.热空气吹出 d.升高阳极区液面上方的气压
(3)二氧化氯(ClO2)为一种黄绿色气体。阳极产生副产物ClO2的电极反应式:_______ 。
(4)在酸性条件下加入NaClO溶液,可将食盐水中的I-转化为I2,再进一步除去。通过测定体系的吸光度,可以检测不同pH下I2的生成量随时间的变化,如下图所示。已知:吸光度越高表明该体系中c(I2)越大。

pH=4.0时,体系的吸光度很快达到最大值,之后快速下降。吸光度快速下降的可能原因:_____ 。

(1)电解饱和食盐水的化学方程式为
(2)电解结束后,能够脱去阳极液中游离氯的试剂或方法是
a.Na2SO4 b.Na2SO3 c.热空气吹出 d.升高阳极区液面上方的气压
(3)二氧化氯(ClO2)为一种黄绿色气体。阳极产生副产物ClO2的电极反应式:
(4)在酸性条件下加入NaClO溶液,可将食盐水中的I-转化为I2,再进一步除去。通过测定体系的吸光度,可以检测不同pH下I2的生成量随时间的变化,如下图所示。已知:吸光度越高表明该体系中c(I2)越大。

pH=4.0时,体系的吸光度很快达到最大值,之后快速下降。吸光度快速下降的可能原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某同学设计下图装置进行电解饱和食盐水自制“84”消毒液。回答下列问题
|
(1)电解饱和食盐水时,a连接电源的_________ 极(填“正”或“负”)。
(2)利用该装置自制消毒液的化学反应方程式是_________ 。
(3)①“84”消毒液不用时需要密封保存,否则会与空气中_________ 发生反应,生成不稳定的物质。
②该同学利用传感技术进行某溶液中次氯酸的稳定性实验。用强光照射盛有该溶液的广口瓶,过程中溶液的pH、Cl-的浓度、瓶中氧气的体积分数变化如下图:

该同学分析数据得出的结论是_________ (用化学方程式表示)。
(4)“84”消毒液不能与洁厕灵混用,也不能与消毒酒精混用,请从物质性质的角度解释“84”消毒液不能与消毒酒精混用的原因________ 。
|

(1)电解饱和食盐水时,a连接电源的
(2)利用该装置自制消毒液的化学反应方程式是
(3)①“84”消毒液不用时需要密封保存,否则会与空气中
②该同学利用传感技术进行某溶液中次氯酸的稳定性实验。用强光照射盛有该溶液的广口瓶,过程中溶液的pH、Cl-的浓度、瓶中氧气的体积分数变化如下图:

该同学分析数据得出的结论是
(4)“84”消毒液不能与洁厕灵混用,也不能与消毒酒精混用,请从物质性质的角度解释“84”消毒液不能与消毒酒精混用的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为______________________ 。
②Y电极上的电极反应式为_________________________ 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是________________ ,电极反应式为_________________________ 。
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为
②Y电极上的电极反应式为
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】冶炼铜矿石所获得的铜通常含有锌、铁、镍、银、金和铂等微量杂质,俗称粗铜。工业上通常通过电解法除去这些杂质制得精铜,以提高铜的使用价值,扩大铜的应用范围。(几种金属的相对原子质量是:Fe-56,Ni-59,Cu-64,Zn-65,Ag-108,Au-197。)
请完成下列问题:
(1)一般来说,电解精炼铜的初始电解质溶液里的阳离子是________ ,写出铜的电解精炼过程中的阴极反应式________________________________________________ 。
(2)如果转移0.020 mol e-,下列说法中一定正确的是________ 。
①阴极质量增加0.64 g ②阳极质量减少0.64 g
③电解质溶液的质量保持不变 ④电解质溶液的温度保持不变
请完成下列问题:
(1)一般来说,电解精炼铜的初始电解质溶液里的阳离子是
(2)如果转移0.020 mol e-,下列说法中一定正确的是
①阴极质量增加0.64 g ②阳极质量减少0.64 g
③电解质溶液的质量保持不变 ④电解质溶液的温度保持不变
您最近一年使用:0次
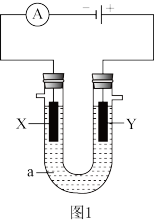
【推荐3】电解原理在化学领域应用广泛如图1表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请完成以下问题:
 +
+
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液:
①在X极附近观察到的现象是______________ ;_______ .
②电解一段时间后,该反应总离子方程式_______ ;
(2)若用该装置电解精炼铜,电解液a选用CuSO4溶液,则:X电极的材料是_______ ,电解一段时间后,CuSO4溶液浓度_______ (填“增大”、减小”或“不变”)。
(3)下列各情况,在其中Fe片腐蚀由快到慢的顺序是:____ ;

(4)如图, 水槽中试管内有一枚铁钉,放置数天观察:
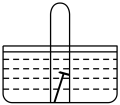
若试管内液面上升,则正极电极反应式为:______________________ 。
 +
+(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液:
①在X极附近观察到的现象是
②电解一段时间后,该反应总离子方程式
(2)若用该装置电解精炼铜,电解液a选用CuSO4溶液,则:X电极的材料是
(3)下列各情况,在其中Fe片腐蚀由快到慢的顺序是:

(4)如图, 水槽中试管内有一枚铁钉,放置数天观察:

若试管内液面上升,则正极电极反应式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】通常氢氧燃料电池有酸式和碱式两种,试回答下列问题:
(1)在酸式介质中,负极反应的物质为____ ,正极反应的物质为______ ,酸式电池的电极反应:
负极:__________________________________ ,正极:___________________________ 。
电解质溶液pH的变化_______________ (填“变大”,“变小”,“不变”)。
(2)在碱式介质中,碱式电池的电极反应:
负极:__________________________________ ,正极:___________________________ 。
电解质溶液pH的变化_______________ (填“变大”,“变小”,“不变”)。
(3)氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法不正确的是________ 。
A.太阳光催化分解水制氢气比电解水气氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀H2SO4、KOH为介质的氢氧燃料电池的负极电极反应式相同
D.以稀H2SO4、KOH为介质的氢氧燃料电池的总反应式相同
(4)纯电动车采用了高效耐用的一种新型可充电电池,该电池的总反应式为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。

①该电池放电时负极反应式为_________________ 。
②放电时每转移3 mol电子,正极有________ mol K2FeO4被还原。
(5)锰酸锂离子电池在混合动力车等大型蓄电池应用领域占据主导地位。
电池反应式为:Li1-xMnO4+Lix LiMnO4,下列有关说法不正确的是
LiMnO4,下列有关说法不正确的是________ 。
A.放电时电池的正极反应式为:Li1-xMnO4+xLi++xe-=LiMnO4
B.放电过程中,石墨没有得失电子
C.该电池也能在KOH溶液的环境中正常工作
D.充电时电池上标有“-”的电极应与外接电源的负极相连
(1)在酸式介质中,负极反应的物质为
负极:
电解质溶液pH的变化
(2)在碱式介质中,碱式电池的电极反应:
负极:
电解质溶液pH的变化
(3)氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法不正确的是
A.太阳光催化分解水制氢气比电解水气氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀H2SO4、KOH为介质的氢氧燃料电池的负极电极反应式相同
D.以稀H2SO4、KOH为介质的氢氧燃料电池的总反应式相同
(4)纯电动车采用了高效耐用的一种新型可充电电池,该电池的总反应式为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
①该电池放电时负极反应式为
②放电时每转移3 mol电子,正极有
(5)锰酸锂离子电池在混合动力车等大型蓄电池应用领域占据主导地位。
电池反应式为:Li1-xMnO4+Lix
 LiMnO4,下列有关说法不正确的是
LiMnO4,下列有关说法不正确的是A.放电时电池的正极反应式为:Li1-xMnO4+xLi++xe-=LiMnO4
B.放电过程中,石墨没有得失电子
C.该电池也能在KOH溶液的环境中正常工作
D.充电时电池上标有“-”的电极应与外接电源的负极相连
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】以氨气代替氢气研发氨燃料电池是当前科研的一个热点.
(1)氨燃料电池使用的电解质溶液是2mol•L﹣1的KOH溶液,电池反应为:4NH3+3O2=2N2+6H2O.该电池负极的电极反应式为______ ;每消耗1.7g NH3转移的电子数目为______ .
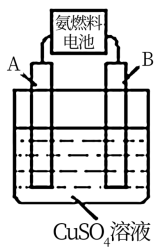
(2)用氨燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,则B电极上发生的电极反应式为______ ;此时向所得溶液中加入8gCuO固体后恰好可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为_______ L.
(3)纳米级氧化亚铜(Cu2O)是一种重要光电材料.现用铜棒和石墨做电极,饱和食盐水做电解质制备纳米级氧化亚铜(Cu2O),电解反应为2Cu+H2O Cu2O+H2↑铜棒上发生的电极反应式为
Cu2O+H2↑铜棒上发生的电极反应式为__ .
(1)氨燃料电池使用的电解质溶液是2mol•L﹣1的KOH溶液,电池反应为:4NH3+3O2=2N2+6H2O.该电池负极的电极反应式为
(2)用氨燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,则B电极上发生的电极反应式为

(3)纳米级氧化亚铜(Cu2O)是一种重要光电材料.现用铜棒和石墨做电极,饱和食盐水做电解质制备纳米级氧化亚铜(Cu2O),电解反应为2Cu+H2O
 Cu2O+H2↑铜棒上发生的电极反应式为
Cu2O+H2↑铜棒上发生的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据下列原电池的装置图,回答问题:
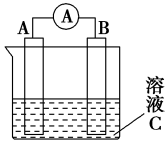
(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且做负极,则A电极上发生的电极反应式为___________ ;反应进行一段时间后溶液C的pH将___________ (填“升高”“降低”或“基本不变”)。
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如上图所示的原电池装置,则负极A极材料为___________ ,正极B极材料为___________ ,溶液C为___________ 。
(3)用CH4和O2组合形成的质子交换膜燃料电池的结构示意图如下:

①则d电极是___________ (填“正极”或“负极”),c电极的反应方程式为___________ 。
②若线路中转移2mol电子,则上述燃料电池,消耗的O2在标准状况下的体积为___________ L。
(4)熔融盐电池具有高的发电效率,因而受到重视。可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃料气,空气与CO2的混合气为正极助燃气,制得在650℃下工作的燃料电池,其负极电极反应式为2CO+2 -4e-=4CO2,则正极电极反应式为
-4e-=4CO2,则正极电极反应式为___________ 。

(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且做负极,则A电极上发生的电极反应式为
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如上图所示的原电池装置,则负极A极材料为
(3)用CH4和O2组合形成的质子交换膜燃料电池的结构示意图如下:

①则d电极是
②若线路中转移2mol电子,则上述燃料电池,消耗的O2在标准状况下的体积为
(4)熔融盐电池具有高的发电效率,因而受到重视。可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃料气,空气与CO2的混合气为正极助燃气,制得在650℃下工作的燃料电池,其负极电极反应式为2CO+2
 -4e-=4CO2,则正极电极反应式为
-4e-=4CO2,则正极电极反应式为
您最近一年使用:0次




