回答下列问题:
(1)现有以下物质:①NaOH溶液;②液氨;③BaCO3固体;④熔融NaHSO4;⑤Fe(OH)3胶体;⑥铜;⑦CO2;⑧CH3COOH;⑨蔗糖;
(i)以上物质中属于电解质的是_______ (填序号);以上纯净物中能导电的是_______ (填序号)。
(ii)写出制备物质⑤的方程式_______ 。
(iii)写出④的电离方程式_______ 。
(iV)上述物质中两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为_______
(V)在含40 g溶质的①溶液中缓缓通入标准状况下35.2 g CO2,则该过程的离子反应方程式为_______ 。
(2)已知一定条件可发生如下反应:NO+NH3=H2O+N2
①配平上述方程式,并用双线桥表示该反应中电子转移的方向和数目_______
②若有3.4 g氨气发生反应,则反应所得还原产物与氧化产物的质量差为_______
(1)现有以下物质:①NaOH溶液;②液氨;③BaCO3固体;④熔融NaHSO4;⑤Fe(OH)3胶体;⑥铜;⑦CO2;⑧CH3COOH;⑨蔗糖;
(i)以上物质中属于电解质的是
(ii)写出制备物质⑤的方程式
(iii)写出④的电离方程式
(iV)上述物质中两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为
(V)在含40 g溶质的①溶液中缓缓通入标准状况下35.2 g CO2,则该过程的离子反应方程式为
(2)已知一定条件可发生如下反应:NO+NH3=H2O+N2
①配平上述方程式,并用双线桥表示该反应中电子转移的方向和数目
②若有3.4 g氨气发生反应,则反应所得还原产物与氧化产物的质量差为
更新时间:2021-10-29 14:22:09
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题。
(1)如图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了 、
、 、
、 、
、 、
、 ,图中相连的物质均可归为一类,相交部分A、B、C、D为相应的分类标准代号。
,图中相连的物质均可归为一类,相交部分A、B、C、D为相应的分类标准代号。

①相连的两种物质都是电解质的是___________ (填分类标准代号,下同),都是氧化物的是___________ 。
②图中相连的两种物质能够相互反应的是___________ ,所属的基本反应类型是___________ 。
③上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,则该反应的离子方程式为___________ 。
(2)分类方法应用广泛,属于同一类的物质具有相似性,在生活和学习中,使用分类的方法处理问题可以做到举一反三,还可以做到由此及彼的效果。
① 、
、 、
、 、
、 都属于酸性氧化物,由
都属于酸性氧化物,由 ,可得出
,可得出 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
② 、
、 、
、 都属于弱酸的酸式盐,由
都属于弱酸的酸式盐,由 、
、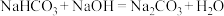 ,完成
,完成 分别与
分别与 、
、 反应的离子方程式
反应的离子方程式___________ 、___________ 。
(1)如图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了
 、
、 、
、 、
、 、
、 ,图中相连的物质均可归为一类,相交部分A、B、C、D为相应的分类标准代号。
,图中相连的物质均可归为一类,相交部分A、B、C、D为相应的分类标准代号。
①相连的两种物质都是电解质的是
②图中相连的两种物质能够相互反应的是
③上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,则该反应的离子方程式为
(2)分类方法应用广泛,属于同一类的物质具有相似性,在生活和学习中,使用分类的方法处理问题可以做到举一反三,还可以做到由此及彼的效果。
①
 、
、 、
、 、
、 都属于酸性氧化物,由
都属于酸性氧化物,由 ,可得出
,可得出 与
与 反应的化学方程式为
反应的化学方程式为②
 、
、 、
、 都属于弱酸的酸式盐,由
都属于弱酸的酸式盐,由 、
、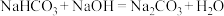 ,完成
,完成 分别与
分别与 、
、 反应的离子方程式
反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有以下物质:①NaCl固体;②液态CO2;③液态氯化氢;④汞;⑤固体BaSO4;⑥蔗糖;⑦酒精;⑧熔融的Na2CO3,请回答下列问题:
(1)以上物质中能导电的是________ ;
(2)以上物质属于电解质的是________ ;
(3)以上物质属于非电解质的是_______ ;
(4)以上物质溶于水后形成的溶液能导电的是______ ;
(5)属于盐的有________ ;
(6)写出⑧溶于水中的电离方程式_____ ;
(7)分离胶体和溶液常用的方法叫__________ ;
(8)等质量的O2和O3所含原子个数比为______ ;
(9)设NA为阿伏加 德罗常数的数值,若ag某气体中含有的分子数为b,则c g该气体在标准状况下的体积是___________ 。(用含有NA的式子表示)
(1)以上物质中能导电的是
(2)以上物质属于电解质的是
(3)以上物质属于非电解质的是
(4)以上物质溶于水后形成的溶液能导电的是
(5)属于盐的有
(6)写出⑧溶于水中的电离方程式
(7)分离胶体和溶液常用的方法叫
(8)等质量的O2和O3所含原子个数比为
(9)设NA为阿伏加 德罗常数的数值,若ag某气体中含有的分子数为b,则c g该气体在标准状况下的体积是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ现有下列物质:①CO2②铜③硫酸溶液④Na2CO3•10H2O晶体⑤NaHSO4固体 ⑥Ba(OH)2固⑦Al2(SO4)3固体⑧氨水⑨稀硝酸。
(1)上述物质中属于电解质的有____ (填数字序号);能导电的是___ (填数字序号)。
(2)写出NaHSO4溶液和NaHCO3溶液反应的离子方程式:_________ 。
Ⅱ有A、B、C、D 四种化合物,分别由K+ 、Ba2+、SO42、CO32、OH中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(1)推断C的化学式:C________ ;
(2)B与盐酸反应的离子方程式_________ 。
(1)上述物质中属于电解质的有
(2)写出NaHSO4溶液和NaHCO3溶液反应的离子方程式:
Ⅱ有A、B、C、D 四种化合物,分别由K+ 、Ba2+、SO42、CO32、OH中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(1)推断C的化学式:C
(2)B与盐酸反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求写出方程式。
其中1、2写离子方程式;3、4写水溶液中的电离方程式;5、6写一个对应的化学方程式
(1)碳酸钙和盐酸_______________________________
(2)氢氧化钡溶液和稀硫酸_______________________________
(3)NaHSO4_______________________________
(4)KClO3_______________________________
(5)H + + OH — = H2O_______________________________
(6)CO32 —+2H + =CO2↑+H2O_______________________________
其中1、2写离子方程式;3、4写水溶液中的电离方程式;5、6写一个对应的化学方程式
(1)碳酸钙和盐酸
(2)氢氧化钡溶液和稀硫酸
(3)NaHSO4
(4)KClO3
(5)H + + OH — = H2O
(6)CO32 —+2H + =CO2↑+H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是我们常见的几种消毒剂:①“84”消毒液;② (二元弱酸);③
(二元弱酸);③ ;④
;④ ;⑤碘酒;⑥75%酒精;⑦高铁酸钠(Na2FeO4)。回答下列问题:
;⑤碘酒;⑥75%酒精;⑦高铁酸钠(Na2FeO4)。回答下列问题:
(1)上述杀菌消毒剂属于非电解质的是___________ (填序号)。
(2)请写出 的电离方程式:
的电离方程式:___________ 。
(3)各类杀菌消毒剂使用时,必须严格按照使用说明。
巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是 与
与 反应产生
反应产生 促进藻类快速生长。当有
促进藻类快速生长。当有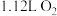 生成时(标准状况下),反应中转移电子为
生成时(标准状况下),反应中转移电子为___________ mol。
(4)工业上可在 溶液中,用
溶液中,用 氧化
氧化 的方法制备
的方法制备 。制备反应的离子方程式为
。制备反应的离子方程式为___________ 。
 (二元弱酸);③
(二元弱酸);③ ;④
;④ ;⑤碘酒;⑥75%酒精;⑦高铁酸钠(Na2FeO4)。回答下列问题:
;⑤碘酒;⑥75%酒精;⑦高铁酸钠(Na2FeO4)。回答下列问题:(1)上述杀菌消毒剂属于非电解质的是
(2)请写出
 的电离方程式:
的电离方程式:(3)各类杀菌消毒剂使用时,必须严格按照使用说明。
巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是
 与
与 反应产生
反应产生 促进藻类快速生长。当有
促进藻类快速生长。当有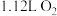 生成时(标准状况下),反应中转移电子为
生成时(标准状况下),反应中转移电子为(4)工业上可在
 溶液中,用
溶液中,用 氧化
氧化 的方法制备
的方法制备 。制备反应的离子方程式为
。制备反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据所学知识,回答下列问题:
(1)下表是对一些物质进行分类
其中 Na2O2中O____ 价,它____ 碱性氧化物(填“是”或“不是”)
(2)过氧化钠水溶液中加入几滴紫色石蕊试液,现象:___________ ,写出过氧化钠与水反应的离子方程式:___________ 。
(3)实验室氯气不能排放在空气中,可用氢氧化钠溶液处理,其原因是:__________ 。氯气通入到⑥的溶液中的离子方程式:___________ 。
(4)如何要检验某溶液中是否含有钾元素,可以用操作方法:___________ 。
(5)实验室通过反应KMnO4+HCl(浓)—MnCl2+KCl+Cl2↑+H2O(未配平)制备氯气,反应中氯化氢表现出的性质是_____ 。(填写字母)
a.还原性 b.酸性 c.氧化性
请配平该反应,并用双线桥标电子转移的方向和数目:___________ 。
(1)下表是对一些物质进行分类
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 单质 |
| 化学式 | ①H2SO4 ②HCl | ③NaOH ④Ba(OH)2 | ⑤NaHCO3 ⑥NaI | ⑦CO2 ⑧Na2O2 | ⑨O2 ⑩Cl2 |
(2)过氧化钠水溶液中加入几滴紫色石蕊试液,现象:
(3)实验室氯气不能排放在空气中,可用氢氧化钠溶液处理,其原因是:
(4)如何要检验某溶液中是否含有钾元素,可以用操作方法:
(5)实验室通过反应KMnO4+HCl(浓)—MnCl2+KCl+Cl2↑+H2O(未配平)制备氯气,反应中氯化氢表现出的性质是
a.还原性 b.酸性 c.氧化性
请配平该反应,并用双线桥标电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】实验室中用氯酸钾、铁、盐酸、二氧化锰和碳酸钙制取氢气、氧气和二氧化碳。
(1)写出实验室制取这三种气体的化学方程式,注明反应的基本类型。
①制氢气:_____________ ,反应类型:____________ ;
②制氧气:____________ ,反应类型:____________ ;
③制二氧化碳:_______________ ,反应类型____________ 。
(2)实验室中可用二氧化锰和浓盐酸共热制取氯气,已知反应中还生成二氯化锰和水,则该反应________ (填“是”或“不是”)氧化还原反应,判断的依据是______________ ,若是氧化还原反应,则请标出该反应电子转移的方向(从还原剂中变价元素出发指向氧化剂中变价元素)和数目;若不是氧化还原反应,则本空不用作答:_______________ 。
(3)在实验室制取氧气和氯气的反应中,都要用到二氧化锰。在制取氧气的反应中,二氧化锰作________ 剂,在制取氯气的反应中,二氧化锰作________ 剂。在实验室制取氢气和氯气的反应中,都用到盐酸,在制取氢气的反应中,HCl作________ 剂,在制取氯气的反应中,HCl作________ 剂。
(1)写出实验室制取这三种气体的化学方程式,注明反应的基本类型。
①制氢气:
②制氧气:
③制二氧化碳:
(2)实验室中可用二氧化锰和浓盐酸共热制取氯气,已知反应中还生成二氯化锰和水,则该反应
(3)在实验室制取氧气和氯气的反应中,都要用到二氧化锰。在制取氧气的反应中,二氧化锰作
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)请写出以下物质的电离方程式:
H2SO4_______ ;NaOH_____ ;NaHSO4_______ ;Al2(SO4)3_____ 。
(2)用双线桥法表示以下氧化还原反应中电子转移方向和数目_____ 。
2Na+2H2O =2NaOH+H2↑
(3)用单线桥法表示以下氧化还原反应中电子转移方向和数目_____ 。
Fe+2HCl=FeCl2+H2↑
(4)钠在空气中变质的最终产物是_______ 。(填化学式)
(1)请写出以下物质的电离方程式:
H2SO4
(2)用双线桥法表示以下氧化还原反应中电子转移方向和数目
2Na+2H2O =2NaOH+H2↑
(3)用单线桥法表示以下氧化还原反应中电子转移方向和数目
Fe+2HCl=FeCl2+H2↑
(4)钠在空气中变质的最终产物是
您最近一年使用:0次
【推荐1】化学方法在文物保护中有重要作用,某博物馆修复出土铁器的部分过程如下:
(1)检测锈蚀产物主要成分的化学式为Fe3O4、Fe2O3•H2O、FeO(OH)、FeOCl,由产物可推测,铁器可能与__ (填2种反应物化学式)发生反应而被腐蚀。
(2)分析认为,铁经过了如下腐蚀循环:
Ⅰ.Fe转化为Fe2+;
Ⅱ.Fe2+在自然环境中形成FeO(OH);
Ⅲ.FeO(OH)和Fe2+反应形成致密的Fe3O4保护层;
Ⅳ.Fe3O4保护层被氧化为FeO(OH),如此往复腐蚀。
①FeOCl中铁的化合价为__ ;上述反应中是氧化还原反应的为__ (填序号)。
②FeO(OH)和Fe2+反应的离子方程式为__ 。
③Ⅳ反应为Fe3O4+O2+H2O→FeO(OH),还原剂为__ ,每反应1mol还原剂,转移电子__ mol。
(1)检测锈蚀产物主要成分的化学式为Fe3O4、Fe2O3•H2O、FeO(OH)、FeOCl,由产物可推测,铁器可能与
(2)分析认为,铁经过了如下腐蚀循环:
Ⅰ.Fe转化为Fe2+;
Ⅱ.Fe2+在自然环境中形成FeO(OH);
Ⅲ.FeO(OH)和Fe2+反应形成致密的Fe3O4保护层;
Ⅳ.Fe3O4保护层被氧化为FeO(OH),如此往复腐蚀。
①FeOCl中铁的化合价为
②FeO(OH)和Fe2+反应的离子方程式为
③Ⅳ反应为Fe3O4+O2+H2O→FeO(OH),还原剂为
您最近一年使用:0次
【推荐2】生活饮用水水质的标准主要有:色度、浑浊度、pH、 细菌总数、嗅和味等等。目前城市自来水处理过程中所使用的主要药剂仍是Cl2 (消毒剂)和Al2(SO4)3 (沉降剂),但由于种种原因,用这两种物质处理水质,总有缺陷。因此,有资料报道: Na2FeO4是一种强氧化剂,可作为一种新型净水剂, 在反应中被还原为Fe3+离子,使用该物质可代替Cl2和Al2(SO4)3 。
(1)配平工业上制备铁酸钠的化学方程式:
Fe2O3+____ NaNO3+____ NaOH 
____ Na2FeO4+____ NaNO2+____ H2O
(2)当反应物中含有1.4mol钠离子,上述反应恰好完全进行时,电子转移总数为___________ NA。
(3)某厂制备铁酸钠后的废液中含NaNO2溶液,直接排放会造成污染,下列试剂中①NaCl
②NH4Cl③KMnO4④浓H2SO4,能使NaNO2转化为N2 (不引起二次污染的)是_____________ (选填编号),反应离子方程式_________________________________
(1)配平工业上制备铁酸钠的化学方程式:
Fe2O3+

(2)当反应物中含有1.4mol钠离子,上述反应恰好完全进行时,电子转移总数为
(3)某厂制备铁酸钠后的废液中含NaNO2溶液,直接排放会造成污染,下列试剂中①NaCl
②NH4Cl③KMnO4④浓H2SO4,能使NaNO2转化为N2 (不引起二次污染的)是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氯及其化合物有重要用途,以下是氯元素的“价类二维图”的部分信息。请回答下列问题:
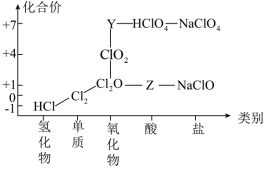
(1)根据图中信息写出Z的化学式_______ 。
(2)已知高氯酸(HClO4)是强酸,写出高氯酸在水中的电离方程式________ 。
(3)氯气既有氧化性又有还原性,结合上图说明理由________ 。
(4)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为2HCl + NaClO = NaCl + Cl2↑ + H2O,在该反应中,氧化剂是_______ ,当生成标准状况下的22.4 L Cl2时,NaClO转移的电子数为_______ 。
(5)某游泳池常用NaClO来抑制藻类生长,工作人员一次错用H2O2消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了O2和NaCl,写出相应的化学方程式_______ 。

(1)根据图中信息写出Z的化学式
(2)已知高氯酸(HClO4)是强酸,写出高氯酸在水中的电离方程式
(3)氯气既有氧化性又有还原性,结合上图说明理由
(4)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为2HCl + NaClO = NaCl + Cl2↑ + H2O,在该反应中,氧化剂是
(5)某游泳池常用NaClO来抑制藻类生长,工作人员一次错用H2O2消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了O2和NaCl,写出相应的化学方程式
您最近一年使用:0次



