在实验室制取乙烯时,其反应为CH3CH2OH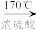 CH2=CH2↑+H2O。该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如下实验装置以验证上述反应生成的混合气体中含乙烯、SO2和水蒸气。
CH2=CH2↑+H2O。该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如下实验装置以验证上述反应生成的混合气体中含乙烯、SO2和水蒸气。
(1)仪器a的名称为___ 。
(2)请根据实验的要求完成下列填空:
①B中可观察到的现象为___ 。
②D中的试剂为___ 。
③E中的试剂为__ ,其作用为___ 。
④F中的试剂为___ ,可能的实验现象为___ 。
(3)简述装置B置于装置A、C之间的理由:___ 。
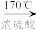 CH2=CH2↑+H2O。该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如下实验装置以验证上述反应生成的混合气体中含乙烯、SO2和水蒸气。
CH2=CH2↑+H2O。该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如下实验装置以验证上述反应生成的混合气体中含乙烯、SO2和水蒸气。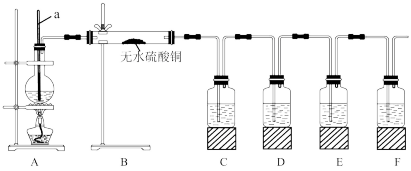
(1)仪器a的名称为
(2)请根据实验的要求完成下列填空:
①B中可观察到的现象为
②D中的试剂为
③E中的试剂为
④F中的试剂为
(3)简述装置B置于装置A、C之间的理由:
更新时间:2021-10-29 11:56:19
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下列物质间在一定条件下可实现如图所示的一系列变化,实验室可用固体 X 和黑色固体 Y 共热来制备气体 A,固体 B 为混合物,白色沉淀 D 难溶于稀硝酸,E 的焰色反应显紫色(透过蓝色钴玻璃),H 加热生成固体 Y 和水。请填写下列空白:
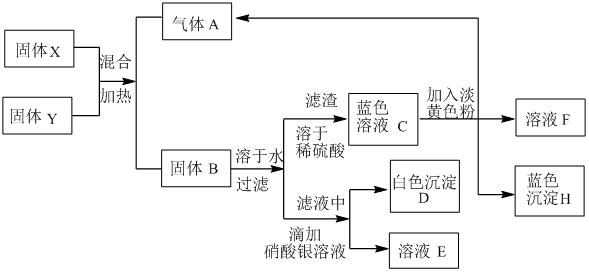
(1)X 和 Y 依次是(填化学式,下同)___ 。
(2)E 是___ 。
(3)X、Y 共热的化学方程式___ ;
(4)C 与淡黄色粉末 G 反应生成 A、F、H 的离子方程式________ 。

(1)X 和 Y 依次是(填化学式,下同)
(2)E 是
(3)X、Y 共热的化学方程式
(4)C 与淡黄色粉末 G 反应生成 A、F、H 的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某绿色溶液A含有H+、Na+、Mg2+、Fe2+、Cu2+、 、Cl-、
、Cl-、 、
、 离子中的种若干种。取该溶液进行如下实验:
离子中的种若干种。取该溶液进行如下实验:
①向溶液中滴加Ba(OH)2溶液,过滤,得到不溶于酸的白色沉淀和绿色滤液B;
②取滤液B,先用硝酸酸化,再滴加AgNO3溶液,有白色沉淀生成。
已知:①CuCl2·2H2O是绿色固体,溶于水浓溶液呈绿色,稀溶液呈蓝色;
②Ag2SO4微溶于水,可溶于硝酸;
③Fe2+(aq)呈浅绿色;Fe(OH)2是白色沉淀,在空气中与氧气和水反应迅速变成灰绿色,最终变成红褐色的Fe(OH)3沉淀。
根据上述信息,回答下列问题:
(1)导致溶液A呈现绿色的原因是_______ ;
(2)通过实验①可以得出_______ 离子存在、_______ 离子不存在的结论;
(3)通过实验②可以得出的结论是_______ ;
(4)结合实验①和②和题干信息,仍不能判断A溶液中是否存在的离子是_______ ;
(5)在绿色滤液B中加入_______ 溶液,依据不同的现象,可以推断出导致溶液呈现绿色的离子的具体存在情况。写出Fe(OH)2在空气中与氧气和水反应生成红褐色的Fe(OH)3的化学方程式_______ 。
 、Cl-、
、Cl-、 、
、 离子中的种若干种。取该溶液进行如下实验:
离子中的种若干种。取该溶液进行如下实验:①向溶液中滴加Ba(OH)2溶液,过滤,得到不溶于酸的白色沉淀和绿色滤液B;
②取滤液B,先用硝酸酸化,再滴加AgNO3溶液,有白色沉淀生成。
已知:①CuCl2·2H2O是绿色固体,溶于水浓溶液呈绿色,稀溶液呈蓝色;
②Ag2SO4微溶于水,可溶于硝酸;
③Fe2+(aq)呈浅绿色;Fe(OH)2是白色沉淀,在空气中与氧气和水反应迅速变成灰绿色,最终变成红褐色的Fe(OH)3沉淀。
根据上述信息,回答下列问题:
(1)导致溶液A呈现绿色的原因是
(2)通过实验①可以得出
(3)通过实验②可以得出的结论是
(4)结合实验①和②和题干信息,仍不能判断A溶液中是否存在的离子是
(5)在绿色滤液B中加入
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某工厂的工业废水中含有大量的Fe2+、SO42-和较多的Cu2+及少量的Na+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,在方框和 括号内填写物质名称(或主要成分的化学式)或操作方法,完成回收硫酸亚铁和铜的简单实 验方案。

(1)操作②的名称为__________ ,所需要的玻璃仪器为__________ 、玻璃棒、烧杯。
(2)试剂⑤的化学式为__________ ,发生化学反应的离子方程式为__________ 。
(3)为验证溶液⑧中含有SO42-:取少量的溶液⑧于试管中,先加入____ 再加入__________ ,若观察到有白色沉淀,则说明溶液⑧中含有SO42-。写出上述反应的离子方程式______________________________ .

(1)操作②的名称为
(2)试剂⑤的化学式为
(3)为验证溶液⑧中含有SO42-:取少量的溶液⑧于试管中,先加入
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐1】煤和石油是化工原料的重要来源,从石油中获得A,是工业上生产A的主要途径,A可用作植物生长调节剂。从煤焦油中可获得烃B,B中碳、氢两种元素的质量比为12:1,且B是常见的有机溶剂。工业上可以通过以下途径获得A、B。
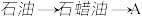
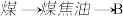
(1)由煤得到煤焦油的方法称为________ ;由石蜡油获得A的方法称为________ 。
(2)A和B中,能使酸性高锰酸钾溶液褪色的是________ (填“A”或“B”)。
(3)写出B发生取代反应的化学方程式:________________________ (写一个即可,并注明反应条件)。
(4)用B和丙烯可以生产两种重要的化工原料:苯酚(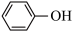 )和丙酮(
)和丙酮(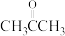 ),生产流程如下:
),生产流程如下:
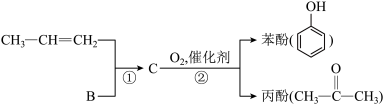
已知反应①是加成反应,C的一氯代物有5种,则C的结构简式为_____________ ;反应②的化学方程式为_________________________________ 。
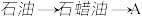
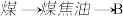
(1)由煤得到煤焦油的方法称为
(2)A和B中,能使酸性高锰酸钾溶液褪色的是
(3)写出B发生取代反应的化学方程式:
(4)用B和丙烯可以生产两种重要的化工原料:苯酚(
 )和丙酮(
)和丙酮(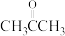 ),生产流程如下:
),生产流程如下:
已知反应①是加成反应,C的一氯代物有5种,则C的结构简式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】将浸透了石蜡油的石棉放在试管中进行下列实验,请回答下列问题。
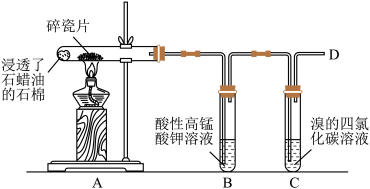
(1)反应一段时间后,B试管中的现象是___ ,由此说明石蜡油分解产生的气体具有___ 性(填“氧化”或“还原”)。
(2)若石蜡油分解产生乙烯,则C中发生反应的化学方程式是___ 。
(3)在D处点燃气体,观察到的现象是___ 。
(4)除去甲烷中混有的乙烯应采用的方法是___ 。

(1)反应一段时间后,B试管中的现象是
(2)若石蜡油分解产生乙烯,则C中发生反应的化学方程式是
(3)在D处点燃气体,观察到的现象是
(4)除去甲烷中混有的乙烯应采用的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
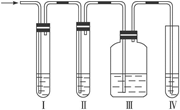
【推荐3】(1)在实验室里制取乙烯常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,有人设计如图所示实验以确认上述混和气体中有C2H4和SO2。(乙烯的制取装置略)
①Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛入的试剂是:Ⅰ______ 、Ⅱ______ 、Ⅲ______ 、Ⅳ______ 。(将下列有关试剂的序号填入空格内)
A. 品红溶液 B. NaOH溶液 C. 浓H2SO4 D. 酸性KMnO4溶液
②能说明SO2气体存在的现象是____________________ 。
③使用装置Ⅲ的目的是____________________________ 。
④确定含有乙烯的现象是_________________________ 。
(2)取一支试管,向其中加入10mL溴水,再加入5mL正己烷(分子式为C6H14,结构简式为CH3CH2CH2CH2CH2CH3)。将此试管中的混合液在光照下振荡后静置,液体分为几乎都是无色的上、下两层。用玻璃棒蘸取浓氨水伸入试管内液面上方,有白烟出现。
① 请写出生成白烟的化学反应方程式:_____________________________ 。
② 该实验证明了这是一个__________ 。
A.取代反应 B.加成反应 C.氧化反应 D.水解反应
①Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛入的试剂是:Ⅰ
A. 品红溶液 B. NaOH溶液 C. 浓H2SO4 D. 酸性KMnO4溶液
②能说明SO2气体存在的现象是
③使用装置Ⅲ的目的是
④确定含有乙烯的现象是
(2)取一支试管,向其中加入10mL溴水,再加入5mL正己烷(分子式为C6H14,结构简式为CH3CH2CH2CH2CH2CH3)。将此试管中的混合液在光照下振荡后静置,液体分为几乎都是无色的上、下两层。用玻璃棒蘸取浓氨水伸入试管内液面上方,有白烟出现。
① 请写出生成白烟的化学反应方程式:
② 该实验证明了这是一个
A.取代反应 B.加成反应 C.氧化反应 D.水解反应
您最近一年使用:0次
【推荐1】如图是石蜡油在炽热碎瓷片的作用下产生乙烯,并检验乙烯性质的实验。

回答下列问题:
(1)从装置A中出来的气体中含有烷烃和________ 。
(2)B中酸性高锰酸钾溶液______ ,这是因为生成的气体被_____ (填“氧化”或“还原”),反应类型为______ 。
(3)C中溴的四氯化碳溶液______ ,发生反应的化学方程式:____ ,反应类型为______ 。
(4)在D处点燃之前必须进行的操作是_______ ,燃烧时反应的化学方程式为______ 。
(5)收集A中放出的气体,让其与水发生反应,生成的物质可以被重铬酸钾氧化成______ ,该反应在实际生活中被交警用来检测________ 。

回答下列问题:
(1)从装置A中出来的气体中含有烷烃和
(2)B中酸性高锰酸钾溶液
(3)C中溴的四氯化碳溶液
(4)在D处点燃之前必须进行的操作是
(5)收集A中放出的气体,让其与水发生反应,生成的物质可以被重铬酸钾氧化成
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学采用下列实验装置模拟工业制乙烯,并探究乙烯的主要化学性质。(已知烃类不与碱反应)回答下列问题:
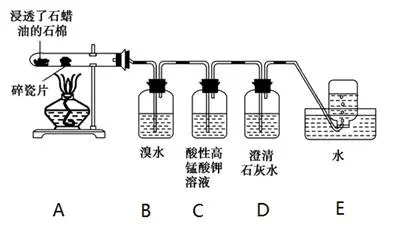
(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷烃发生反应:C16H34 C8H18+甲,甲
C8H18+甲,甲 4乙,则甲的分子式为
4乙,则甲的分子式为___________ ,乙的结构简式为___________ 。
(2) 装置中反应的化学方程式:
装置中反应的化学方程式:___________ ,其反应类型是___________ 。
(3) 装置中可观察到的现象是
装置中可观察到的现象是___________ ,反应类型是___________ 。
(4)通过上述实验探究,检验甲烷和乙烯的方法是___________ (填序号,下同);除去甲烷中乙烯的方法是___________ 。
A.气体通入水中 B.气体通过盛溴水的洗气瓶
C.气体通过盛酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液

(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷烃发生反应:C16H34
 C8H18+甲,甲
C8H18+甲,甲 4乙,则甲的分子式为
4乙,则甲的分子式为(2)
 装置中反应的化学方程式:
装置中反应的化学方程式:(3)
 装置中可观察到的现象是
装置中可观察到的现象是(4)通过上述实验探究,检验甲烷和乙烯的方法是
A.气体通入水中 B.气体通过盛溴水的洗气瓶
C.气体通过盛酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】为探究乙烯与溴的加成反应,甲同学设计并进行如下实验:先取一定量的工业用乙烯气体(在储气瓶中),使气体通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应;乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊物质,推测在工业上制得的乙烯中还可能含有少量还原性气体杂质,由此他提出必须先除去杂质,再让乙烯与溴水反应。请回答下列问题:
(1)甲同学设计的实验________ (填“能”或“不能”)验证乙烯与溴发生了加成反应,其理由是________ (填序号)。
①使溴水褪色的反应不一定是加成反应
②使溴水褪色的反应就是加成反应
③使溴水褪色的物质不一定是乙烯
④使溴水褪色的物质就是乙烯
(2)乙同学推测此乙烯中一定含有的一种杂质气体是________ ,它与溴水反应的化学方程式是________________ 。在实验前必须全部除去,除去该杂质的试剂可用________ 。
(3)为验证乙烯与溴发生的反应是加成反应而不是取代反应,丙同学提出可用 试纸来测试反应后溶液的酸性,理由是
试纸来测试反应后溶液的酸性,理由是_____________________________________________________________________________ 。
(1)甲同学设计的实验
①使溴水褪色的反应不一定是加成反应
②使溴水褪色的反应就是加成反应
③使溴水褪色的物质不一定是乙烯
④使溴水褪色的物质就是乙烯
(2)乙同学推测此乙烯中一定含有的一种杂质气体是
(3)为验证乙烯与溴发生的反应是加成反应而不是取代反应,丙同学提出可用
 试纸来测试反应后溶液的酸性,理由是
试纸来测试反应后溶液的酸性,理由是
您最近一年使用:0次
【推荐1】二氧化硫通入氯化钡溶液中理论上不产生沉淀,而实际受到空气和溶液中氧气的影响很快便能观察到沉淀现象。为了避免产生沉淀,某化学小组设计了如下实验装置,实验操作步骤如下:
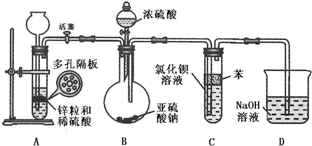
①气密性检查完好后,在装置A中的多孔隔板上放上锌粒,通过_______注入稀硫酸、打开活塞,将产生的氢气导入到后续装置。
②________后,关闭活塞,将装置D的导管插入烧杯中。
③通过装置B的________滴加浓硫酸,产生的气体进入到BaCl2溶液中,溶液保持澄清。
④打开活塞,将产生的氢气导入后续装置一段时间。
⑤将盛有BaCl2溶液的试管从装置中取出,拔去橡皮塞用胶头滴管伸入到苯层下方滴加双氧水,随即出现白色浑浊,滴加稀盐酸并振荡,白色浑浊不消失。
⑥拆卸装置,清洗仪器,处理剩余药品。
请回答下列问题:
(1)实验步骤①和③的空白处使用的仪器分别为__________ 、__________
(2)装置C中苯的作用是__________ 。
(3)实验步骤②的操作为__________ 。
(4)实验步骤④的目的是__________ 。
(5)写出实验步骤⑤试管中发生反应的化学方程式:__________ 、____________ 。
(6)为了避免产生沉淀,你认为还应采取哪些措施?请举一例:__________ 。

①气密性检查完好后,在装置A中的多孔隔板上放上锌粒,通过_______注入稀硫酸、打开活塞,将产生的氢气导入到后续装置。
②________后,关闭活塞,将装置D的导管插入烧杯中。
③通过装置B的________滴加浓硫酸,产生的气体进入到BaCl2溶液中,溶液保持澄清。
④打开活塞,将产生的氢气导入后续装置一段时间。
⑤将盛有BaCl2溶液的试管从装置中取出,拔去橡皮塞用胶头滴管伸入到苯层下方滴加双氧水,随即出现白色浑浊,滴加稀盐酸并振荡,白色浑浊不消失。
⑥拆卸装置,清洗仪器,处理剩余药品。
请回答下列问题:
(1)实验步骤①和③的空白处使用的仪器分别为
(2)装置C中苯的作用是
(3)实验步骤②的操作为
(4)实验步骤④的目的是
(5)写出实验步骤⑤试管中发生反应的化学方程式:
(6)为了避免产生沉淀,你认为还应采取哪些措施?请举一例:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验题:
(1)下列说法正确的是_________
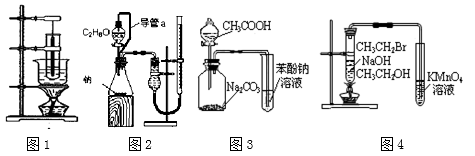
A.图1为实验室制备硝基苯的装置
B.图2可以用于测定乙醇分子结构
C.图3装置可以达到验证酸性:CH3COOH > H2CO3 > C6H5OH的目的
D.图4装置可以达到验证溴乙烷发生消去反应生成烯烃的目的
(2)用氧化还原滴定法测定制备得到的TiO2试样中的TiO2的质量分数:在一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作为指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
①TiCl4水解生成TiO2·xH2O的化学方程式为____________________ 。
②滴定终点的现象是___________________ 。
③滴定分析时,称取TiO2试样0.2 g,消耗0.1 mol·L—1NH4Fe(SO4)2标准溶液20mL,则TiO2的质量分数为________________ 。
④若在滴定终点读取滴定管刻度时,俯视标准溶液的液面,使其测定结果__________ (填“偏大”“偏小”或“无影响”)。
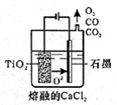
⑤工业上由H4TiO4可制得钛白粉TiO2。TiO2直接电解还原法生产钛是一种较先进的方法,电解质为熔融的CaCl2,原理如图所示,阴极的电极反应为_________ 。
(3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl-,利用Ag+与Cr 生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5 mol·L-1)时,溶液中c(Ag+)为
生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5 mol·L-1)时,溶液中c(Ag+)为______ mol·L-1,此时溶液中c(Cr )等于
)等于_______ mol·L-1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)
(1)下列说法正确的是

A.图1为实验室制备硝基苯的装置
B.图2可以用于测定乙醇分子结构
C.图3装置可以达到验证酸性:CH3COOH > H2CO3 > C6H5OH的目的
D.图4装置可以达到验证溴乙烷发生消去反应生成烯烃的目的
(2)用氧化还原滴定法测定制备得到的TiO2试样中的TiO2的质量分数:在一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作为指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
①TiCl4水解生成TiO2·xH2O的化学方程式为
②滴定终点的现象是
③滴定分析时,称取TiO2试样0.2 g,消耗0.1 mol·L—1NH4Fe(SO4)2标准溶液20mL,则TiO2的质量分数为
④若在滴定终点读取滴定管刻度时,俯视标准溶液的液面,使其测定结果
⑤工业上由H4TiO4可制得钛白粉TiO2。TiO2直接电解还原法生产钛是一种较先进的方法,电解质为熔融的CaCl2,原理如图所示,阴极的电极反应为

(3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl-,利用Ag+与Cr
 生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5 mol·L-1)时,溶液中c(Ag+)为
生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5 mol·L-1)时,溶液中c(Ag+)为 )等于
)等于
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某研究性学习小组设计了一组实验来探究元素周期律。甲同学一次性完成N、C、Si的非金属性强弱的比较;乙同学完成了氧元素的非金属性比硫强的实验。

(1)从以下所给物质中选出甲同学设计的实验所用到物质:
①稀HNO3溶液②稀盐酸③碳酸钙④Na2SiO3溶液⑤SiO2
试剂A为_________ ;试剂C为_________ (填序号)。
(2)乙同学设计的实验所用到试剂A为________ ;装置C中反应的化学方程式为___________________________ 。
(3)丙同学认为甲设计的实验方案不够严谨并做出改进,他在装置B、D之间加装了一个盛有某溶液的洗气瓶,则该溶液的溶质为________________ (填化学式)。

(1)从以下所给物质中选出甲同学设计的实验所用到物质:
①稀HNO3溶液②稀盐酸③碳酸钙④Na2SiO3溶液⑤SiO2
试剂A为
(2)乙同学设计的实验所用到试剂A为
(3)丙同学认为甲设计的实验方案不够严谨并做出改进,他在装置B、D之间加装了一个盛有某溶液的洗气瓶,则该溶液的溶质为
您最近一年使用:0次



