下列有关反应热的叙述正确的是
A.浓硫酸与 溶液混合,生成 溶液混合,生成 水时的反应热代表中和热 水时的反应热代表中和热 |
B.若反应的 和 和 均为负值,则任何温度,反应均可自发进行 均为负值,则任何温度,反应均可自发进行 |
C.含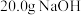 的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为 的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为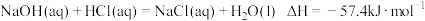 |
D.若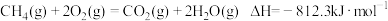 ,则甲烷的燃烧热为 ,则甲烷的燃烧热为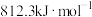 |
更新时间:2021-10-31 11:32:31
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法中正确的是
| A.已知2C(s)+2O2(g)=2CO2(g)△H=a kJ•mol-1,2C(s)+O2(g)=2CO(g)△H=b kJ•mol-1,则a>b |
B.石墨和金刚石完全燃烧的化学方程式均可表示为“C+O2 CO2”,故相同条件下,12g的石墨和金刚石充分燃烧放出的热量相等 CO2”,故相同条件下,12g的石墨和金刚石充分燃烧放出的热量相等 |
| C.一定条件下,0.5 mol N2和1.5 mol H2置于某密闭容器中充分反应生成NH3,放热19.3 kJ,据此实验事实可知:该条件下,每生成1mol NH3,放热19.3 kJ |
| D.4 HCl(g)+O2(g)=2Cl2(g)+2H2O(g)是放热反应,Cl-Cl键和O=O键的键能分别243kJ•mol-1和498kkJ•mol-1,则可推算出H-O键的键能比H-Cl键的键能大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】由N2O和NO反应生成N2和NO2的能量变化如图所示。下列说法正确的是( )
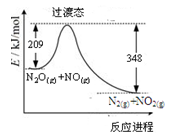

| A.断键吸收能量之和大于成键释放能量之和 |
| B.反应物总能量小于生成物总能量 |
| C.N2O(g) +NO(g) =N2(g) +NO2(g)△H= -139kJ/mol |
| D.反应生成1 mol N2时转移4 mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列热化学方程式正确的是
| A.甲烷的燃烧热为890.3 kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=+890.3 kJ/mol |
| B.表示中和热的热化学方程式:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H= -57.3 kJ/mol |
C.表示H2燃烧热的热化学方程式:H2(g)+ O2(g)= H2O(g) △H = -241.8 kJ/mol O2(g)= H2O(g) △H = -241.8 kJ/mol |
D.500℃、30MPa下,将0.5 molN2和1.5 molH2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g) +3H2(g) 2NH3(g);△H= -38.6 kJ/mol 2NH3(g);△H= -38.6 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列与化学反应能量变化相关的叙述正确的是
A.对于反应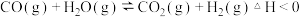 ,在其他条件不变的情况下,改变压强,平衡不发生移动,反应放出的热量不变 ,在其他条件不变的情况下,改变压强,平衡不发生移动,反应放出的热量不变 |
B.同温同压下,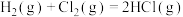 在光照和点燃条件下的焓变不同 在光照和点燃条件下的焓变不同 |
C.甲烷的标准燃烧热为 ,则甲烷燃烧的热化学方程式可表示为: ,则甲烷燃烧的热化学方程式可表示为: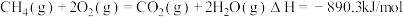 |
D.500℃、30MPa下,将 和 和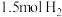 置于密闭容器中充分反应生成 置于密闭容器中充分反应生成 气体,放热 气体,放热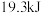 ,其热化学方程式为: ,其热化学方程式为: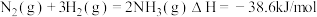 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知CO(g)的燃烧热△H=-283kJ·mol-1,结合如图信息,则2N2O(g)=2N2(g)+O2(g)的反应△H(kJ·mol-1)为


| A.-152 | B.-76 | C.+76 | D.+152 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法正确的是
| A.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的ΔH>0 |
| B.已知2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ·mol-1,则CO的燃烧热ΔH=-283kJ |
| C.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1,则稀H2SO4溶液和稀Ba(OH)2溶液反应的反应热ΔH=2×(-57.3)kJ·mol-1 |
| D.甲烷的燃烧热ΔH=-890.3 kJ·mol-1,则CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列根据事实书写的热化学方程式正确的是
| 选项 | 事实 | 热化学方程式 |
| A | 400℃、催化剂作用下, 和 和 充分反应放热48kJ 充分反应放热48kJ |  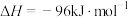 |
| B | 液态联氨( )的燃烧热为 )的燃烧热为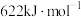 | 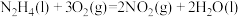  |
| C | HF溶液和NaOH溶液反应的中和热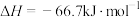 | 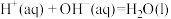 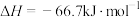 |
| D | 101kPa,18g葡萄糖( )固体完全燃烧生成 )固体完全燃烧生成 气体和液态水放热280kJ 气体和液态水放热280kJ | 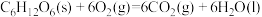 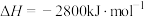 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是( )
| A.6g碳和12gO2反应放出6akJ热量,则碳的热值为akJ•g-1 |
| B.在稀溶液中,H+(aq)+OH-(aq)═H2O(1)△H=-57.3kJ•mol-1,若将含0.5molH2SO4的浓硫酸与含1molNaOH的氢氧化钠溶液混合,放出的热量等于57.3kJ |
| C.由石墨比金刚石稳定可知:C(金刚石,s)=C(石墨,s)△H<0 |
| D.已知:298K时,N2(g)+3H2(g)⇌2NH3(g)△H=-92.0kJ•mol-1, 在相同温度下,向密闭容器中通入0.5molN2和1.5molH2,充分反应放出46.0kJ的热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】用50 mL0.50 mol•L-1盐酸和50 mL0.55 mol•L-1NaOH溶液测定H+(aq)+OH-(aq)=H2O(l)的反应热(ΔH)的实验时,下列说法不正确的是
| A.酸碱混合时,量筒中NaOH溶液应缓缓倒入量热计内筒中,不断用玻璃搅拌器搅拌 |
| B.装置中的大小烧杯之间填满碎泡沫塑料的作用是保温隔热,减少热量损失 |
| C.用量筒量取NaOH溶液时,仰视取液,测得的反应热ΔH不变 |
| D.改用25 mL0.50 mol•L-1盐酸跟25 mL0.55 mol•L-1NaOH溶液进行测定,ΔH数值不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知:①2H2(g)+O2(g)===2H2O(l) ΔH=-570.0 kJ·mol-1;②CO(g)+ O2(g)===CO2(g) ΔH=-280 kJ·mol-1。某H2和CO的混合气体完全燃烧放出141 kJ热量,同时消耗标准状况下5.6 L O2,则原混合气体中H2和CO的物质的量之比为( )
O2(g)===CO2(g) ΔH=-280 kJ·mol-1。某H2和CO的混合气体完全燃烧放出141 kJ热量,同时消耗标准状况下5.6 L O2,则原混合气体中H2和CO的物质的量之比为( )
 O2(g)===CO2(g) ΔH=-280 kJ·mol-1。某H2和CO的混合气体完全燃烧放出141 kJ热量,同时消耗标准状况下5.6 L O2,则原混合气体中H2和CO的物质的量之比为( )
O2(g)===CO2(g) ΔH=-280 kJ·mol-1。某H2和CO的混合气体完全燃烧放出141 kJ热量,同时消耗标准状况下5.6 L O2,则原混合气体中H2和CO的物质的量之比为( )| A.2∶1 | B.1∶2 | C.1∶1 | D.2∶3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:①2H2(g)+O2(g)=2H2O(g) ΔH1=-483.6 kJ·mol-1
②H2(g)+S(g) H2S(g) ΔH2=-20.1 kJ·mol-1。
H2S(g) ΔH2=-20.1 kJ·mol-1。
下列判断一定正确的是
②H2(g)+S(g)
 H2S(g) ΔH2=-20.1 kJ·mol-1。
H2S(g) ΔH2=-20.1 kJ·mol-1。下列判断一定正确的是
| A.由反应①可知,氢气的燃烧热ΔH=-241.8kJ·mol-1 |
| B.由2H2(g)+O2(g)=2H2O(l) ΔH3,可知ΔH3>ΔH1 |
| C.若反应②中改用固态硫,放出的热量将小于20.1kJ |
| D.因为ΔH2>ΔH1,故H2O(g)没有H2S(g)稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法不正确的是
| A.CH4 的燃烧热是890.3kJ·mol-1,则表示 CH4 的燃烧热的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
| B.由C(金刚石)=C(石墨) ΔH=-1.9 kJ·mol-1可知,石墨比金刚石稳定 |
| C.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,若将含 1mol HNO3 的稀溶液与含 1mol Ba(OH)2 的稀溶液混合,放出的热量为 57.3 kJ |
| D.1mol 钠蒸气与 2 mol 钠蒸气完全燃烧时,燃烧热相同 |
您最近一年使用:0次



