我国自主研发的长征系列火箭为发射“神舟”“嫦娥”作出了杰出贡献。某液体化合物X2Y4,常用作火箭燃料。16 g X2Y4在一定量的O2中恰好完全燃烧,化学方程式为 冷却后标准状况下测得生成物的体积为11.2 L,其密度为1.25 g·L-1,则:
冷却后标准状况下测得生成物的体积为11.2 L,其密度为1.25 g·L-1,则:
(1)反应前O2的体积V(O2)为___________ 。
(2)X2的摩尔质量为___________ ;Y元素的名称是___________ 。
(3)若反应生成0.1 mol X2,则转移电子的物质的量为___________ mol。
 冷却后标准状况下测得生成物的体积为11.2 L,其密度为1.25 g·L-1,则:
冷却后标准状况下测得生成物的体积为11.2 L,其密度为1.25 g·L-1,则:(1)反应前O2的体积V(O2)为
(2)X2的摩尔质量为
(3)若反应生成0.1 mol X2,则转移电子的物质的量为
更新时间:2021-11-04 15:56:02
|
【知识点】 物质的量有关计算
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知1.505×10 23 个X气体分子的质量为8 g,则X气体的摩尔质量是多少_____________ ?
您最近半年使用:0次
【推荐2】磷及部分重要化合物的相互转化如图所示。
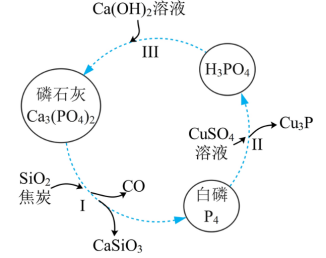
(1)不慎将白磷沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为______ 。
(2)步骤Ⅲ中,反应物的比例不同可获得不同的产物,除Ca3(PO4)2外可能的产物还有______ 。
磷灰石是生产磷肥的原料,它的组成可以看作是Ca3(PO4)2、CaF2、CaSO4、CaCO3、SiO2的混合物,部分元素的分析结果如下(各元素均以氧化物形式表示):
(3)磷灰石中,碳元素的质量分数为______ %(保留两位小数)。
(4)取100g磷灰石粉末,加入足量的浓硫酸,并加热,钙元素全部以CaSO4的形式存在,可以得到CaSO4______ g(保留两位小数)。
(5)取m g 磷灰石粉末,用50.00mL混酸溶液(磷酸为0.5mol/L、硫酸为0.1mol/L)与其反应,结果Ca、S、P元素全部以CaSO4和Ca(H2PO4)2的形式存在,求m的值______ 。

(1)不慎将白磷沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为
(2)步骤Ⅲ中,反应物的比例不同可获得不同的产物,除Ca3(PO4)2外可能的产物还有
磷灰石是生产磷肥的原料,它的组成可以看作是Ca3(PO4)2、CaF2、CaSO4、CaCO3、SiO2的混合物,部分元素的分析结果如下(各元素均以氧化物形式表示):
| 成分 | CaO | P2O5 | SO3 | CO2 |
| 质量分数(%) | 47.30 | 28.40 | 3.50 | 6.10 |
(3)磷灰石中,碳元素的质量分数为
(4)取100g磷灰石粉末,加入足量的浓硫酸,并加热,钙元素全部以CaSO4的形式存在,可以得到CaSO4
(5)取m g 磷灰石粉末,用50.00mL混酸溶液(磷酸为0.5mol/L、硫酸为0.1mol/L)与其反应,结果Ca、S、P元素全部以CaSO4和Ca(H2PO4)2的形式存在,求m的值
您最近半年使用:0次
【推荐3】已知铜和浓硫酸可以在加热条件下发生反应,化学方程式为(已配平):Cu+2H2SO4(浓) CuSO4+A↑+2H2O;试通过计算和推理完成下面的问题:
CuSO4+A↑+2H2O;试通过计算和推理完成下面的问题:
(1)在参加反应的硫酸中,被还原的硫酸与未被还原的硫酸的物质的量之比为_______ ,A物质可以与强碱反应生成盐和水,则A应该属于_______ (用字母代号填写)。
A.酸 B.酸性氧化物 C.盐 D.电解质 E.非电解质
(2)一定量的铜片与含1.2mol的H2SO4的浓硫酸充分反应(浓硫酸过量),如果该反应过程中转移了0.4mol电子,生成的A气体在标况下的体积为_______ L(假设气体全部逸出)。
(3)将(2)中反应后所得的溶液稀释后与足量的Ba(OH)2溶液反应,所得沉淀的质量为_______ g。
(4)请将方程式配平并用双线桥法表示出电子转移的方向和数目:_______
_______Cu +_______HNO3 =_______Cu(NO3)2+_______NO↑+_______H2O
 CuSO4+A↑+2H2O;试通过计算和推理完成下面的问题:
CuSO4+A↑+2H2O;试通过计算和推理完成下面的问题:(1)在参加反应的硫酸中,被还原的硫酸与未被还原的硫酸的物质的量之比为
A.酸 B.酸性氧化物 C.盐 D.电解质 E.非电解质
(2)一定量的铜片与含1.2mol的H2SO4的浓硫酸充分反应(浓硫酸过量),如果该反应过程中转移了0.4mol电子,生成的A气体在标况下的体积为
(3)将(2)中反应后所得的溶液稀释后与足量的Ba(OH)2溶液反应,所得沉淀的质量为
(4)请将方程式配平并用双线桥法表示出电子转移的方向和数目:
_______Cu +_______HNO3 =_______Cu(NO3)2+_______NO↑+_______H2O
您最近半年使用:0次



