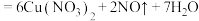现有由硝酸钾、硝酸铵、硝酸镁组成的无土栽培液 ,部分离子的浓度如下表所示:
,部分离子的浓度如下表所示:
(1)混合液中,硝酸铵的物质的量为___________ ,硝酸钾的质量为___________ 。
(2)该混合溶液中硝酸镁的物质的量浓度为___________ ,将该混合溶液加水稀释至体积为 ,稀释后溶液中
,稀释后溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
(3)向该稀释后的溶液中通入标准状况下的
___________ L可使 沉淀完全,写出
沉淀完全,写出 沉淀过程中的离子方程式
沉淀过程中的离子方程式___________ 。
 ,部分离子的浓度如下表所示:
,部分离子的浓度如下表所示:| 离子种类 |  |  |  |
离子的物质的量浓度( ) ) | 0.2 | 0.1 | 0.6 |
(1)混合液中,硝酸铵的物质的量为
(2)该混合溶液中硝酸镁的物质的量浓度为
 ,稀释后溶液中
,稀释后溶液中 的物质的量浓度为
的物质的量浓度为(3)向该稀释后的溶液中通入标准状况下的

 沉淀完全,写出
沉淀完全,写出 沉淀过程中的离子方程式
沉淀过程中的离子方程式
更新时间:2021-11-07 10:28:12
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】下图是氮气及几种氮的化合物间的转换关系。请回答下列问题:___________ 。
(2)工业上常用 制取
制取 ,请写出反应的化学方程式
,请写出反应的化学方程式___________ 。
(3)实验室里常用Cu与稀硝酸反应制取 ,当生成标准状况下3.36L
,当生成标准状况下3.36L 时,转移的电子数目为
时,转移的电子数目为___________ 。
(4)生产硝酸时排放的 会污染环境,一种治理方案是用氨气在催化剂作用下将
会污染环境,一种治理方案是用氨气在催化剂作用下将 还原成
还原成 ,请配平化学方程式:
,请配平化学方程式:___________ 。
___________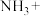 ___________
___________
 ___________
___________ ___________
___________
(5)有一瓶稀硫酸和稀硝酸的混合溶液,其中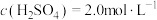 ,
,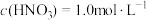 。取
。取 该混合溶液与12.8g铜粉反应,标准状况下生成
该混合溶液与12.8g铜粉反应,标准状况下生成 的体积为
的体积为___________ L。
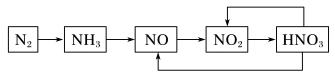
(2)工业上常用
 制取
制取 ,请写出反应的化学方程式
,请写出反应的化学方程式(3)实验室里常用Cu与稀硝酸反应制取
 ,当生成标准状况下3.36L
,当生成标准状况下3.36L 时,转移的电子数目为
时,转移的电子数目为(4)生产硝酸时排放的
 会污染环境,一种治理方案是用氨气在催化剂作用下将
会污染环境,一种治理方案是用氨气在催化剂作用下将 还原成
还原成 ,请配平化学方程式:
,请配平化学方程式:___________
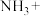 ___________
___________
 ___________
___________ ___________
___________
(5)有一瓶稀硫酸和稀硝酸的混合溶液,其中
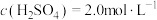 ,
,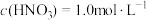 。取
。取 该混合溶液与12.8g铜粉反应,标准状况下生成
该混合溶液与12.8g铜粉反应,标准状况下生成 的体积为
的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】现有一瓶标准状况下的44.8 L HCl气体,回答下列各小题:
(1)所含HCl的物质的量是______ 。
(2)所含HCl的质量是_______ 。
(3)所含电子的数目是_______ 。(用NA表示)
(4)与_____ g NH3所含原子数相等。
(5)将所含的HCl全部溶于水配成1 L溶液,则c(Cl-)是______ ,与_____ mol/L的CuCl2溶液中的Cl-浓度相同。
(1)所含HCl的物质的量是
(2)所含HCl的质量是
(3)所含电子的数目是
(4)与
(5)将所含的HCl全部溶于水配成1 L溶液,则c(Cl-)是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(1)0.5mol/ (NH4)2S溶液中NH4+ 的物质的量浓度_____________ 。
(2)标准状况下,1.7 g NH3与______ L H2S气体含有的氢原子数相同。
(3)标准状况下,1.6g某气态氧化物RO2体积为0.56L,该气体的物质的量为____ mol,RO2的相对分子质量为_______ 。
(4)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O该反应中的氧化剂是
MnCl2+Cl2↑+2H2O该反应中的氧化剂是________ ,若有4molHCl参加反应,则被氧化的HCl的物质的量是______ mol,如反应中转移了0.4mol电子,则产生的Cl2在标准状况下体积为_________ L。
(5)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L,该混合气体的平均摩尔质量为______ ,该气体对氢气的相对密度为______ 。
(2)标准状况下,1.7 g NH3与
(3)标准状况下,1.6g某气态氧化物RO2体积为0.56L,该气体的物质的量为
(4)MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O该反应中的氧化剂是
MnCl2+Cl2↑+2H2O该反应中的氧化剂是(5)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L,该混合气体的平均摩尔质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】为确定Fe2O3和Cu混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别投入30.0 mL某浓度的稀硫酸中。充分反应后,每组样品剩余固体的质量与原样品质量的关系如图所示。请根据反应中各物质的计量关系分析图象,回答下列问题。

(1)各组样品均发生了反应:______ ,_____ 。(写离子方程式)
(2)1.76 g样品充分反应后,溶液中一定存在_____ ,_____ ;一定不存在___ (填写离子符号),请设计实验证明充分反应后的溶液中不存在该离子___ 。
(3)求算该混合物中组分物质的量之比(写出简要的解题过程)_____ 。
(4)求稀硫酸的物质的量浓度(写出简要的解题过程)_____ 。

(1)各组样品均发生了反应:
(2)1.76 g样品充分反应后,溶液中一定存在
(3)求算该混合物中组分物质的量之比(写出简要的解题过程)
(4)求稀硫酸的物质的量浓度(写出简要的解题过程)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】常温下,浓度均为0.1mol·L-1的两种溶液:①氨水 ②NH4Cl溶液。
(1)写出①氨水中NH3·H2O的电离方程式:_______ 。
(2)测得②溶液的pH<7,则溶液中c(NH )
)______ c(Cl-)(填“>”“<”或“=”),写出②溶液发生水解反应的化学方程式:_______ 。
(3)需要配制2L 0.1mol·L-1NH4Cl溶液,则用托盘天平称取的固体NH4Cl(M=53.5)为______ 克。
(1)写出①氨水中NH3·H2O的电离方程式:
(2)测得②溶液的pH<7,则溶液中c(NH
 )
)(3)需要配制2L 0.1mol·L-1NH4Cl溶液,则用托盘天平称取的固体NH4Cl(M=53.5)为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】化学计量在化学知识体系中占有重要地位,请回答下列问题。
(1)标准状况下,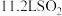 的物质的量是
的物质的量是___________ ,质量是___________ g。
(2)同温同压下,质量相等的 、
、 、
、 、
、 四种气体中,含有分子数目最多的是
四种气体中,含有分子数目最多的是___________ ,密度最大的是___________ 。
(3) 中含有的
中含有的 为
为 ,则X的摩尔质量为
,则X的摩尔质量为___________ 。
(4) 的盐酸与
的盐酸与 铁屑反应,参与反应的
铁屑反应,参与反应的 物质的量为
物质的量为___________ ,生成的 在标准状况下的体积为
在标准状况下的体积为___________ L。
(5)现有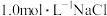 溶液
溶液 ,若取
,若取 该溶液用水稀释到
该溶液用水稀释到 ,所得溶液的
,所得溶液的 的物质的量浓度为
的物质的量浓度为___________ 。
(1)标准状况下,
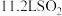 的物质的量是
的物质的量是(2)同温同压下,质量相等的
 、
、 、
、 、
、 四种气体中,含有分子数目最多的是
四种气体中,含有分子数目最多的是(3)
 中含有的
中含有的 为
为 ,则X的摩尔质量为
,则X的摩尔质量为(4)
 的盐酸与
的盐酸与 铁屑反应,参与反应的
铁屑反应,参与反应的 物质的量为
物质的量为 在标准状况下的体积为
在标准状况下的体积为(5)现有
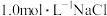 溶液
溶液 ,若取
,若取 该溶液用水稀释到
该溶液用水稀释到 ,所得溶液的
,所得溶液的 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】在0.4L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:

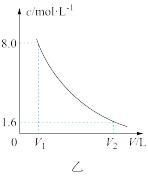
(1)该混合液中,NaCl的物质的量为________ mol,含溶质MgCl2的质量为_______ g。
(2)该混合液中CaCl2的物质的量为________ mol,将该混合液加水稀释至体积为1L,稀释后溶液中Ca2+的物质的量浓度为________ mol∙L-1。
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀________ mol。
(4)将该营养液加水稀释,稀释过程中Cl-的浓度(c)随溶液体积(V)变化的曲线如图乙所示,则V1=________ ,V2=________ 。


(1)该混合液中,NaCl的物质的量为
(2)该混合液中CaCl2的物质的量为
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀
(4)将该营养液加水稀释,稀释过程中Cl-的浓度(c)随溶液体积(V)变化的曲线如图乙所示,则V1=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】物质的量是联系宏观的和微观的桥梁。
(1)标准状况下,与5.6L的CH4气体含相同H原子数的H2S的质量为____ g。
(2)将0.2mol·L-1Al2(SO4)3和0.2mol·L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c (SO )=
)=____ mol·L-1。若用容量瓶以质量分数为98%、密度为1.84g·cm-3的浓硫酸,配制500mL浓度成0.2mol·L-1稀硫酸,计算需要量取____ mL的浓硫酸。
(3)某无土栽培用的营养液,要求KCl、K2SO4和NH4Cl三种固体原料的物质的量之比为1︰4︰8。
①配制该营养液后c(NH )=0.016mol·L-1,溶液中c(K+)=
)=0.016mol·L-1,溶液中c(K+)=____ 。
②若采用(NH4)2SO4和KCl来配制该营养液,则(NH4)2SO4和KCl物质的量之比为____ 。
(1)标准状况下,与5.6L的CH4气体含相同H原子数的H2S的质量为
(2)将0.2mol·L-1Al2(SO4)3和0.2mol·L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c (SO
 )=
)=(3)某无土栽培用的营养液,要求KCl、K2SO4和NH4Cl三种固体原料的物质的量之比为1︰4︰8。
①配制该营养液后c(NH
 )=0.016mol·L-1,溶液中c(K+)=
)=0.016mol·L-1,溶液中c(K+)=②若采用(NH4)2SO4和KCl来配制该营养液,则(NH4)2SO4和KCl物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物的“价一类”二维图的部分信息如下:

回答下列问题:
(1)据图中信息,写出Y、Z的化学式:_______ 、_______ 。
(2)已知高氯酸(HClO4)是强酸,写出高氯酸溶液与氢氧化钠溶液反应的离子方程式:______ 。
(3)氯气既有氧化性又有还原性,结合上图说明理由:_______ 。
(4)二氧化氯(ClO2)为新时代绿色消毒剂,制备原理为:5NaClO2+4HCl=4ClO2+5NaCl+2H2O
①按照物质类别对上述反应中的各物质进行分类,未涉及的物质类别是_______ (填序号)。
A.金属氧化物 B.非金属氧化物 C.酸 D.碱 E.盐
②NaClO2发生还原反应的产物是_______ (写化学式);该反应_______ (填“能”或“不能”)用稀硫酸代替盐酸。

回答下列问题:
(1)据图中信息,写出Y、Z的化学式:
(2)已知高氯酸(HClO4)是强酸,写出高氯酸溶液与氢氧化钠溶液反应的离子方程式:
(3)氯气既有氧化性又有还原性,结合上图说明理由:
(4)二氧化氯(ClO2)为新时代绿色消毒剂,制备原理为:5NaClO2+4HCl=4ClO2+5NaCl+2H2O
①按照物质类别对上述反应中的各物质进行分类,未涉及的物质类别是
A.金属氧化物 B.非金属氧化物 C.酸 D.碱 E.盐
②NaClO2发生还原反应的产物是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】纳米碳酸钙又称为超细碳酸钙,标准的名称即超细碳酸钙。纳米碳酸钙应用最成熟的行业是塑料工业,主要用于高档塑料制品。其粒度介于10纳米—100纳米之间,一般以石灰石为原料,经煅烧、消化、碳化、分离、干燥、分级、包装等工序制备。
(1)煅烧工艺中发生反应的化学方程式:_______
(2)消化时,生石灰溶于水,制得消石灰悬浊液,该悬浊液、溶液和胶体的本质区别是:_______ ;若将制得的纳米碳酸钙粉末均匀分散在溶剂中,可用于鉴别其不同于溶液的方法是:_______
(3)消石灰悬浊液静置一段时间后,上层为清液,下层有大量白色浑浊的现象,取少量的上层清液于试管中,滴加少量的氯化铜溶液会出现蓝色沉淀,写出反应的离子方程式:_______ ,其反应属于_______ (填反应类型)。
(4)碳化时,需要将CO2通入消石灰悬浊液中,可采用连续喷雾碳化法,其目的是:_______ 。碳化后,经多步物理操作后,可获得纳米碳酸钙。
(5)在上述反应不涉及的基本反应类型有:_______ ;请利用上述涉及的元素写出一个符合该反应类型的化学方程式:_______
(1)煅烧工艺中发生反应的化学方程式:
(2)消化时,生石灰溶于水,制得消石灰悬浊液,该悬浊液、溶液和胶体的本质区别是:
(3)消石灰悬浊液静置一段时间后,上层为清液,下层有大量白色浑浊的现象,取少量的上层清液于试管中,滴加少量的氯化铜溶液会出现蓝色沉淀,写出反应的离子方程式:
(4)碳化时,需要将CO2通入消石灰悬浊液中,可采用连续喷雾碳化法,其目的是:
(5)在上述反应不涉及的基本反应类型有:
您最近一年使用:0次


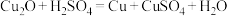
 (稀)
(稀)