现有一瓶标准状况下的44.8 L HCl气体,回答下列各小题:
(1)所含HCl的物质的量是______ 。
(2)所含HCl的质量是_______ 。
(3)所含电子的数目是_______ 。(用NA表示)
(4)与_____ g NH3所含原子数相等。
(5)将所含的HCl全部溶于水配成1 L溶液,则c(Cl-)是______ ,与_____ mol/L的CuCl2溶液中的Cl-浓度相同。
(1)所含HCl的物质的量是
(2)所含HCl的质量是
(3)所含电子的数目是
(4)与
(5)将所含的HCl全部溶于水配成1 L溶液,则c(Cl-)是
更新时间:2024-01-09 13:51:50
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1) 和
和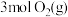 的质量之比
的质量之比___________ ,分子数之比___________ ,同温同压的密度之比为___________ ,原子数之比为___________ ,体积之比为___________ 。
(2)①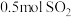 ,含有的分子数约为
,含有的分子数约为___________ 个,质量为___________ ,标准状况下体积为___________ 。
②标准状况下,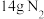 所占有的体积为
所占有的体积为___________ 。
③标准状况下,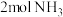 与
与___________ 
 的体积相等。
的体积相等。
(1)
 和
和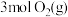 的质量之比
的质量之比(2)①
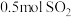 ,含有的分子数约为
,含有的分子数约为②标准状况下,
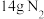 所占有的体积为
所占有的体积为③标准状况下,
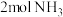 与
与
 的体积相等。
的体积相等。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某气体分子为双原子分子,它的摩尔质量为M g·mol-1,该气体质量为m g,阿伏加 德罗常数用NA表示,则:
(1)该气体的物质的量为________ mol。
(2)该气体所含原子总数为________ 个。
(3)该气体在标准状况下的密度为________ g·L-1。
(4)该气体一个分子的质量为________ g。
(1)该气体的物质的量为
(2)该气体所含原子总数为
(3)该气体在标准状况下的密度为
(4)该气体一个分子的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题:
(1)4.9gH2SO4,含___________ 个H2SO4分子、能和___________ molNaOH完全反应
(2)含有相同碳原子数的CO和CO2,其质量之比为______
(3)含0.2molFe3+的 Fe2(SO4)3中含SO 的物质的量为
的物质的量为______
(4)把淀粉溶液溶于沸水中,制成淀粉胶体是___________ ,提纯、精制胶体的方法是___________ 。
(1)4.9gH2SO4,含
(2)含有相同碳原子数的CO和CO2,其质量之比为
(3)含0.2molFe3+的 Fe2(SO4)3中含SO
 的物质的量为
的物质的量为(4)把淀粉溶液溶于沸水中,制成淀粉胶体是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)相同质量的C2H4和C3H6,所含分子数目之比为_____ ,所含原子数目之比为____ 。
(2)在标准状况下,①4 g H2、②11.2 L O2、③1 mol H2O中,含原子数最多的是_______ ,体积最小的是_______ 。(填序号)
(2)在标准状况下,①4 g H2、②11.2 L O2、③1 mol H2O中,含原子数最多的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】以物质的量为中心的计算在高中化学学习中很重要。请完成下列题目。
(1)1gH2中含有_______ 个H。
(2)6.02×1023个CO2分子与16gO2,二者在标况下的体积之比_______ 。
(3)从2L0.5mol·L-1NaOH溶液中取出1L,则所取出的溶液中含NaOH的质量是_______ g。
(1)1gH2中含有
(2)6.02×1023个CO2分子与16gO2,二者在标况下的体积之比
(3)从2L0.5mol·L-1NaOH溶液中取出1L,则所取出的溶液中含NaOH的质量是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】铁是人体必需的微量元素,黑木耳等食品中富含铁元素。下图是某学习小组同学检验黑木耳中的铁元素并测定其含量的实验流程图。
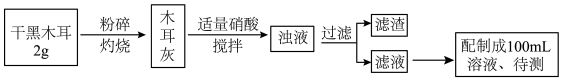
(一)定性检验
(1)粉碎后的黑木耳应置于___________ (填仪器名称)中灼烧。取3滴待测液滴在点滴板上,加几滴___________ (填化学式)溶液,若出现___________ 的现象,则此溶液中存在Fe3+。
(2)下列过滤操作中不规范的有___________(填字母序号)。
(二)定量测定
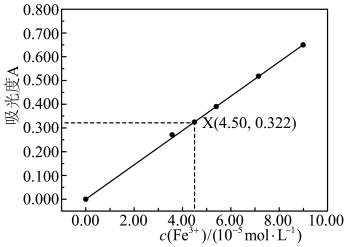
(3)已知溶液的吸光度A与溶液中c(Fe3+)关系如下图。该小组从上述100mL溶液中取出10mL待测液,测得待测液吸光度位于图中X点,试计算该黑木耳中铁元素的含量(mg/100g)___________ 。(要求有计算过程)

(一)定性检验
(1)粉碎后的黑木耳应置于
(2)下列过滤操作中不规范的有___________(填字母序号)。
| A.玻璃棒用作引流 |
| B.用玻璃棒在漏斗中轻轻搅动以加快过滤速度 |
| C.将滤纸湿润,使其紧贴漏斗壁 |
| D.漏斗末端颈尖未紧靠烧杯内壁 |
(二)定量测定
(3)已知溶液的吸光度A与溶液中c(Fe3+)关系如下图。该小组从上述100mL溶液中取出10mL待测液,测得待测液吸光度位于图中X点,试计算该黑木耳中铁元素的含量(mg/100g)

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】取100mL等物质的量浓度的盐酸和硫酸混合溶液,当加入100mL3.00mol/L的Ba(OH)2溶液时,溶液显中性。请计算:
(1)盐酸的物质的量浓度为___________ mol·L-1
(2)当加入的Ba(OH)2体积为___________ mL时,产生的沉淀质量为34.95g。
(1)盐酸的物质的量浓度为
(2)当加入的Ba(OH)2体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】下列有几种溶液,其中硝酸根离子的物质的量浓度相等的组合是_________
①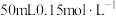 硝酸镁溶液 ②
硝酸镁溶液 ②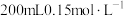 硝酸钠溶液
硝酸钠溶液
③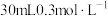 硝酸银溶液 ④
硝酸银溶液 ④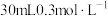 硝酸钡溶液
硝酸钡溶液
①
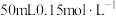 硝酸镁溶液 ②
硝酸镁溶液 ②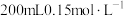 硝酸钠溶液
硝酸钠溶液③
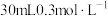 硝酸银溶液 ④
硝酸银溶液 ④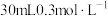 硝酸钡溶液
硝酸钡溶液
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】有以下物质:①铁红②Al③C④稀硫酸⑤浓硫酸⑥NaOH溶液⑦Al2(SO4)3
(1)写出①与④反应的离子方程式___ 。
(2)既能跟④又能跟⑥反应的是___ (填序号),写出它与⑥反应的化学方程式___ 。
(3)34.2g⑦溶于水配成500mL溶液,溶液中SO 的物质的量浓度为
的物质的量浓度为___ 。
(1)写出①与④反应的离子方程式
(2)既能跟④又能跟⑥反应的是
(3)34.2g⑦溶于水配成500mL溶液,溶液中SO
 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次



