100g 12mol/L(密度为1.19g/mL)的盐酸用100g水稀释后,其物质的量浓度_______ (填“大于”、“等于”或“小于”)6mol/L。
更新时间:2024-01-02 20:46:43
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】氯气和氯化氢在生产生活中有着重要的应用。回答下列问题:
(1)氯碱工业是化工重要制备之一,写出工业生成氯气的化学方程式:___________ 。
(2)氯气可以制得漂粉精和消毒水(有效成分为NaClO),漂粉精可用于游泳池中水的消毒,原因是(用化学方程式表示):___________ 。将一瓶NaClO溶液(只含一种溶质),长时间放置在空气中,最终变为___________ (填溶质的化学式)。
(3)在标准状态下,224体积的氯化氢溶解在1体积的水中,形成密度为1.2g/cm3的溶液。则该溶液的物质的量浓度为___________ 。(结果保留一位小数)
(4)已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反应的体系,共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质,写出一个包含上述七种物质的氧化还原反应方程式(不用配平):___________ 。上述反应中,还原剂是:___________ ,还原产物是:___________ 。
(1)氯碱工业是化工重要制备之一,写出工业生成氯气的化学方程式:
(2)氯气可以制得漂粉精和消毒水(有效成分为NaClO),漂粉精可用于游泳池中水的消毒,原因是(用化学方程式表示):
(3)在标准状态下,224体积的氯化氢溶解在1体积的水中,形成密度为1.2g/cm3的溶液。则该溶液的物质的量浓度为
(4)已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反应的体系,共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质,写出一个包含上述七种物质的氧化还原反应方程式(不用配平):
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】填空。
(1)工业上用_______ 和_______ 作为原料来制取漂白粉,反应的化学方程式为_______ 。漂白粉的有效成分是_______ ,漂白粉溶于水后,滴加少量盐酸可加快漂白和杀菌的速度,此过程中发生反应的化学方程式_______ 。
(2)从200 mL、5 mol/L Na2CO3溶液中取出20 mL溶液,其溶质的物质的量是_______ 。将取出的溶液稀释至100 mL,其Na+的物质的量浓度是_______ 。
(3)有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.2 mol/L, 的物质的量浓度为0.5 mol/L,则此溶液中K+的物质的量浓度为
的物质的量浓度为0.5 mol/L,则此溶液中K+的物质的量浓度为_______ 。
(4)在标准状况下,CO和CO2的混合气体共11.2 L,质量为18.8 g,其中含有_______ 个CO分子,该混合气体中CO与CO2的密度之比为_______ 。
(1)工业上用
(2)从200 mL、5 mol/L Na2CO3溶液中取出20 mL溶液,其溶质的物质的量是
(3)有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.2 mol/L,
 的物质的量浓度为0.5 mol/L,则此溶液中K+的物质的量浓度为
的物质的量浓度为0.5 mol/L,则此溶液中K+的物质的量浓度为(4)在标准状况下,CO和CO2的混合气体共11.2 L,质量为18.8 g,其中含有
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】物质的量是联系宏观的和微观的桥梁。
(1)标准状况下,与5.6L的CH4气体含相同H原子数的H2S的质量为____ g。
(2)将0.2mol·L-1Al2(SO4)3和0.2mol·L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c (SO )=
)=____ mol·L-1。若用容量瓶以质量分数为98%、密度为1.84g·cm-3的浓硫酸,配制500mL浓度成0.2mol·L-1稀硫酸,计算需要量取____ mL的浓硫酸。
(3)某无土栽培用的营养液,要求KCl、K2SO4和NH4Cl三种固体原料的物质的量之比为1︰4︰8。
①配制该营养液后c(NH )=0.016mol·L-1,溶液中c(K+)=
)=0.016mol·L-1,溶液中c(K+)=____ 。
②若采用(NH4)2SO4和KCl来配制该营养液,则(NH4)2SO4和KCl物质的量之比为____ 。
(1)标准状况下,与5.6L的CH4气体含相同H原子数的H2S的质量为
(2)将0.2mol·L-1Al2(SO4)3和0.2mol·L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c (SO
 )=
)=(3)某无土栽培用的营养液,要求KCl、K2SO4和NH4Cl三种固体原料的物质的量之比为1︰4︰8。
①配制该营养液后c(NH
 )=0.016mol·L-1,溶液中c(K+)=
)=0.016mol·L-1,溶液中c(K+)=②若采用(NH4)2SO4和KCl来配制该营养液,则(NH4)2SO4和KCl物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】已知浓硫酸密度为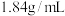 ,质量分数为98%,配制
,质量分数为98%,配制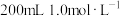 的稀硫酸需用量筒量取该浓硫酸
的稀硫酸需用量筒量取该浓硫酸___________ mL。
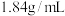 ,质量分数为98%,配制
,质量分数为98%,配制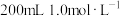 的稀硫酸需用量筒量取该浓硫酸
的稀硫酸需用量筒量取该浓硫酸
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】如图为实验室某浓盐酸试剂瓶标签上的有关数据,根据有关数据回答下列问题:
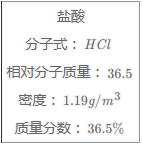
(1)该浓盐酸中HCl的物质的量浓度为________ mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量不随所取体积多少而变化的是_______ 。
A.溶液中HCl的质量
B.溶液的pH
C.溶液中H+的数目
D.溶液的密度
(3)欲用上述浓盐酸配制500mL 2mol/L的稀盐酸,需要_____ mL上述盐酸 (保留1位小数)
(4)现有1 L1mol/L的稀盐酸,欲使其浓度增大1倍。采取的措施合理的是________________ 。
A、通入标况下HCl气体22.4L
B、将溶液加热浓缩至0. 5L
C、加入5mol/L的盐酸0.6L.再稀释至2L.
D、加入1L 3mol/L的盐酸混合均匀

(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量不随所取体积多少而变化的是
A.溶液中HCl的质量
B.溶液的pH
C.溶液中H+的数目
D.溶液的密度
(3)欲用上述浓盐酸配制500mL 2mol/L的稀盐酸,需要
(4)现有1 L1mol/L的稀盐酸,欲使其浓度增大1倍。采取的措施合理的是
A、通入标况下HCl气体22.4L
B、将溶液加热浓缩至0. 5L
C、加入5mol/L的盐酸0.6L.再稀释至2L.
D、加入1L 3mol/L的盐酸混合均匀
您最近一年使用:0次



