已知浓硫酸密度为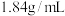 ,质量分数为98%,配制
,质量分数为98%,配制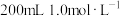 的稀硫酸需用量筒量取该浓硫酸
的稀硫酸需用量筒量取该浓硫酸___________ mL。
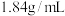 ,质量分数为98%,配制
,质量分数为98%,配制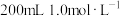 的稀硫酸需用量筒量取该浓硫酸
的稀硫酸需用量筒量取该浓硫酸
更新时间:2021-12-04 19:01:27
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】在0.4L由NaCl,MgSO4、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题。

(1)该混合液中,NaCl的物质的量为__ mol,含溶质MgSO4的质量为___ g。
(2)该混合液中CaCl2的物质的量为___ mol,将该混合液加水稀释至体积为500mL,稀释后溶液中Ca2+的物质的量浓度为__ mol∙L−1。
(3)向该稀释后的溶液中加入足量氯化钡溶液,可得到沉淀__ g。

(1)该混合液中,NaCl的物质的量为
(2)该混合液中CaCl2的物质的量为
(3)向该稀释后的溶液中加入足量氯化钡溶液,可得到沉淀
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】现有由硝酸钾、硝酸铵、硝酸镁组成的无土栽培液 ,部分离子的浓度如下表所示:
,部分离子的浓度如下表所示:
(1)混合液中,硝酸铵的物质的量为___________ ,硝酸钾的质量为___________ 。
(2)该混合溶液中硝酸镁的物质的量浓度为___________ ,将该混合溶液加水稀释至体积为 ,稀释后溶液中
,稀释后溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
(3)向该稀释后的溶液中通入标准状况下的
___________ L可使 沉淀完全,写出
沉淀完全,写出 沉淀过程中的离子方程式
沉淀过程中的离子方程式___________ 。
 ,部分离子的浓度如下表所示:
,部分离子的浓度如下表所示:| 离子种类 |  |  |  |
离子的物质的量浓度( ) ) | 0.2 | 0.1 | 0.6 |
(1)混合液中,硝酸铵的物质的量为
(2)该混合溶液中硝酸镁的物质的量浓度为
 ,稀释后溶液中
,稀释后溶液中 的物质的量浓度为
的物质的量浓度为(3)向该稀释后的溶液中通入标准状况下的

 沉淀完全,写出
沉淀完全,写出 沉淀过程中的离子方程式
沉淀过程中的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】物质的量是联系宏观的和微观的桥梁。
(1)标准状况下,与5.6L的CH4气体含相同H原子数的H2S的质量为____ g。
(2)将0.2mol·L-1Al2(SO4)3和0.2mol·L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c (SO )=
)=____ mol·L-1。若用容量瓶以质量分数为98%、密度为1.84g·cm-3的浓硫酸,配制500mL浓度成0.2mol·L-1稀硫酸,计算需要量取____ mL的浓硫酸。
(3)某无土栽培用的营养液,要求KCl、K2SO4和NH4Cl三种固体原料的物质的量之比为1︰4︰8。
①配制该营养液后c(NH )=0.016mol·L-1,溶液中c(K+)=
)=0.016mol·L-1,溶液中c(K+)=____ 。
②若采用(NH4)2SO4和KCl来配制该营养液,则(NH4)2SO4和KCl物质的量之比为____ 。
(1)标准状况下,与5.6L的CH4气体含相同H原子数的H2S的质量为
(2)将0.2mol·L-1Al2(SO4)3和0.2mol·L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c (SO
 )=
)=(3)某无土栽培用的营养液,要求KCl、K2SO4和NH4Cl三种固体原料的物质的量之比为1︰4︰8。
①配制该营养液后c(NH
 )=0.016mol·L-1,溶液中c(K+)=
)=0.016mol·L-1,溶液中c(K+)=②若采用(NH4)2SO4和KCl来配制该营养液,则(NH4)2SO4和KCl物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】实验室需配制250mL0.20mol/LNa2CO3溶液,请你参与实验过程,并完成相关实验报告(填写表格中横线上数字序号所示内容)。
| 实验原理 | m=cVM |
| 实验仪器 | 托盘天平、药匙、烧杯、玻璃棒、250mL |
| 实验步骤 | (1)计算:溶质Na2CO3固体的质量为 (2)称量:用托盘天平称取所需Na2CO3固体。 (3)溶解:将称好的Na2CO3固体放入烧杯中,用适量蒸馏水溶解并冷却。 (4)转移、洗涤:将烧杯中的溶液注入仪器①中,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也都注入仪器①中。 (5)定容 :将蒸馏水注入仪器至液面离刻度线1~2cm时,改用 (6)摇匀:盖好瓶塞 ,反复上下颠倒,然后静置。 |
| 思考与探究 | (1)实验步骤(3)、(4)中都要用到玻璃棒,其作用分别是搅拌、 (2)某同学在进行实验步骤(5)时,俯视向容器中滴加蒸馏水至刻度线,则该同学所配置溶液是浓度 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】硫酸亚铁铵晶体的化学式为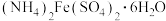 ,是常用的还原剂,实验室制备它的原理为
,是常用的还原剂,实验室制备它的原理为 .已知几种盐的溶解度(g)如下表所示:
.已知几种盐的溶解度(g)如下表所示:
回答下列问题:
(1)下列有关 的说法错误的是_______(填序号)。
的说法错误的是_______(填序号)。
(2)实验室制备硫酸亚铁铵晶体时,从混合液中获取该晶体的操作是_______ 、过滤、洗涤、干燥。
(3)若某次实验中需要使用480mL0.1mol/L硫酸亚铁铵溶液,则实验中需要称取_______ g硫酸亚铁铵晶体。配制时所用的水要先用蒸馏法处理,其目的是_______ 。若定容时仰视容量瓶刻度线,则所配溶液浓度_______ (填“偏高”或“偏低”)。
(4)取20mL所配溶液与足量NaOH溶液反应,将所得沉淀充分放置一段时间后过滤、洗涤、灼烧,最终可得到_______ g固体。
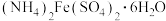 ,是常用的还原剂,实验室制备它的原理为
,是常用的还原剂,实验室制备它的原理为 .已知几种盐的溶解度(g)如下表所示:
.已知几种盐的溶解度(g)如下表所示:| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
 | 15.6 | 20.5 | 26.5 | 32.9 | 40.2 | 48.6 |
 | 70.6 | 73.0 | 75.4 | 78.0 | 81.63 | 84.4 |
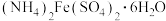 | 12.5 | 17.2 | 33.0 | 40.0 |
回答下列问题:
(1)下列有关
 的说法错误的是_______(填序号)。
的说法错误的是_______(填序号)。| A.是硫酸盐 | B.是铁盐 | C.是含氧酸盐 | D.是可溶性盐 |
(3)若某次实验中需要使用480mL0.1mol/L硫酸亚铁铵溶液,则实验中需要称取
(4)取20mL所配溶液与足量NaOH溶液反应,将所得沉淀充分放置一段时间后过滤、洗涤、灼烧,最终可得到
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】化学与人类生活密切相关。现有以下物质:
A. NaHCO3 B. Fe(OH)3 胶体 C. 冰醋酸(固态醋酸) D. 葡萄糖(C6H12O6) E.明矾 F. ClO2 G. Cu H.浓硫酸。
请回答下列问题:
(1)①以上物质中属于电解质的是___________ ; 属于非电解质的是___________ 。 (填字母序号)
②A在水溶液中的电离方程式为___________ 。
(2)葡萄糖注射液标签上的部分内容如图所示:
该注射液中葡萄糖的物质的量浓度为___________ mol/L。(保留两位小数)
(3)实验室用浓硫酸配制500mL lmol/L的H2SO4溶液。配制时必需的玻璃仪器有:烧杯、量筒、玻璃棒、___________ 、___________ 。 定容时仰视刻度线会导致溶液浓度___________ (填 “偏高”“偏低”或“无影响”)。
(4)下列事实与浓硫酸表现出的性质(括号中)对应关系正确的是________
A. NaHCO3 B. Fe(OH)3 胶体 C. 冰醋酸(固态醋酸) D. 葡萄糖(C6H12O6) E.明矾 F. ClO2 G. Cu H.浓硫酸。
请回答下列问题:
(1)①以上物质中属于电解质的是
②A在水溶液中的电离方程式为
(2)葡萄糖注射液标签上的部分内容如图所示:
| 5%葡萄糖注射液 [性状]本品为无色透明溶液。甜味。 [规格] 1000mL: 50g |
(3)实验室用浓硫酸配制500mL lmol/L的H2SO4溶液。配制时必需的玻璃仪器有:烧杯、量筒、玻璃棒、
(4)下列事实与浓硫酸表现出的性质(括号中)对应关系正确的是________
| A.在空气中敞口久置的浓硫酸,溶液质量增大(难挥发性) |
| B.浓硫酸与铜在加热条件下反应生成SO2(酸性和强氧化性) |
| C.蔗糖与浓硫酸反应中有海绵状的炭生成(吸水性) |
| D.浓硫酸与少量胆矾晶体混合,晶体由蓝色变成白色(脱水性) |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】某同学帮助水质监测站配制240mL0.5mol∙L-1的NaOH溶液以备使用。
(1)完成该实验所需要的计量仪器除了托盘天平、量筒外,还需要_______ ;
(2)配制NaOH溶液的过程中涉及的一些关键步骤和操作如图所示(部分步骤未画出);
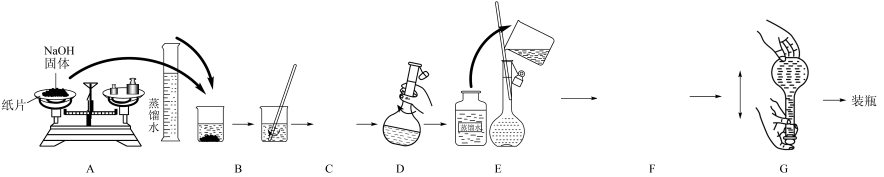
①步骤A简称为称量,该同学应称取_______ gNaOH固体。
②步骤C简称为移液,在此过程中,如果有少量液体溅出来,则所配制溶液的浓度会_______ (填“偏大”“偏小”或“无影响”);
③步骤F简称为_______ ,若操作过程中未洗涤烧杯和玻璃棒,所配制溶液的浓度会_______ (填“偏大”“偏小”或“无影响”);
④步骤G简称为摇匀,摇匀后发现溶液的凹液面低于刻度线,则所配制溶液的浓度会_______ (填“偏大”“偏小”或“无影响”);
(3)若要配制与NaOH溶液的物质的量浓度相等的100mL盐酸,则需要量取_______ mL质量分数为20%、密度为1.098g∙mL-1的盐酸(计算结果保留2位有效数字)。
(1)完成该实验所需要的计量仪器除了托盘天平、量筒外,还需要
(2)配制NaOH溶液的过程中涉及的一些关键步骤和操作如图所示(部分步骤未画出);

①步骤A简称为称量,该同学应称取
②步骤C简称为移液,在此过程中,如果有少量液体溅出来,则所配制溶液的浓度会
③步骤F简称为
④步骤G简称为摇匀,摇匀后发现溶液的凹液面低于刻度线,则所配制溶液的浓度会
(3)若要配制与NaOH溶液的物质的量浓度相等的100mL盐酸,则需要量取
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】实验室现在需要配制480mL2.0mol/L的NaOH溶液,请回答下列问题:
(1)除烧杯、玻璃棒以外,还需用到的玻璃仪器有_____ 、_____ 。若用固体NaOH配置,则需用托盘天平称取NaOH的质量_____ g。
(2)若用10mol/LNaOH的浓溶液来配置,则使用量筒量取该溶液的体积为_____ mL。
(3)容量瓶上标有以下五项中的_____ 。(填序号)
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(4)浓溶液稀释法中配制NaOH过程中下列操作导致所配浓度:(填偏高、偏低或不变)
A.定容时仰视刻度线_____ ;
B.容量瓶使用前没有干燥_____ 。
(1)除烧杯、玻璃棒以外,还需用到的玻璃仪器有
(2)若用10mol/LNaOH的浓溶液来配置,则使用量筒量取该溶液的体积为
(3)容量瓶上标有以下五项中的
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(4)浓溶液稀释法中配制NaOH过程中下列操作导致所配浓度:(填偏高、偏低或不变)
A.定容时仰视刻度线
B.容量瓶使用前没有干燥
您最近一年使用:0次

 的
的 溶液500mL,有以下仪器:①烧杯②100mL量筒③1000mL容量瓶④500mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)⑦药匙。
溶液500mL,有以下仪器:①烧杯②100mL量筒③1000mL容量瓶④500mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)⑦药匙。

