【变式探究】在一定温度下,某饱和氢氧化钠溶液体积为V mL,溶液密度为d g·cm-3,质量分数为w,物质的量浓度为c mol·L-1,溶液中含氢氧化钠的质量为m g,该温度下NaOH的溶解度为S。
(1)用w来表示该温度下氢氧化钠的溶解度(S)为________ 。
(2)用m、V表示溶液中溶质的物质的量浓度(c)为________ 。
(3)用S表示溶液中溶质的质量分数(w)为________ 。
(1)用w来表示该温度下氢氧化钠的溶解度(S)为
(2)用m、V表示溶液中溶质的物质的量浓度(c)为
(3)用S表示溶液中溶质的质量分数(w)为
2019高三·全国·专题练习 查看更多[1]
(已下线)2019高考备考一轮复习精品资料 第一章 从实验学化学 第2讲 物质的量浓度及一定物质的量浓度溶液的配制
更新时间:2018-09-12 13:54:10
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】向体积均为10 mL且物质的量浓度相同的两份NaOH溶液中分别通入一定量的CO2,得到溶液甲和乙。向甲、乙两溶液中分别滴加0.1mol/L盐酸。此时反应生成CO2体积(标准状况)与所加盐酸体积间的关系如图所示。

请回答下列问题:
(1)乙溶液中含有的溶质是___________ 。
(2)当0<V(HCl)<10mL时,甲溶液中发生反应的离子方程式为:___________ 。
(3)原NaOH溶液的物质的量浓度为___________ mol/L。

请回答下列问题:
(1)乙溶液中含有的溶质是
(2)当0<V(HCl)<10mL时,甲溶液中发生反应的离子方程式为:
(3)原NaOH溶液的物质的量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】NA为阿伏加德罗常数,下列对0.3 K2SO4溶液的说法中,正确的是
K2SO4溶液的说法中,正确的是_______ 。
A.1L溶液中含0.3NA个K+
B.1L溶液中含0.9NA个离子
C.2L溶液中K+浓度是1.2mol/L
D.2L溶液中含0.6NA个离子
E.该溶液就是将52.2g的K2SO4溶于1L水中所得到的溶液
F.K+的浓度是SO 的2倍
的2倍
G.溶液中含0.6 个K+
个K+
 K2SO4溶液的说法中,正确的是
K2SO4溶液的说法中,正确的是A.1L溶液中含0.3NA个K+
B.1L溶液中含0.9NA个离子
C.2L溶液中K+浓度是1.2mol/L
D.2L溶液中含0.6NA个离子
E.该溶液就是将52.2g的K2SO4溶于1L水中所得到的溶液
F.K+的浓度是SO
 的2倍
的2倍G.溶液中含0.6
 个K+
个K+
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】28.5g氯化镁的物质的量是_______________ ,其中Cl-的个数为_______ ,它与__________ 克食盐含有相同量的Cl-,将该氯化镁溶于水配成的500mL溶液中Cl—浓度是______ ,写出氯化镁的电离方程式_________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知反应:2SO2+O2 2SO3,4molSO2和2molO2在2L的密闭容器中反应2min后,SO2的物质的量浓度为1.5mol/L,求SO2、O2、SO3的反应速率
2SO3,4molSO2和2molO2在2L的密闭容器中反应2min后,SO2的物质的量浓度为1.5mol/L,求SO2、O2、SO3的反应速率____ 、____ 、____ 。
 2SO3,4molSO2和2molO2在2L的密闭容器中反应2min后,SO2的物质的量浓度为1.5mol/L,求SO2、O2、SO3的反应速率
2SO3,4molSO2和2molO2在2L的密闭容器中反应2min后,SO2的物质的量浓度为1.5mol/L,求SO2、O2、SO3的反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)标准状况下,5.6LCO物质的量是______ ,质量______ 。相同质量的CO和CO2所含原子个数比是_____ 。20gNaOH溶于水得到0.5升溶液其物质的量浓度为______ mol•L-1。
(2)NH4NO3是______ (填电解质或非电解质),写出硫酸铁的电离方程式______ 。
(3)写出将碳酸氢钠溶液与稀盐酸混合,反应的离子方程式为______ ;向氯化亚铁溶液中通入氯气的离子方程式是______ 。
(4)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式(未配平)表示为:
_______ClO-+_______Fe3++_______OH-=_______FeO +_______Cl-+_______H2O
+_______Cl-+_______H2O
请配平上述反应方程式______ ;上述反应中氧化剂是______ ,还原剂是______ 。
(1)标准状况下,5.6LCO物质的量是
(2)NH4NO3是
(3)写出将碳酸氢钠溶液与稀盐酸混合,反应的离子方程式为
(4)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式(未配平)表示为:
_______ClO-+_______Fe3++_______OH-=_______FeO
 +_______Cl-+_______H2O
+_______Cl-+_______H2O请配平上述反应方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】鲜花中加入“鲜花营养液”,能延长鲜花的寿命。某同学配的“鲜花营养液”成分表如下:
(1)配置此“鲜花营养液”500mL,准确称取所需的各成分,其中高锰酸钾固体的质量为______ g(结果保留3位小数)
(2)称量好后,进行如下实验步骤,A-F正确的实验次序为______ (填字母)。
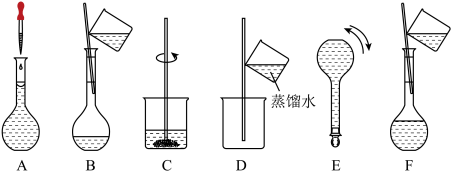
(3)定容时的操作:当液面离容量瓶颈部的刻度线______ 时,___
(4)配制过程中若出现下列情况,会造成溶液浓度偏低的是___
a.配制前容量瓶中有少量蒸馏水残留
b.进行上述步骤A操作时,仰视刻度线
c.进行上述步骤B操作时,烧杯中的溶液不慎洒到容量瓶外
d.进行上述步骤E操作后,发现液面低于刻度线,又加水至刻度线
| 成分 | 蔗糖 | 硫酸钾 | 阿司匹林 | 高锰酸钾 | 硫酸镁 |
| 物质的量浓度(mol/L) | 0.005 | 0.001 | 0.001 | 0.002 | 0.002 |
(1)配置此“鲜花营养液”500mL,准确称取所需的各成分,其中高锰酸钾固体的质量为
(2)称量好后,进行如下实验步骤,A-F正确的实验次序为

(3)定容时的操作:当液面离容量瓶颈部的刻度线
(4)配制过程中若出现下列情况,会造成溶液浓度偏低的是
a.配制前容量瓶中有少量蒸馏水残留
b.进行上述步骤A操作时,仰视刻度线
c.进行上述步骤B操作时,烧杯中的溶液不慎洒到容量瓶外
d.进行上述步骤E操作后,发现液面低于刻度线,又加水至刻度线
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题:
(1)含1.0molFe3+的Fe2(SO4)3中所含SO 的物质的量是
的物质的量是______ 。
(2)等质量的N2、NH3、NO2、Cl2四种气体中,在相同温度和压强下,体积最大的是______ 。
(3)某混合溶液中含有Na+、Al3+、Cl-、SO ,测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO
,测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO 的微粒个数比为
的微粒个数比为______ 。
(4)实验室常用KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O制取少量氯气。若转移电子数目为NA,则产生Cl2的体积为______ (标准状况),被氧化的HCl的物质的量为______ 。
(5)黑火药是我国古代四大发明之一,其化学反应方程式为:S+2KNO3+3C=K2S+3CO2↑+N2↑。
①上述反应所涉及到的物质中属于非电解质的是_____ 。
②上述反应中被氧化的元素是_____ (填元素符号);氧化剂是______ (填化学式)。
③收集上述反应生成的气体0.4mol,通入100mL4mol•L-1的氢氧化钠溶液中,最终所得溶液中的溶质是______ (填化学式)。
(6)我国古代常用绿矾FeSO4•7H2O来制备硫酸,若将绿矾投入到稀硝酸中,发生反应的离子方程式为______ 。
(1)含1.0molFe3+的Fe2(SO4)3中所含SO
 的物质的量是
的物质的量是(2)等质量的N2、NH3、NO2、Cl2四种气体中,在相同温度和压强下,体积最大的是
(3)某混合溶液中含有Na+、Al3+、Cl-、SO
 ,测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO
,测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO 的微粒个数比为
的微粒个数比为(4)实验室常用KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O制取少量氯气。若转移电子数目为NA,则产生Cl2的体积为
(5)黑火药是我国古代四大发明之一,其化学反应方程式为:S+2KNO3+3C=K2S+3CO2↑+N2↑。
①上述反应所涉及到的物质中属于非电解质的是
②上述反应中被氧化的元素是
③收集上述反应生成的气体0.4mol,通入100mL4mol•L-1的氢氧化钠溶液中,最终所得溶液中的溶质是
(6)我国古代常用绿矾FeSO4•7H2O来制备硫酸,若将绿矾投入到稀硝酸中,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按要求填空。
(1)与 具有相同电子数且含两种元素的阴离子的符号为
具有相同电子数且含两种元素的阴离子的符号为______ 。
(2)某元素的一种同位素X的质量数为A,含N个中子,它与 原子组成
原子组成 分子。在a克
分子。在a克 中所含质子的物质的量是
中所含质子的物质的量是______ mol。
(3)10.8g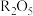 中氧原子的数目为
中氧原子的数目为 ,则元素R的相对原子质量为
,则元素R的相对原子质量为______ 。
(4)由CO、 两气体组成的混合气体12.8g,标况下,体积为8.96L,则CO和
两气体组成的混合气体12.8g,标况下,体积为8.96L,则CO和 的物质的量之比为
的物质的量之比为______ 。
(5) 和
和 的混合溶液,已知其中
的混合溶液,已知其中 物质的量浓度为
物质的量浓度为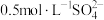 物质的量浓度为
物质的量浓度为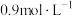 ,则
,则 的物质的量浓度为
的物质的量浓度为______  。
。
(6)体积相等的NaCl、 、
、 三种溶液,与等体积、等物质的量浓度的
三种溶液,与等体积、等物质的量浓度的 溶液均恰好完全反应,则NaCl、
溶液均恰好完全反应,则NaCl、 、
、 三种溶液的物质的量浓度之比为
三种溶液的物质的量浓度之比为______ 。
(7)等质量的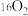 和
和 ,所含中子数之比为
,所含中子数之比为______ 。
(8)以下为中学化学中常见的几种物质:①液氨,②熔融KCl,③ 固体,④铜,⑤稀硫酸,⑥蔗糖,⑦澄清石灰水。请按下列分类标准回答问题。
固体,④铜,⑤稀硫酸,⑥蔗糖,⑦澄清石灰水。请按下列分类标准回答问题。
能导电的有______ (填写物质编号);属于电解质有______ (填写物质编号)
(9)如图是中学化学中常用于混合物分离和提纯的装置,请根据装置回答问题:
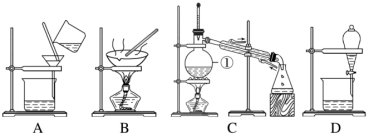
装置C中①的名称是______ ,在分液时,为使液体顺利滴下,应进行的具体操作是______ 。
(1)与
 具有相同电子数且含两种元素的阴离子的符号为
具有相同电子数且含两种元素的阴离子的符号为(2)某元素的一种同位素X的质量数为A,含N个中子,它与
 原子组成
原子组成 分子。在a克
分子。在a克 中所含质子的物质的量是
中所含质子的物质的量是(3)10.8g
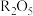 中氧原子的数目为
中氧原子的数目为 ,则元素R的相对原子质量为
,则元素R的相对原子质量为(4)由CO、
 两气体组成的混合气体12.8g,标况下,体积为8.96L,则CO和
两气体组成的混合气体12.8g,标况下,体积为8.96L,则CO和 的物质的量之比为
的物质的量之比为(5)
 和
和 的混合溶液,已知其中
的混合溶液,已知其中 物质的量浓度为
物质的量浓度为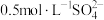 物质的量浓度为
物质的量浓度为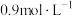 ,则
,则 的物质的量浓度为
的物质的量浓度为 。
。(6)体积相等的NaCl、
 、
、 三种溶液,与等体积、等物质的量浓度的
三种溶液,与等体积、等物质的量浓度的 溶液均恰好完全反应,则NaCl、
溶液均恰好完全反应,则NaCl、 、
、 三种溶液的物质的量浓度之比为
三种溶液的物质的量浓度之比为(7)等质量的
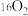 和
和 ,所含中子数之比为
,所含中子数之比为(8)以下为中学化学中常见的几种物质:①液氨,②熔融KCl,③
 固体,④铜,⑤稀硫酸,⑥蔗糖,⑦澄清石灰水。请按下列分类标准回答问题。
固体,④铜,⑤稀硫酸,⑥蔗糖,⑦澄清石灰水。请按下列分类标准回答问题。能导电的有
(9)如图是中学化学中常用于混合物分离和提纯的装置,请根据装置回答问题:

装置C中①的名称是
您最近一年使用:0次



