取10.6g Na2CO3溶于水配成100ml溶液,求:
(1)Na2CO3物质的量_______ 。
(2)Na2CO3溶液的物质的量浓度_______ 。
(3)取出20ml该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.4mol/L,求加入蒸馏水的体积(设稀释时,对溶液体积的影响忽略不计)_______ 。
(1)Na2CO3物质的量
(2)Na2CO3溶液的物质的量浓度
(3)取出20ml该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.4mol/L,求加入蒸馏水的体积(设稀释时,对溶液体积的影响忽略不计)
更新时间:2018-12-28 20:33:05
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)1molO3的质量为________ ,O2的摩尔质量为________ ,2molO3和3molO2的质量之比为_____ ,分子数之比为_____ ,同温同压下的密度之比为_____ .含氧原子数之比为_____ .
(2)10.6gNa2CO3溶于水配成500mL 溶液,物质的量浓度为_________ ,其中Na+的物质的量浓度为________ 。
(3)标准状况下11.2LHCl气体的物质的量为________ ,所含氢原子与________ g CH4中的氢原子数相同
(2)10.6gNa2CO3溶于水配成500mL 溶液,物质的量浓度为
(3)标准状况下11.2LHCl气体的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】请填写下表:
| 物质 | 摩尔质量 | 物质的量 | 质量 | 分子或离子数目 |
| SO 2 | | 2 mol | | |
| SO42- | | | | 6.02×10 23 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】计算。
(1)1.2RSO4中含0.01molR2+,则RSO4的摩尔质量是_______ ; 的相对原子质量约是
的相对原子质量约是_______ 。
(2)配制50mL0.2mol/LCuSO4溶液,需要CuSO4·5H2O_______ g。
(1)1.2RSO4中含0.01molR2+,则RSO4的摩尔质量是
 的相对原子质量约是
的相对原子质量约是(2)配制50mL0.2mol/LCuSO4溶液,需要CuSO4·5H2O
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】计算并填写下列空白
(1)1.8g水所含的分子的物质的量为______ mol,所含原子数与______ g氧气所含的原子数相同。
(2)标准状况下,22.4L的氯化氢气体溶于水中配成500mL溶液,则该溶液溶质的物质的量浓度______ 。
(3)气体A在标准状况下的密度为1.25g/L,则气体A的摩尔质量为________ 。若气体A为空气的主要成分,则气体A的化学式为_______ ;若气体A为有毒的双原子分子,则其化学式为____ 。
(1)1.8g水所含的分子的物质的量为
(2)标准状况下,22.4L的氯化氢气体溶于水中配成500mL溶液,则该溶液溶质的物质的量浓度
(3)气体A在标准状况下的密度为1.25g/L,则气体A的摩尔质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】按照要求回答下列问题。
(1)已知下列七种物质:①NaCl②Cu③SO2④氯化铁溶液⑤稀硫酸⑥硫酸钡⑦熔融KNO3,其中属于电解质的是____ 。
(2)工业中常将钠块加入正己烷中,除去微量的水,反应的化学方程式为____ ;若将23g钠与一定量的水发生上述反应,最终形成1L的溶液,其溶液的物质的量浓度为____ ,同时生成的气体在标准状况下的体积为____ 。
(3)利用焰色试验的原理既可制作五彩缤纷的节日烟花,也可定性鉴别某些金属盐,立德粉ZnS·BaSO4(也称锌钡白),是一种常用白色颜料。灼烧立德粉样品时,钡的焰色为____ 。
(4)工业废水中含有的重铬酸根离子(Cr2O )有毒,必须处理达标后才能排放,工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O
)有毒,必须处理达标后才能排放,工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O。
+14H+=6Fe3++2Cr3++7H2O。
①在该反应中还原产物是____ (填离子符号);
②用单线桥标出该反应电子转移的方向和数目____ 。
(1)已知下列七种物质:①NaCl②Cu③SO2④氯化铁溶液⑤稀硫酸⑥硫酸钡⑦熔融KNO3,其中属于电解质的是
(2)工业中常将钠块加入正己烷中,除去微量的水,反应的化学方程式为
(3)利用焰色试验的原理既可制作五彩缤纷的节日烟花,也可定性鉴别某些金属盐,立德粉ZnS·BaSO4(也称锌钡白),是一种常用白色颜料。灼烧立德粉样品时,钡的焰色为
| A.黄色 | B.砖红色 | C.紫色 | D.黄绿色 |
(4)工业废水中含有的重铬酸根离子(Cr2O
 )有毒,必须处理达标后才能排放,工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O
)有毒,必须处理达标后才能排放,工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O。
+14H+=6Fe3++2Cr3++7H2O。①在该反应中还原产物是
②用单线桥标出该反应电子转移的方向和数目
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】“84”消毒液能有效杀灭甲型H1N1病毒,某同学购买了一瓶某品牌“84”消毒液,仔细阅读瓶体标签并回答下列问题:

(1)该“84”消毒液的物质的量浓度为___________ mol·L-1。
(2)取任意体积“84”消毒液,下列物理量不随所取体积的多少而变化的是___________ (填字母)。若取出10mL溶液加水稀释100倍,稀释前后保持不变的是___________ (填字母)。
A.溶液中NaClO的物质的量
B.溶液中Na+的浓度
C.溶液中H2O分子的数目
D.溶液的密度
(3)某学生参阅标签,欲使用固体NaClO和蒸馏水配制480mL该品牌“84”消毒液。下列说法正确的是___________ (填字母)。
A.该同学应选用480mL的容量瓶配制溶液
B.容量瓶用蒸馏水洗净后,未烘干就用于配制溶液,会导致浓度偏低
C.定容时,加水超过刻度线,应立即用胶头滴管将多余的液体吸出
D.配制过程中,未洗涤烧杯和玻璃棒,会导致浓度偏低

(1)该“84”消毒液的物质的量浓度为
(2)取任意体积“84”消毒液,下列物理量不随所取体积的多少而变化的是
A.溶液中NaClO的物质的量
B.溶液中Na+的浓度
C.溶液中H2O分子的数目
D.溶液的密度
(3)某学生参阅标签,欲使用固体NaClO和蒸馏水配制480mL该品牌“84”消毒液。下列说法正确的是
A.该同学应选用480mL的容量瓶配制溶液
B.容量瓶用蒸馏水洗净后,未烘干就用于配制溶液,会导致浓度偏低
C.定容时,加水超过刻度线,应立即用胶头滴管将多余的液体吸出
D.配制过程中,未洗涤烧杯和玻璃棒,会导致浓度偏低
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】按要求填写下列空格(设阿伏加德罗常数的值为NA)
(1)在标准状况下,0.5molO2的体积为_______ L;
(2)某2LMgCl2溶液中含有4molCl-,MgCl2溶液的物质的量浓度为_______ mol/L;
(3)在标准状况下,44.8L的氢气质量为_______ g;
(4)39gNa2O2中的Na+数目为_______ NA。
(1)在标准状况下,0.5molO2的体积为
(2)某2LMgCl2溶液中含有4molCl-,MgCl2溶液的物质的量浓度为
(3)在标准状况下,44.8L的氢气质量为
(4)39gNa2O2中的Na+数目为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题:
(1)含1.0molFe3+的Fe2(SO4)3中所含SO 的物质的量是
的物质的量是______ 。
(2)等质量的N2、NH3、NO2、Cl2四种气体中,在相同温度和压强下,体积最大的是______ 。
(3)某混合溶液中含有Na+、Al3+、Cl-、SO ,测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO
,测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO 的微粒个数比为
的微粒个数比为______ 。
(4)实验室常用KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O制取少量氯气。若转移电子数目为NA,则产生Cl2的体积为______ (标准状况),被氧化的HCl的物质的量为______ 。
(5)黑火药是我国古代四大发明之一,其化学反应方程式为:S+2KNO3+3C=K2S+3CO2↑+N2↑。
①上述反应所涉及到的物质中属于非电解质的是_____ 。
②上述反应中被氧化的元素是_____ (填元素符号);氧化剂是______ (填化学式)。
③收集上述反应生成的气体0.4mol,通入100mL4mol•L-1的氢氧化钠溶液中,最终所得溶液中的溶质是______ (填化学式)。
(6)我国古代常用绿矾FeSO4•7H2O来制备硫酸,若将绿矾投入到稀硝酸中,发生反应的离子方程式为______ 。
(1)含1.0molFe3+的Fe2(SO4)3中所含SO
 的物质的量是
的物质的量是(2)等质量的N2、NH3、NO2、Cl2四种气体中,在相同温度和压强下,体积最大的是
(3)某混合溶液中含有Na+、Al3+、Cl-、SO
 ,测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO
,测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO 的微粒个数比为
的微粒个数比为(4)实验室常用KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O制取少量氯气。若转移电子数目为NA,则产生Cl2的体积为
(5)黑火药是我国古代四大发明之一,其化学反应方程式为:S+2KNO3+3C=K2S+3CO2↑+N2↑。
①上述反应所涉及到的物质中属于非电解质的是
②上述反应中被氧化的元素是
③收集上述反应生成的气体0.4mol,通入100mL4mol•L-1的氢氧化钠溶液中,最终所得溶液中的溶质是
(6)我国古代常用绿矾FeSO4•7H2O来制备硫酸,若将绿矾投入到稀硝酸中,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】100g 12mol/L(密度为1.19g/mL)的盐酸用100g水稀释后,其物质的量浓度_______ (填“大于”、“等于”或“小于”)6mol/L。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】化学计量在化学知识体系中占有重要地位,请回答下列问题。
(1)标准状况下,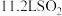 的物质的量是
的物质的量是___________ ,质量是___________ g。
(2)同温同压下,质量相等的 、
、 、
、 、
、 四种气体中,含有分子数目最多的是
四种气体中,含有分子数目最多的是___________ ,密度最大的是___________ 。
(3) 中含有的
中含有的 为
为 ,则X的摩尔质量为
,则X的摩尔质量为___________ 。
(4) 的盐酸与
的盐酸与 铁屑反应,参与反应的
铁屑反应,参与反应的 物质的量为
物质的量为___________ ,生成的 在标准状况下的体积为
在标准状况下的体积为___________ L。
(5)现有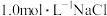 溶液
溶液 ,若取
,若取 该溶液用水稀释到
该溶液用水稀释到 ,所得溶液的
,所得溶液的 的物质的量浓度为
的物质的量浓度为___________ 。
(1)标准状况下,
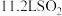 的物质的量是
的物质的量是(2)同温同压下,质量相等的
 、
、 、
、 、
、 四种气体中,含有分子数目最多的是
四种气体中,含有分子数目最多的是(3)
 中含有的
中含有的 为
为 ,则X的摩尔质量为
,则X的摩尔质量为(4)
 的盐酸与
的盐酸与 铁屑反应,参与反应的
铁屑反应,参与反应的 物质的量为
物质的量为 在标准状况下的体积为
在标准状况下的体积为(5)现有
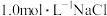 溶液
溶液 ,若取
,若取 该溶液用水稀释到
该溶液用水稀释到 ,所得溶液的
,所得溶液的 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】(1)当SO2、SO3的分子个数之比为1∶1时,原子总数之比为________ ,质量之比为________ 。
(2)中和含0.2 mol HCl的稀盐酸,需NaOH的质量为________ g。
(3)将5 mol·L-1的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO 的物质的量浓度是
的物质的量浓度是______ mol·L-1。
(4)用等体积的0.1 mol·L-1的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液中的SO 都恰好完全沉淀,则三种硫酸盐的物质的量浓度之比为
都恰好完全沉淀,则三种硫酸盐的物质的量浓度之比为________ 。
(2)中和含0.2 mol HCl的稀盐酸,需NaOH的质量为
(3)将5 mol·L-1的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO
 的物质的量浓度是
的物质的量浓度是(4)用等体积的0.1 mol·L-1的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液中的SO
 都恰好完全沉淀,则三种硫酸盐的物质的量浓度之比为
都恰好完全沉淀,则三种硫酸盐的物质的量浓度之比为
您最近一年使用:0次

 含杂质
含杂质 的大理石(杂质与盐酸不反应)投入
的大理石(杂质与盐酸不反应)投入

