某小组利用氯酸钾与10mol/L盐酸反应制氯气并进行氯气性质的探究,实验装置如图所示:
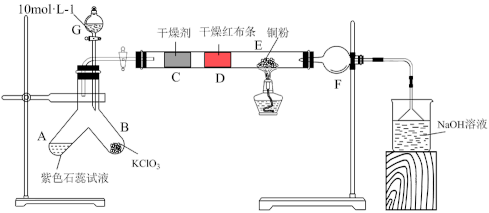
请回答:
(1)玻璃仪器G的名称是___________ 。
(2)E中实验现象是___________ 。
(3)根据相关实验现象就可以证明起漂白作用的不是氯气而是次氯酸,相关现象是___________ 。
(4)现要配制240mL 10mol/L所需盐酸,请回答下列问题:
①所用的仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要的仪器是___________ 。
②配制好的盐酸放入试剂瓶中后,需要贴上标签,请你在下图标签上填好所配溶液的信息。___________

③配制过程中有下列实验操作步骤,其正确的顺序为___________ 。
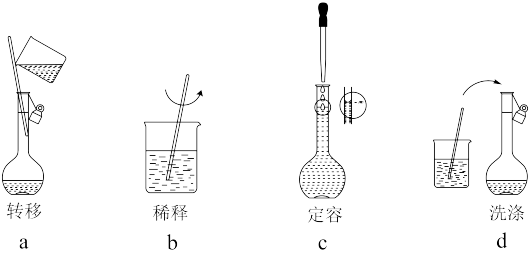
④下列操作会使配制结果偏高的是___________ 。
A. 容量瓶洗净后未干燥直接用来配制溶液
B. 反复摇匀后发现液面低于刻度线,继续加水至刻度线
C. 定容时俯视读数
D. 用量筒量取浓盐酸配制所需盐酸时,量筒仰视读数

请回答:
(1)玻璃仪器G的名称是
(2)E中实验现象是
(3)根据相关实验现象就可以证明起漂白作用的不是氯气而是次氯酸,相关现象是
(4)现要配制240mL 10mol/L所需盐酸,请回答下列问题:
①所用的仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要的仪器是
②配制好的盐酸放入试剂瓶中后,需要贴上标签,请你在下图标签上填好所配溶液的信息。

③配制过程中有下列实验操作步骤,其正确的顺序为

④下列操作会使配制结果偏高的是
A. 容量瓶洗净后未干燥直接用来配制溶液
B. 反复摇匀后发现液面低于刻度线,继续加水至刻度线
C. 定容时俯视读数
D. 用量筒量取浓盐酸配制所需盐酸时,量筒仰视读数
更新时间:2021-11-10 12:13:29
|
【知识点】 氯气的化学性质
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】硫酰氯(SO2Cl2)是一种重要的化工试剂,氯化法是合成硫酰氯(SO2Cl2)的常用方法。实验室合成硫酰氯的实验装置如图所示(部分夹持装置未画出):
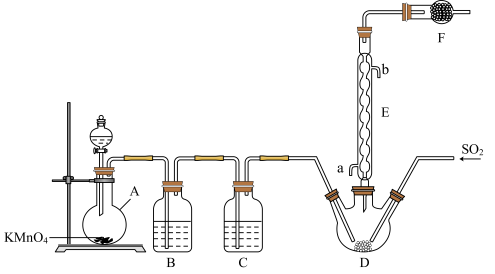
已知:①SO2(g)+Cl2(g)=SO2Cl2(l) ΔH=-97.3 kJ/mol。②硫酰氯常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”。③100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气。回答下列问题:
(1)A仪器的名称为_____ ,将分液漏斗中的浓盐酸加入A中发生反应的离子方程式为_____ 。
(2)装置B中的除杂试剂为_______ (填名称),若缺少装置C,会导致装置D中SO2与Cl2还可能发生反应的化学方程式为_______ 。
(3)E中冷凝水的的出口是_______ (填“a”或“b”),F的作用是______ 。
(4)当装置A中排出氯气1.12 L(已折算成标准状况)时,最终得到4.05g纯净的硫酰氯,则硫酰氯的产率为_______ 。长期存放的硫酰氯会发黄,其原因可能是_____ 。

已知:①SO2(g)+Cl2(g)=SO2Cl2(l) ΔH=-97.3 kJ/mol。②硫酰氯常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”。③100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气。回答下列问题:
(1)A仪器的名称为
(2)装置B中的除杂试剂为
(3)E中冷凝水的的出口是
(4)当装置A中排出氯气1.12 L(已折算成标准状况)时,最终得到4.05g纯净的硫酰氯,则硫酰氯的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某学生利用如图装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
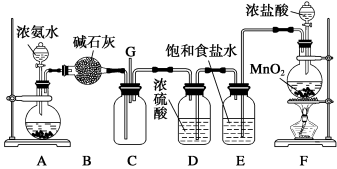
请回答下列问题:
(1)实验室利用固固反应制取氨气的化学方程式为_______
(2)装置A中的烧瓶内固体不可以选用
(3)装置F中发生反应的离子方程式是_______
(4)B装置的作用_______ ;E装置的作用_______
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式:_______
(6)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,可以将尾气通入盛有_______ 溶液的烧杯来处理。

请回答下列问题:
(1)实验室利用固固反应制取氨气的化学方程式为
(2)装置A中的烧瓶内固体不可以选用
| A.生石灰 | B.碱石灰 | C.五氧化二磷 | D.烧碱 |
(4)B装置的作用
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式:
(6)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,可以将尾气通入盛有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室里除了用二氧化笽和浓盐酸加热制取氯气,也可以在常温下利用反应: 制取并收集纯净、干燥的氯气,装置如图所示:
制取并收集纯净、干燥的氯气,装置如图所示:

(1)装置A中盛放浓盐酸的仪器名称是___________ ,该装置相比普通分液漏斗的优点是___________ 。
(2)装置B的作用是___________ ,装置E中发生反应的化学方程式是___________ 。
(3)在该反应中,被还原的元素是___________ ,若产生 ,则转移的电子数目为
,则转移的电子数目为___________ 。
(4)为进一步探究氯气是否具有漂白性,进行了如下实验

将干燥的氯气依次通过盛有干燥红纸条的集气瓶和湿润红纸条的集气瓶,可观察到的现象是___________ 。结合化学方程式和适当的文字解释原因:___________ 。
 制取并收集纯净、干燥的氯气,装置如图所示:
制取并收集纯净、干燥的氯气,装置如图所示:
(1)装置A中盛放浓盐酸的仪器名称是
(2)装置B的作用是
(3)在该反应中,被还原的元素是
 ,则转移的电子数目为
,则转移的电子数目为(4)为进一步探究氯气是否具有漂白性,进行了如下实验

将干燥的氯气依次通过盛有干燥红纸条的集气瓶和湿润红纸条的集气瓶,可观察到的现象是
您最近一年使用:0次



