按要求写出下列方程式。
(1)实验室(舍勒法)制氯气的离子方程式:___________ 。
(2)碳酸钙溶于醋酸的离子方程式:___________ 。
(3) 胶体制备的离子方程式:
胶体制备的离子方程式:___________ 。
(4)工业制漂白粉的化学方程式:___________ 。
(5)向 溶液滴加
溶液滴加 溶液至
溶液至 时的离子方程式:
时的离子方程式:___________ 。
(1)实验室(舍勒法)制氯气的离子方程式:
(2)碳酸钙溶于醋酸的离子方程式:
(3)
 胶体制备的离子方程式:
胶体制备的离子方程式:(4)工业制漂白粉的化学方程式:
(5)向
 溶液滴加
溶液滴加 溶液至
溶液至 时的离子方程式:
时的离子方程式:
更新时间:2021-11-10 18:50:32
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】Fe2O3又称铁红,请根据要求完成下列问题。
(1)Fe2O3固体(红棕色)属于___________ (填“纯净物”或者“混合物”)。将其加入适量盐酸。反应的化学方程式:___________ 。
(2)用上述所得溶液进行下列实验:取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀产生,反应的离子方程式:___________ 。
(3)在100mL小烧杯中加入20mL蒸馏水,加热至沸腾后。向烧杯中加入几滴FeCl3溶液,继续煮沸至出现___________ 色,即可制得Fe(OH)3胶体。其分散质的微粒直径大小在___________ 之间。
(4)另取一个100mL小烧杯也加入20mL蒸馏水,向烧杯中加入1 mLFeCl3溶液,振荡摇匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置干暗处,分别用激光笔照射烧杯中的液体,可以看到___________ 烧杯的液体中产生了丁达尔效应。
(1)Fe2O3固体(红棕色)属于
(2)用上述所得溶液进行下列实验:取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀产生,反应的离子方程式:
(3)在100mL小烧杯中加入20mL蒸馏水,加热至沸腾后。向烧杯中加入几滴FeCl3溶液,继续煮沸至出现
(4)另取一个100mL小烧杯也加入20mL蒸馏水,向烧杯中加入1 mLFeCl3溶液,振荡摇匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置干暗处,分别用激光笔照射烧杯中的液体,可以看到
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】“皮鞋很忙”的恶搞段子曾经风靡网络,揭露了某些行业用烂皮鞋制造酸奶或毒胶囊的不法行为。央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知Fe(CrO2)2中铁元素是+2价,则其中铬元素是_______ 价。
(2)明胶的水溶液和K2SO4溶液共同具备的性质是_______ (填序号)。
a.都不稳定,密封放置沉淀 b.分散质粒子可通过滤纸 c.丁达尔效应
(3)制备Fe(OH)3胶体的离子方程式_______ 。
(4)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的方法是_______ ,装置是下列中的_______ (填序号)。

(5)现有10 mL明胶的水溶液与5 mL Na2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明SO 能够透过半透膜:
能够透过半透膜:_______ 。
(1)已知Fe(CrO2)2中铁元素是+2价,则其中铬元素是
(2)明胶的水溶液和K2SO4溶液共同具备的性质是
a.都不稳定,密封放置沉淀 b.分散质粒子可通过滤纸 c.丁达尔效应
(3)制备Fe(OH)3胶体的离子方程式
(4)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的方法是

(5)现有10 mL明胶的水溶液与5 mL Na2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明SO
 能够透过半透膜:
能够透过半透膜:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】现有甲、乙、丙三名同学分别进行 Fe(OH)3胶体的制备实验。
甲同学:向 FeCl3溶液中加少量NaOH溶液。
乙同学:向40mL煮沸的蒸馏水中逐滴加入5~6滴 FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。
丙同学:直接加热饱和 FeCl3溶液。
(1)其中操作正确的同学是___________ ,反应的离子方程式为___________ 。
(2)证明有Fe(OH)3胶体生成的方法是___________ 。
(3)向Fe(OH)3胶体中逐滴加入稀硫酸至过量,过程中的现象是___________ 。
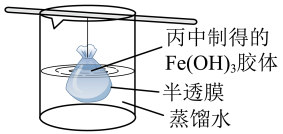
(4)可用如图所示的装置除去 Fe(OH)3胶体中的杂质离子来提纯 Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入AgNO3溶液,若___________ (填实验现象),则说明该Fe(OH)3胶体中的杂质离子已经完全除去。
甲同学:向 FeCl3溶液中加少量NaOH溶液。
乙同学:向40mL煮沸的蒸馏水中逐滴加入5~6滴 FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。
丙同学:直接加热饱和 FeCl3溶液。
(1)其中操作正确的同学是
(2)证明有Fe(OH)3胶体生成的方法是
(3)向Fe(OH)3胶体中逐滴加入稀硫酸至过量,过程中的现象是
(4)可用如图所示的装置除去 Fe(OH)3胶体中的杂质离子来提纯 Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入AgNO3溶液,若

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】燃料电池是一种化学电池,具有能量转化率高、对环境友好等优点。例如,氢氧燃料电池在工作时,从负极连续通入①H2,从正极连续通入②O2,二者在电池内部(含有③H2SO4或④KOH)的溶液中发生反应生成⑤H2O,同时产生电能。⑥CH4等也可以作为燃料电池的燃料。目前已研制成功⑦Al-⑧空气燃料电池,它可以代替⑨汽油为汽车提供动力,也可以用作照明电源等。
(1)在上述标有序号的物质中,属于混合物的是___________ (填序号,下同);属于氧化物的是___________ ;属于酸的是___________ ;属于碱的是___________ ;属于有机物的是___________ 。
(2)①、②和⑦三种物质,从类别来看,都属于___________ ﹔从基本反应类型看,它们两两之间能发生___________ 反应,从电子得失看,它们两两之间能发生___________ 反应。
(3)写出氢氧燃料电池产生电能时反应的化学方程式:___________ 。
写出③和④反应的离子方程式:___________ 。
写出③和⑦反应的化学方程式:___________ 。
(1)在上述标有序号的物质中,属于混合物的是
(2)①、②和⑦三种物质,从类别来看,都属于
(3)写出氢氧燃料电池产生电能时反应的化学方程式:
写出③和④反应的离子方程式:
写出③和⑦反应的化学方程式:
您最近一年使用:0次
【推荐2】回答下列问题。
Ⅰ. KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示为:2KClO3+4HCl(浓) =2KCl+2ClO2↑+Cl2↑+2H2O
(1)氧化剂是________ ,氧化产物是__________ 。生成一个Cl2分子转移电子数_____ 个。
(2)请将上述反应改写成离子方程式_______________ 。
(3)浓盐酸在反应中显示出来的性质是____________ (填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若产生71g Cl2,则被氧化的HCl为_________ g。
Ⅱ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(5)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是_____ (填化学式)。
(6)湿法制备高铁酸钾(Na2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、 、 Cl-、H2O。
、 Cl-、H2O。
①请依据上述信息,写出湿法制高铁酸钾的离子反应方程式(不需要配平):______________ 。
②每生成1个 转移
转移_________ 个电子。
Ⅰ. KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示为:2KClO3+4HCl(浓) =2KCl+2ClO2↑+Cl2↑+2H2O
(1)氧化剂是
(2)请将上述反应改写成离子方程式
(3)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若产生71g Cl2,则被氧化的HCl为
Ⅱ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(5)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是
(6)湿法制备高铁酸钾(Na2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、
 、 Cl-、H2O。
、 Cl-、H2O。①请依据上述信息,写出湿法制高铁酸钾的离子反应方程式(不需要配平):
②每生成1个
 转移
转移
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】填空
(1)在钢铁厂的生产中,炽热的铁水或者钢水注入模具之前,模具必须进行充分的干燥处理,不得留有水,原因是________ (用化学方程式表示)。
(2)由于Na2O2已与CO2、H2O发生反应放出氧气,因此可在呼吸面具或潜水艇中作为氧气的来源,写出Na2O2与H2O反应的化学方程式_________ 。
(3)将Cl2通入冷的石灰乳中,即制得以Ca(ClO)2为有效成分的漂白粉,写出对应的化学方程式________ 。
(4)配平化学方程式:Fe2++ +H+=Fe3++NO↑+H2O。
+H+=Fe3++NO↑+H2O。_______
(5)向一个铝制易拉罐中充满CO2,然后往罐中注入足量的浓NaOH溶液,立即用胶布封严罐口。一会儿听到罐内发出“咔、咔”的响声,且易拉罐变瘪,再过一会易拉罐又鼓起来恢复原样,写出变瘪的离子方程式___________ 。
(1)在钢铁厂的生产中,炽热的铁水或者钢水注入模具之前,模具必须进行充分的干燥处理,不得留有水,原因是
(2)由于Na2O2已与CO2、H2O发生反应放出氧气,因此可在呼吸面具或潜水艇中作为氧气的来源,写出Na2O2与H2O反应的化学方程式
(3)将Cl2通入冷的石灰乳中,即制得以Ca(ClO)2为有效成分的漂白粉,写出对应的化学方程式
(4)配平化学方程式:Fe2++
 +H+=Fe3++NO↑+H2O。
+H+=Fe3++NO↑+H2O。(5)向一个铝制易拉罐中充满CO2,然后往罐中注入足量的浓NaOH溶液,立即用胶布封严罐口。一会儿听到罐内发出“咔、咔”的响声,且易拉罐变瘪,再过一会易拉罐又鼓起来恢复原样,写出变瘪的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】按要求回答问题:
(1)漂白粉的有效成分:___________ (填化学式)。
(2)NaHCO3的电离方程式___________ 。
(3)实验室制取氯气的的离子方程式为___________ 。
(4)过氧化钠与二氧化碳反应的化学方程式为___________ 。
(1)漂白粉的有效成分:
(2)NaHCO3的电离方程式
(3)实验室制取氯气的的离子方程式为
(4)过氧化钠与二氧化碳反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)现有①Na2CO3溶液 ②液态氯化氢 ③CCl4④Cl2⑤熔融BaCl2回答下列问题:属于电解质的是 ___________ (填代号,下同);能导电的是___________ 属于共价化合物的是___________
(2)写出CCl4的结构式___________ 写出BaCl2的电子式___________
(3)由铜片、锌片和200mL稀硫酸组成的原电池中,则当铜片上共放出3.36L(标准状况)气体时,硫酸恰好全部作用完。写出正极的电极反应式:___________ 。有___________ mol电子通过了导线
(4)其实验室制备NH3的化学方程式__________ ,实验室制氯气的离子方程式 ___________
(2)写出CCl4的结构式
(3)由铜片、锌片和200mL稀硫酸组成的原电池中,则当铜片上共放出3.36L(标准状况)气体时,硫酸恰好全部作用完。写出正极的电极反应式:
(4)其实验室制备NH3的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】实验室制取、净化并收集氯气涉及以下几个主要阶段:

(1)实验室制取氯气的离子方程式为______ , 表示阿伏加德罗常数的值,若有
表示阿伏加德罗常数的值,若有 的
的 被氧化,则转移的电子总数为
被氧化,则转移的电子总数为______ ;将足量的 投入含
投入含 的浓盐酸中,充分加热,可生成的
的浓盐酸中,充分加热,可生成的
______ (填“>”“=”或“<”) 。
。
(2)现有3种试剂可供选择:A.饱和食盐水 B.浓硫酸 C. 溶液,则Y溶液应选用
溶液,则Y溶液应选用______ (填字母),X溶液的作用是______ 。
(3) 溶液用于尾气吸收,常温下发生反应的离子方程式为
溶液用于尾气吸收,常温下发生反应的离子方程式为______ 。

(1)实验室制取氯气的离子方程式为
 表示阿伏加德罗常数的值,若有
表示阿伏加德罗常数的值,若有 的
的 被氧化,则转移的电子总数为
被氧化,则转移的电子总数为 投入含
投入含 的浓盐酸中,充分加热,可生成的
的浓盐酸中,充分加热,可生成的
 。
。(2)现有3种试剂可供选择:A.饱和食盐水 B.浓硫酸 C.
 溶液,则Y溶液应选用
溶液,则Y溶液应选用(3)
 溶液用于尾气吸收,常温下发生反应的离子方程式为
溶液用于尾气吸收,常温下发生反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】按照题目的要求填空
(1)NaHSO4与NaHCO3反应的离子方程式:___________ 。
(2)向少量NaHCO3溶液中加入Ca(OH)2溶液反应的离子方程式:___________ 。
(3)未打磨过的铝条与NaOH反应的离子方程式:___________ 。
(4)工业制取漂白粉的化学方程式:___________ 。
(1)NaHSO4与NaHCO3反应的离子方程式:
(2)向少量NaHCO3溶液中加入Ca(OH)2溶液反应的离子方程式:
(3)未打磨过的铝条与NaOH反应的离子方程式:
(4)工业制取漂白粉的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】根据要求写出方程式
(1)写出铝与氢氧化钠溶液反应的离子方程式______________________________________ 。
(2)写出Na2O2和水反应的离子方程式____________________________________________ 。
(3)工业上制取漂白粉的反应化学方程式为________________________________________ 。
(4)向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边振荡,未得到白色沉淀的原因是发生了____ 反应。
(1)写出铝与氢氧化钠溶液反应的离子方程式
(2)写出Na2O2和水反应的离子方程式
(3)工业上制取漂白粉的反应化学方程式为
(4)向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边振荡,未得到白色沉淀的原因是发生了
您最近一年使用:0次



