按要求回答问题:
(1)漂白粉的有效成分:___________ (填化学式)。
(2)NaHCO3的电离方程式___________ 。
(3)实验室制取氯气的的离子方程式为___________ 。
(4)过氧化钠与二氧化碳反应的化学方程式为___________ 。
(1)漂白粉的有效成分:
(2)NaHCO3的电离方程式
(3)实验室制取氯气的的离子方程式为
(4)过氧化钠与二氧化碳反应的化学方程式为
更新时间:2024-01-30 08:27:33
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】写出下列电离方程式。
⑴NaHSO4加热融化___ ;
⑵高氯酸(HClO4)溶于水___ ;
⑶(NH4)Fe(SO4)2溶于水___ ;
⑷二元弱酸H2A溶于水__ 。
⑴NaHSO4加热融化
⑵高氯酸(HClO4)溶于水
⑶(NH4)Fe(SO4)2溶于水
⑷二元弱酸H2A溶于水
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)食盐水、食醋、澄清石灰水、小苏打中属于电解质的是________ ;
(2)请写出熟石灰的化学式________ ;
(3)请写出电解质的电离方程式________ 。
(4)试写出向食盐水中通入硝酸银溶液的化学方程式及离子方程式:________
(2)请写出熟石灰的化学式
(3)请写出电解质的电离方程式
(4)试写出向食盐水中通入硝酸银溶液的化学方程式及离子方程式:
您最近一年使用:0次
【推荐3】阅读下列科普短文并填空:
海水中含有多种盐类,如NaCl、MgSO4等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水用以生产NaOH、Na2CO3、Na、Cl2、盐酸等,经过氯气氧化,热空气吹出、SO2吸收等一系列操作可获得Br2。
(1)写出Na2CO3溶于水的电离方程式:____ 。
(2)海水提溴的过程中涉及的反应有
i.2Br-+Cl2=Br2+2Cl-
ii.2H2O+SO2+Br2=4H++2Br-+SO
①用双线桥法表示反应i中的电子转移方向和数目:____ 。
②ii中的氧化剂为:____ 。
③根据上述反应可判断Cl-、Br-、SO2的还原性由强到弱的顺序为____ 。
海水中含有多种盐类,如NaCl、MgSO4等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水用以生产NaOH、Na2CO3、Na、Cl2、盐酸等,经过氯气氧化,热空气吹出、SO2吸收等一系列操作可获得Br2。
(1)写出Na2CO3溶于水的电离方程式:
(2)海水提溴的过程中涉及的反应有
i.2Br-+Cl2=Br2+2Cl-
ii.2H2O+SO2+Br2=4H++2Br-+SO

①用双线桥法表示反应i中的电子转移方向和数目:
②ii中的氧化剂为:
③根据上述反应可判断Cl-、Br-、SO2的还原性由强到弱的顺序为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(一)1774年,瑞典化学家合勒在研究软锰矿(主要成分是 )的过程中,将其与浓盐酸混合加热,产生黄绿色气体
)的过程中,将其与浓盐酸混合加热,产生黄绿色气体 。
。
(1)上述反应的离子方程式为___________ 。
(2)若将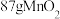 跟含
跟含 的浓盐酸混合加热,产生
的浓盐酸混合加热,产生 的体积小于
的体积小于 (标准状况下),其原因可能是
(标准状况下),其原因可能是___________ 。
(3)将 通入石灰乳中可制得漂白粉,有关反应的化学方程式为
通入石灰乳中可制得漂白粉,有关反应的化学方程式为___________ 。
(4)实验室制备氯气时验满的方法是___________ ,涉及的离子方程式为___________ 。
(二)钠、碳及它们的化合物在生产、生活中有着重要的用途。
(5)某汽车安全气囊的产气药剂主要含有 、
、 、
、 、
、 等物质。当汽车发生碰撞时,
等物质。当汽车发生碰撞时, 迅速分解产生
迅速分解产生 和
和 ,同时放出大量的热。
,同时放出大量的热。 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。
① 可处理产生的
可处理产生的 ,反应为
,反应为 ,该反应中若
,该反应中若 被氧化时,则
被氧化时,则 获得
获得___________  电子。
电子。
② 是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式是
是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式是___________
 )的过程中,将其与浓盐酸混合加热,产生黄绿色气体
)的过程中,将其与浓盐酸混合加热,产生黄绿色气体 。
。(1)上述反应的离子方程式为
(2)若将
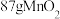 跟含
跟含 的浓盐酸混合加热,产生
的浓盐酸混合加热,产生 的体积小于
的体积小于 (标准状况下),其原因可能是
(标准状况下),其原因可能是(3)将
 通入石灰乳中可制得漂白粉,有关反应的化学方程式为
通入石灰乳中可制得漂白粉,有关反应的化学方程式为(4)实验室制备氯气时验满的方法是
(二)钠、碳及它们的化合物在生产、生活中有着重要的用途。
(5)某汽车安全气囊的产气药剂主要含有
 、
、 、
、 、
、 等物质。当汽车发生碰撞时,
等物质。当汽车发生碰撞时, 迅速分解产生
迅速分解产生 和
和 ,同时放出大量的热。
,同时放出大量的热。 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。①
 可处理产生的
可处理产生的 ,反应为
,反应为 ,该反应中若
,该反应中若 被氧化时,则
被氧化时,则 获得
获得 电子。
电子。②
 是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式是
是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】“分类研究”是重要的学习与科研方法,请用提供的物质答题。
a.蔗糖 b.氨水 c.C60 d.Fe e.SO2 f.金刚石 g.CaF2 h.熔融的Ba(OH)2 i.NaHCO3溶液 m.Ca(ClO)2晶体物质。
(1)上述物质属于电解质的是___________ ,属于同素异形体的是___________ ,不属于电解质但能导电的是___________ ,在水中不能电离出离子的化合物是___________ 。
(2)Ca(ClO)2是漂白粉的有效成分,其与空气中的___________ 反应而具有漂白能力,写出Ca(ClO)2电离方程式___________ 。
a.蔗糖 b.氨水 c.C60 d.Fe e.SO2 f.金刚石 g.CaF2 h.熔融的Ba(OH)2 i.NaHCO3溶液 m.Ca(ClO)2晶体物质。
(1)上述物质属于电解质的是
(2)Ca(ClO)2是漂白粉的有效成分,其与空气中的
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】禽流感病毒是一种没有超常抵抗力的病毒。研究证明,许多常用消毒药物如漂粉精、漂白粉、高锰酸钾等,可以将禽流感病毒杀灭。氯气与氢氧化钙充分反应,使次氯酸钙成为主要成分,得到漂粉精,其稳定性比漂白粉高。将漂粉精溶于适量水中,呈白色浊状物,静置沉降。取少许上层清液,滴加碳酸钠溶液出现白色沉淀,发生反应的离子方程式为___ 。另取少许上层清液,先滴加适量的____ (填化学式)酸化,再滴加_ (填化学式)溶液即可检验Cl-的存在,发生反应的离子方程式为___ 。再取少许上层清液,滴加几滴酚酞溶液,溶液呈红色,随后溶液迅速褪色,说明漂粉精溶液呈__ 性并具有___ 性。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】某同学利用如下实验装置制备少量的漂白粉。回答下列问题
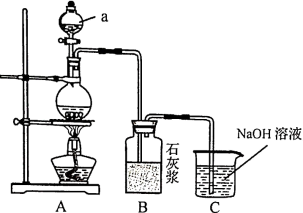
(1)漂白粉的有效成分是_______ (填化学式)。
(2)仪器a的名称是_______ ,利用二氧化锰和浓盐酸制取氯气的化学方程式为_______ 。
(3)装置B中反应放热会使体系温度升高,导致氯气和石灰浆发生副反应产生杂质Ca(ClO3)2,该副反应中氧化剂与还原剂的质量之比为_______ ;为防止该副反应发生,可采取的措施是_______ 。
(4)装置C的作用是_______ ,C中发生反应的离子方程式为_______ 。

(1)漂白粉的有效成分是
(2)仪器a的名称是
(3)装置B中反应放热会使体系温度升高,导致氯气和石灰浆发生副反应产生杂质Ca(ClO3)2,该副反应中氧化剂与还原剂的质量之比为
(4)装置C的作用是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】基础知识填空:
(1)酸雨的pH小于______ ;硅酸钠的水溶液俗称______ ;
(2)有以下物质:①Cu ②Al ③ C ④稀硫酸 ⑤浓硫酸 ⑥稀硝酸 ⑦浓硝酸。
加热条件下,①和④______ (填“能”或者“不能”)反应;
常温下,⑤和⑦可盛装在______ (选填①或②)容器中;
写出①与⑥反应的化学方程式______ ;
(3)实验室用MnO2与浓盐酸反应制氯气,在该反应中,氧化剂是______ ,如有1 mol Cl2生成,则被氧化的HCl的物质的量是______ mol,转移的电子数目为______ 。
(1)酸雨的pH小于
(2)有以下物质:①Cu ②Al ③ C ④稀硫酸 ⑤浓硫酸 ⑥稀硝酸 ⑦浓硝酸。
加热条件下,①和④
常温下,⑤和⑦可盛装在
写出①与⑥反应的化学方程式
(3)实验室用MnO2与浓盐酸反应制氯气,在该反应中,氧化剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】实验室要制取一瓶纯净干燥的氯气。现有如图所示仪器和药品可供使用:

(1)实验室制取氯气的原理:
其中HCl所表现的性质是
(2)接上述仪器的正确顺序是 。
| A.ABCEFGHD | B.ABCFEGHD | C.AFEBCGHD | D.AFEBCHGD |
A.除去氯气中的水蒸气 B.除去氯气中的氯化氢
C.尾气吸收 D.收集氯气
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】按照如图所示装置进行实验,填写有关现象及化学方程式。

已知:浓硫酸有吸水性,可用做干燥剂。
(1)A中发生反应的化学方程式为___________ 。
(2)B中浓硫酸的作用是___________ 。
(3)C中发生反应的化学方程式为___________ 。
(4)若D中把所有的 全部吸收干净,则E中收集的气体是
全部吸收干净,则E中收集的气体是___________ (填化学式)。

已知:浓硫酸有吸水性,可用做干燥剂。
(1)A中发生反应的化学方程式为
(2)B中浓硫酸的作用是
(3)C中发生反应的化学方程式为
(4)若D中把所有的
 全部吸收干净,则E中收集的气体是
全部吸收干净,则E中收集的气体是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】金属钠及其化合物在人类生产、生活中起着重要作用。诸回答下列问题:
(1)向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中加入黄豆粒大小的金属钠,可能观察到的现象是___________(填字母)。
过氧化钠是重要的化工原料,具有多种用途。
(2)过氧化钠是_____________ 色固体。
(3)过氧化钠可用作呼吸面具、潜水艇的供氧剂,写出 和
和 反应的化学方程式:
反应的化学方程式:__________________ ,消耗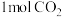 时,反应中转移的电子总数为
时,反应中转移的电子总数为__________ mol。
(4)某实验小组通过如图所示实验,探究 与水的反应,下列说法正确的是_________。
与水的反应,下列说法正确的是_________。
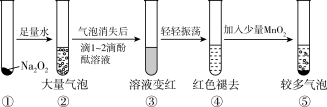
(5)向酸性 溶液中加入
溶液中加入 粉末,观察到溶液褪色,发生反应的离子方程式:
粉末,观察到溶液褪色,发生反应的离子方程式: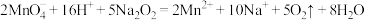
①比较氧化性强弱:
______  (选填“>”或“<”)。
(选填“>”或“<”)。
②该反应说明 具有
具有______ (选填“氧化性”或“还原性”)。
(1)向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中加入黄豆粒大小的金属钠,可能观察到的现象是___________(填字母)。
A.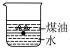 | B.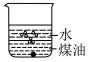 |
C.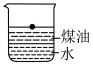 | D.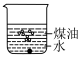 |
过氧化钠是重要的化工原料,具有多种用途。
(2)过氧化钠是
(3)过氧化钠可用作呼吸面具、潜水艇的供氧剂,写出
 和
和 反应的化学方程式:
反应的化学方程式: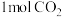 时,反应中转移的电子总数为
时,反应中转移的电子总数为(4)某实验小组通过如图所示实验,探究
 与水的反应,下列说法正确的是_________。
与水的反应,下列说法正确的是_________。
| A.②中的大量气泡主要成分是氢气 |
| B.③中溶液变红,说明有酸性物质生成 |
| C.④中现象可能是由于溶液中含有强氧化性物质造成的 |
D.⑤中 的主要作用是降低了水中氧气的溶解度 的主要作用是降低了水中氧气的溶解度 |
(5)向酸性
 溶液中加入
溶液中加入 粉末,观察到溶液褪色,发生反应的离子方程式:
粉末,观察到溶液褪色,发生反应的离子方程式: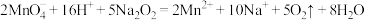
①比较氧化性强弱:

 (选填“>”或“<”)。
(选填“>”或“<”)。②该反应说明
 具有
具有
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】2022年11月30日,神舟十五号载人飞船与空间站组合体成功交会对接。飞船的轨道舱内安装盛有 颗粒装置,为宇航员供氧。回答下列问题:
颗粒装置,为宇航员供氧。回答下列问题:
(1)39g 中的阳离子的物质的量为
中的阳离子的物质的量为_______ 。
(2) 与
与 发生反应的化学方程式为
发生反应的化学方程式为_______ ,该反应中体现了 的性质有
的性质有_______ 。
(3) 是一种重要的工业原料,实验室需0.1mol/L的
是一种重要的工业原料,实验室需0.1mol/L的 溶液450mL,配制时应选用容量瓶的规格和称取
溶液450mL,配制时应选用容量瓶的规格和称取 的质量分别是
的质量分别是_______ (填字母)。
A.450mL,4.77g B.450mL,4.8g C.500mL,5.3g
 颗粒装置,为宇航员供氧。回答下列问题:
颗粒装置,为宇航员供氧。回答下列问题:(1)39g
 中的阳离子的物质的量为
中的阳离子的物质的量为(2)
 与
与 发生反应的化学方程式为
发生反应的化学方程式为 的性质有
的性质有(3)
 是一种重要的工业原料,实验室需0.1mol/L的
是一种重要的工业原料,实验室需0.1mol/L的 溶液450mL,配制时应选用容量瓶的规格和称取
溶液450mL,配制时应选用容量瓶的规格和称取 的质量分别是
的质量分别是A.450mL,4.77g B.450mL,4.8g C.500mL,5.3g
您最近一年使用:0次



