课题式研究性学习是培养学生创造性思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:
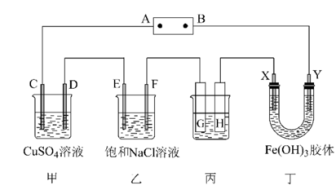
(1)电源A极的名称是___________ 。
(2)甲装置中在两极分别滴加紫色石蕊溶液,有现象的是___________ (填电极符号)。
(3)如果收集乙装置中产生的气体,两种气体的体积比是___________ 。
(4)欲用丙装置给铜镀银,G应该是___________ (填“铜”或“银”),电镀液的主要成分是___________ (填化学式)。
(5)若丙装置的两极产生气体的质量比为1∶8,则丙中的溶液可以为___________ (填化学式)。

(1)电源A极的名称是
(2)甲装置中在两极分别滴加紫色石蕊溶液,有现象的是
(3)如果收集乙装置中产生的气体,两种气体的体积比是
(4)欲用丙装置给铜镀银,G应该是
(5)若丙装置的两极产生气体的质量比为1∶8,则丙中的溶液可以为
21-22高二上·宁夏银川·阶段练习 查看更多[2]
更新时间:2021-11-12 12:02:31
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】人们应用原电池原理制作了多种电池,以满足不同的需要。请根据题中提供的信息,填写空格。
(1)碱性水溶液条件下纽扣式银锌电池的总反应为:Zn+Ag2O=2Ag+ZnO,则其正极电极反应式为:___________ 。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生反应2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为___________ ,电解质溶液为___________ ,反应中Cl-移向___________ (填“负极”或“正极”),FeCl3溶液发生___________ 反应(填“氧化”或“还原”)。当线路中转移0.2mol电子时,参与反应的铜的质量为___________ g.
(3)燃料电池是一种高效、环境友好的供电装置,如图为乙烷燃料电池原理示意图。
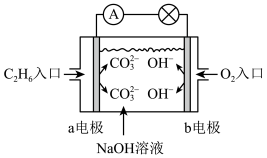
①乙烷通入的一极为电源的___________ 极,该电极反应式:___________ 。
②有0.05molC2H6参与反应时,消耗的氧气体积在标准状况下为___________ L。
(1)碱性水溶液条件下纽扣式银锌电池的总反应为:Zn+Ag2O=2Ag+ZnO,则其正极电极反应式为:
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生反应2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为
(3)燃料电池是一种高效、环境友好的供电装置,如图为乙烷燃料电池原理示意图。

①乙烷通入的一极为电源的
②有0.05molC2H6参与反应时,消耗的氧气体积在标准状况下为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流表。原电池工作时电子是从_____ 到______ (填锌片或银片),锌片电极上发生的是_______________ 反应(“氧化”或“还原”)。电极反应式为_________________________________ ,锌片上观察到的现象为___________
(2)银片上发生的是____________ 反应(“氧化”或“还原”),电极反应式是__________ ,银片上观察到的现象是______________________ 溶液中的C(H+)____________ (填“增大”或“减小”)。
(3)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算:产生氢气的体积为________ L(标准状况);导线中通过的电子数为______ 。
Ⅱ.根据反应:CuCl2 + Fe= FeCl2 + Cu 设计原电池:
(1)在该原电池中,以__________ (写名称)为电解质溶液,铁为______ 极,电极反应式为_______ ,
(2)在该原电池中,选__________ (写名称)作正极,电极反应式是__________________________
(3)画出装置图,标出正、负极材料及电解质溶液名称____________________ 。
(2)银片上发生的是
(3)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算:产生氢气的体积为
Ⅱ.根据反应:CuCl2 + Fe= FeCl2 + Cu 设计原电池:
(1)在该原电池中,以
(2)在该原电池中,选
(3)画出装置图,标出正、负极材料及电解质溶液名称
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据电化学知识回答下列问题:
(1)如图所示,在不同的电解质溶液中可以组成不同的电池。

①当电解质溶液为稀硫酸时,Fe电极是________ (填“正”或“负”)极,其电极反应式为__________ 。
②当电解质溶液为NaOH溶液时,Al电极是________ (填“正”或“负”) 极,其电极反应式为_________ 。
③若把铝改为锌,电解质溶液为浓硝酸,则Fe电极是______ (填“正”或“负”)极,其电极反应式为_______________________________ 。
(2)请你利用原电池原理,设计实验,比较铜和银的金属活动性。画出实验装置图,标出正负极、电子流动方向。________

(1)如图所示,在不同的电解质溶液中可以组成不同的电池。

①当电解质溶液为稀硫酸时,Fe电极是
②当电解质溶液为NaOH溶液时,Al电极是
③若把铝改为锌,电解质溶液为浓硝酸,则Fe电极是
(2)请你利用原电池原理,设计实验,比较铜和银的金属活动性。画出实验装置图,标出正负极、电子流动方向。

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】由硫可制得多硫化钠Na2Sx,x的值一般为2~6。当x=2时,多硫化钠称为过硫化钠。
Ⅰ.过硫化钠加入盐酸中有硫沉淀析出,写出该反应的化学方程式____________ ,该反应的还原产物是__________ 。
Ⅱ.某些多硫化钠可用于制作蓄电池。下图是一种正在投入生产的大型蓄电系统的原理图。
电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过。电池充、放电的化学反应方程式为:



(1)电池中的左侧“电极”的电极名称是________ (填“正极”或“负极”)。
(2)放电过程中钠离子从_______ (选“左到右”或“右到左”)通过离子交换膜。
(3)写出充电过程中阳极的电极反应式__________________________________ 。
Ⅰ.过硫化钠加入盐酸中有硫沉淀析出,写出该反应的化学方程式
Ⅱ.某些多硫化钠可用于制作蓄电池。下图是一种正在投入生产的大型蓄电系统的原理图。
电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过。电池充、放电的化学反应方程式为:



(1)电池中的左侧“电极”的电极名称是
(2)放电过程中钠离子从
(3)写出充电过程中阳极的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336 mL(标准状况)气体。回答:

(1)直流电源中,M为_________ 极。
(2)Pt电极上生成的物质是_________ ,其质量为___________ g。
(3)AgNO3溶液的浓度______ 填“增大”、“减小”或“不变”,下同),AgNO3溶液的pH_________ ,硫酸的浓度________ , 硫酸的pH_________ 。

(1)直流电源中,M为
(2)Pt电极上生成的物质是
(3)AgNO3溶液的浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化工生产的副产氢也是氢气的来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH- FeO
FeO +3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色FeO
+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色FeO ,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。电解一段时间后,c(OH-)降低的区域在
,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。电解一段时间后,c(OH-)降低的区域在_______ (填“阴极室”或“阳极室”),电解过程中,须将阴极产生的气体及时排出,其原因是_______ 。

 FeO
FeO +3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色FeO
+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色FeO ,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。电解一段时间后,c(OH-)降低的区域在
,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。电解一段时间后,c(OH-)降低的区域在
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】环境问题越来越受到人们的重视,研究表明氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。

回答下列问题:
(1)NH3的电子式为____________ ,NH4NO3中含有的化学键是________________ :
(2)下列关于雾霾的叙述错误的是________ (填序号)
A.雾霾中含有硝酸铵和硫酸铵 B.NH3是形成无机颗粒物的催化剂
C.雾霾的形成与过度施用氮肥有关 D.雾霾的形成过程涉及氧化还原反应
(3)预防含硫化合物雾霾生成的方法之一是将氨气和二氧化硫通入水中,再充入O2充分反应生成一种正盐,该反应的化学方程式为________________________ 。预防含氮化合物雾霾生成的方法之一是用稀硝酸吸收NOx,得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸,电解后该溶液的pH_______ (填“变大”“变小”或“不变”)。
(4)在有氧条件下,催化剂能催化NH3与NOx反应生成N2,将一定比例的O2、NH3和NOx混合气体匀速通入装有催化剂的反应器中反应,测得反应温度高于380℃时,NOx的去除率迅速下降,其原因之一是催化剂活性下降,另一重要原因是__________________________ 。在无氧条件下,反应器中NH3能将NO2还原为N2,当生成1mol N2时转移电子________ mol(可用分数表示)。

回答下列问题:
(1)NH3的电子式为
(2)下列关于雾霾的叙述错误的是
A.雾霾中含有硝酸铵和硫酸铵 B.NH3是形成无机颗粒物的催化剂
C.雾霾的形成与过度施用氮肥有关 D.雾霾的形成过程涉及氧化还原反应
(3)预防含硫化合物雾霾生成的方法之一是将氨气和二氧化硫通入水中,再充入O2充分反应生成一种正盐,该反应的化学方程式为
(4)在有氧条件下,催化剂能催化NH3与NOx反应生成N2,将一定比例的O2、NH3和NOx混合气体匀速通入装有催化剂的反应器中反应,测得反应温度高于380℃时,NOx的去除率迅速下降,其原因之一是催化剂活性下降,另一重要原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336moL(标准状况)气体。回答下列问题:

(1)直流电源中,M为_________ 填“正”或“负”)极。
(2)Pt电极上生成的物质是__________ ,其质量为__________ g。
(3)电源输出的电子的物质的量与电极b、c、d分别生成的物质的物质的量之比为2:____ :____ :____ 。
(4) 溶液的浓度
溶液的浓度_________ 填“增大”“减小”或“不变”,下同), 溶液的pH
溶液的pH__________ , 溶液的浓度
溶液的浓度__________ , 溶液的pH
溶液的pH__________ 。
(5)若 溶液的质量分数由5.00%变为5.02%,则原有5.00%的
溶液的质量分数由5.00%变为5.02%,则原有5.00%的 溶液的质量为
溶液的质量为__________ g。

(1)直流电源中,M为
(2)Pt电极上生成的物质是
(3)电源输出的电子的物质的量与电极b、c、d分别生成的物质的物质的量之比为2:
(4)
 溶液的浓度
溶液的浓度 溶液的pH
溶液的pH 溶液的浓度
溶液的浓度 溶液的pH
溶液的pH(5)若
 溶液的质量分数由5.00%变为5.02%,则原有5.00%的
溶液的质量分数由5.00%变为5.02%,则原有5.00%的 溶液的质量为
溶液的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)有一种燃料电池,所用燃料为H2和空气,电解质为熔融的K2CO3。回答下列问题
①CO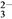 移向
移向____________ 极。
②正极反应式为____________________ 。
③电池中CO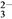 的物质的量将逐渐
的物质的量将逐渐________________ (填增大、减少、不变)。
(2)用上面的电池对下物质进行电解,其中a、b、c、d、e、f电极均为惰性电极,通电后,a极产生的气体明显多于b极,2分钟后,测得乙池的pH为12,则

①电源A极是______________ 极。
②c极上的电极反应式:___________________ 。
③甲、乙两池共可收集到________ mol气体。
④丙装置上某极可析出固体________ 克,溶液的pH为________________ 。(常温,不考虑溶液体积变化)
⑤电解n分钟后,硫酸铜正好消耗完,再将e、f电极反接电源,用同样的电流再电解n分钟,则丙溶液中的硫酸铜的物质的量浓度为______________ mol/L。(不考虑溶液体积变化)
①CO
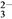 移向
移向②正极反应式为
③电池中CO
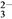 的物质的量将逐渐
的物质的量将逐渐(2)用上面的电池对下物质进行电解,其中a、b、c、d、e、f电极均为惰性电极,通电后,a极产生的气体明显多于b极,2分钟后,测得乙池的pH为12,则

①电源A极是
②c极上的电极反应式:
③甲、乙两池共可收集到
④丙装置上某极可析出固体
⑤电解n分钟后,硫酸铜正好消耗完,再将e、f电极反接电源,用同样的电流再电解n分钟,则丙溶液中的硫酸铜的物质的量浓度为
您最近一年使用:0次
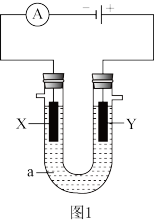
【推荐1】电解原理在化学领域应用广泛如图1表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请完成以下问题:
 +
+
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液:
①在X极附近观察到的现象是______________ ;_______ .
②电解一段时间后,该反应总离子方程式_______ ;
(2)若用该装置电解精炼铜,电解液a选用CuSO4溶液,则:X电极的材料是_______ ,电解一段时间后,CuSO4溶液浓度_______ (填“增大”、减小”或“不变”)。
(3)下列各情况,在其中Fe片腐蚀由快到慢的顺序是:____ ;

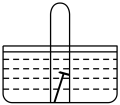
(4)如图, 水槽中试管内有一枚铁钉,放置数天观察:
若试管内液面上升,则正极电极反应式为:______________________ 。
 +
+(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液:
①在X极附近观察到的现象是
②电解一段时间后,该反应总离子方程式
(2)若用该装置电解精炼铜,电解液a选用CuSO4溶液,则:X电极的材料是
(3)下列各情况,在其中Fe片腐蚀由快到慢的顺序是:

(4)如图, 水槽中试管内有一枚铁钉,放置数天观察:

若试管内液面上升,则正极电极反应式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①在X极附近观察到的现象是_________________________________________ 。
②Y电极上的电极反应式为___________________________________ 。
(2)如用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是_______ ,电极反应式为__________________________ 。
②Y电极的材料是_______
(3)工业品氢氧化钾的溶液中含有某些含氧酸杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。
①该电解槽的阳极反应式是_____________________ 。
②通电开始后,阴极附近溶液pH会增大,请简述原因________________ 。
③除去杂质后的氢氧化钾溶液从溶液出口________ (填写“A”或“B”)导出。


(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①在X极附近观察到的现象是
②Y电极上的电极反应式为
(2)如用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是
②Y电极的材料是
(3)工业品氢氧化钾的溶液中含有某些含氧酸杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。
①该电解槽的阳极反应式是
②通电开始后,阴极附近溶液pH会增大,请简述原因
③除去杂质后的氢氧化钾溶液从溶液出口

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如下图所示,A为电源,B为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央有一滴 溶液,C、D为电解槽,其电极材料如图所示。C装置中溶液为
溶液,C、D为电解槽,其电极材料如图所示。C装置中溶液为 溶液,D装置中溶液为
溶液,D装置中溶液为 溶液。
溶液。

(1)关闭 ,打开
,打开 ,通电后,B的
,通电后,B的 紫红色液滴向d端移动。则电源a端为
紫红色液滴向d端移动。则电源a端为_______ 极,通电一段时间后,观察到滤纸c端出现的现象是:_______ 。
(2)打开 ,关闭
,关闭 ,通电一段时间:则D装置中Cu极的电极反应式:
,通电一段时间:则D装置中Cu极的电极反应式:_______ 。C装置中 电极上的电极反应式为:
电极上的电极反应式为:_______ 。C装置中总反应方程式为:_______ 。
 溶液,C、D为电解槽,其电极材料如图所示。C装置中溶液为
溶液,C、D为电解槽,其电极材料如图所示。C装置中溶液为 溶液,D装置中溶液为
溶液,D装置中溶液为 溶液。
溶液。
(1)关闭
 ,打开
,打开 ,通电后,B的
,通电后,B的 紫红色液滴向d端移动。则电源a端为
紫红色液滴向d端移动。则电源a端为(2)打开
 ,关闭
,关闭 ,通电一段时间:则D装置中Cu极的电极反应式:
,通电一段时间:则D装置中Cu极的电极反应式: 电极上的电极反应式为:
电极上的电极反应式为:
您最近一年使用:0次



