为了探究化学能与热能的转化,某实验小组设计了如图所示三套实验装置:

(1)上述3个装置中,不能用于探究“镁与稀盐酸反应是吸热反应还是放热反应”的是___________ (选填“I”、“II”或“III”)。:
(2)某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U形管中可观察到的现象是___________ ,说明该反应属于___________ (选填“吸热”或“放热”)反应。
(3)为探究固体M溶于水的热效应,选择装置II进行实验(在甲试管中进行)。
①若M为钠,则实验过程中烧杯中可观察到的现象是___________ 。
②若观察到烧杯里产生气泡,则说明M溶于水___________ (选填“一定是放热反应”、“一定是吸热反应”或“可能是放热反应”);
③若实验过程中观察到烧杯里的导管内形成一段水柱,则M可能是___________ 。
(4)至少有两种实验方法能证明超氧化钾与水的反应(4KO2+2H2O=4KOH+3O2↑)是放热反应还是吸热反应。
方法①:选择上述装置___________ 进行实验;
方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是___________ (选填“吸热”或“放热”)反应。

(1)上述3个装置中,不能用于探究“镁与稀盐酸反应是吸热反应还是放热反应”的是
(2)某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U形管中可观察到的现象是
(3)为探究固体M溶于水的热效应,选择装置II进行实验(在甲试管中进行)。
①若M为钠,则实验过程中烧杯中可观察到的现象是
②若观察到烧杯里产生气泡,则说明M溶于水
③若实验过程中观察到烧杯里的导管内形成一段水柱,则M可能是
(4)至少有两种实验方法能证明超氧化钾与水的反应(4KO2+2H2O=4KOH+3O2↑)是放热反应还是吸热反应。
方法①:选择上述装置
方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是
更新时间:2021-11-14 10:38:38
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】为了探究化学能与热能的转化,某实验小组设计了如下三套实验装置:
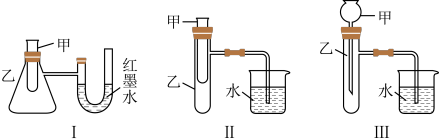
(1)上述装置中,不能证明“锌和稀硫酸反应是吸热反应还是放热反应”的是___ (填序号)。
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡晶体与氯化铵固体搅拌反应,U形管中可观察到的现象是_______ ,化学反应方程式为______ 。
(3)为探究固体M溶于水的热效应,选择装置Ⅱ进行实验(反应在甲中进行)。若观察到烧杯里产生气泡,则M可能是________ (填一种物质的化学式)。
(4)除了图示某些装置,还有其它方法能证明超氧化钾粉末与水的反应(4KO2+2H2O=4KOH+3O2↑)是放热反应还是吸热反应:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是________ 反应(填“放热”或“吸热”)。
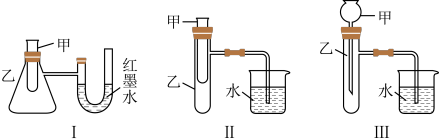
(1)上述装置中,不能证明“锌和稀硫酸反应是吸热反应还是放热反应”的是
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡晶体与氯化铵固体搅拌反应,U形管中可观察到的现象是
(3)为探究固体M溶于水的热效应,选择装置Ⅱ进行实验(反应在甲中进行)。若观察到烧杯里产生气泡,则M可能是
(4)除了图示某些装置,还有其它方法能证明超氧化钾粉末与水的反应(4KO2+2H2O=4KOH+3O2↑)是放热反应还是吸热反应:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。请回答下列问题。
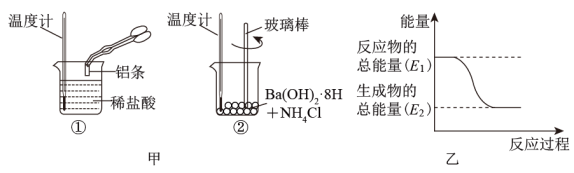
(1)某实验小组同学进行如图甲所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度___________ (填“升高”或“降低”)。反应过程___________ 。(填“①”或“②”)的能量变化可用图乙表示。
(2)工业合成氨反应N2(g) +3H2(g) 2NH3(g)是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1 mol N2(g)完全反应生成NH3(g)可放出92kJ热量。如果将10 mol N2(g)和足量H2(g)混合,使其充分反应,放出的热量
2NH3(g)是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1 mol N2(g)完全反应生成NH3(g)可放出92kJ热量。如果将10 mol N2(g)和足量H2(g)混合,使其充分反应,放出的热量 ___________ (填“大于” “小于”或“等于”)920kJ。
(3)用H2和O2组合形成的质子交换膜燃料电池的结构如图丙:
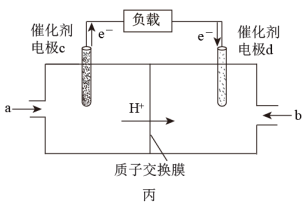
①则电极d是___________ (填“正极”或“负极”),此电极的电极反应式为_____
②若线路中转移2mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为_______ L。

(1)某实验小组同学进行如图甲所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度
(2)工业合成氨反应N2(g) +3H2(g)
 2NH3(g)是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1 mol N2(g)完全反应生成NH3(g)可放出92kJ热量。如果将10 mol N2(g)和足量H2(g)混合,使其充分反应,放出的热量
2NH3(g)是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1 mol N2(g)完全反应生成NH3(g)可放出92kJ热量。如果将10 mol N2(g)和足量H2(g)混合,使其充分反应,放出的热量 (3)用H2和O2组合形成的质子交换膜燃料电池的结构如图丙:

①则电极d是
②若线路中转移2mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】(1)为 了探究化学能与热能的转化,某实验小组设计了如下三套实验装置:
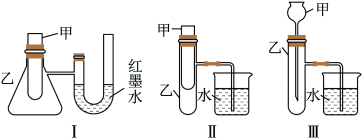
①上述装置中,不能用来证明“锌和稀硫酸反应是吸热反应还是放热反应”的是______ (填序号)。
②某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡晶体与氯化铵固体搅拌反应,U形管中可观察到的现象是__________ 。
③除了图示某些装置,还有其它方法能证明超氧化钾粉末与水的反应(4KO2+2H2O=4KOH+3O2↑)是放热反应还是吸热反应:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是_____ 反应(填“放热”或“吸热”)。
(2)化学反应的焓变通常用实验进行测定,也可进行理论推算。
实验测得,标准状况下11.2 L甲烷在氧气中充分燃烧生成液态水和二氧化碳气体时释放出a kJ的热量,试写出表示甲烷燃烧热的热化学方程式:_____________ 。
(3)研究NO2、SO2、 CO等大气污染气体的处理有重要意义。
如图为1 mol NO2(g)和1 mol CO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图。已知E1=134 kJ/mol,E2=368 kJ/mol (E1、E2为反应的活化能)。

若在反应体系中加入催化剂,反应速率增大,则E1、△H的变化分别是_____ 、______ (填“增大"、“减小”或“不变");该反应放出的热量为________ kJ。

①上述装置中,不能用来证明“锌和稀硫酸反应是吸热反应还是放热反应”的是
②某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡晶体与氯化铵固体搅拌反应,U形管中可观察到的现象是
③除了图示某些装置,还有其它方法能证明超氧化钾粉末与水的反应(4KO2+2H2O=4KOH+3O2↑)是放热反应还是吸热反应:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是
(2)化学反应的焓变通常用实验进行测定,也可进行理论推算。
实验测得,标准状况下11.2 L甲烷在氧气中充分燃烧生成液态水和二氧化碳气体时释放出a kJ的热量,试写出表示甲烷燃烧热的热化学方程式:
(3)研究NO2、SO2、 CO等大气污染气体的处理有重要意义。
如图为1 mol NO2(g)和1 mol CO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图。已知E1=134 kJ/mol,E2=368 kJ/mol (E1、E2为反应的活化能)。

若在反应体系中加入催化剂,反应速率增大,则E1、△H的变化分别是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO。
(1)反应需要在闪电或极高温条件下发生,说明该反应_________ 。(填字母)
A.所需的活化能很高 B.吸收的能量很多
(2)在不同温度下,反应N2(g)+O2(g) 2NO(g)的平衡常数K如下表:
2NO(g)的平衡常数K如下表:
①该反应的△H______ 0。(填“>”、“=”或“<”)
②其他条件相同时,在上述三个温度下分别发生该反应。1538℃时,N2的转化率随时间变化如图所示,请 补充完成1760℃、2404℃时N2的转化率随时间变化的示意图。________________
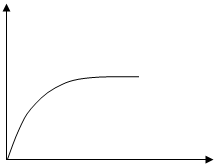
(3)2404℃时,在容积为1.0L的密闭容器中通入2.6mol N2和2.6mol O2,计算反应N2(g)+O2(g) 2NO(g)达到平衡时NO的浓度和O2的转化率。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
2NO(g)达到平衡时NO的浓度和O2的转化率。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)_____________
(1)反应需要在闪电或极高温条件下发生,说明该反应
A.所需的活化能很高 B.吸收的能量很多
(2)在不同温度下,反应N2(g)+O2(g)
 2NO(g)的平衡常数K如下表:
2NO(g)的平衡常数K如下表:| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
①该反应的△H
②其他条件相同时,在上述三个温度下分别发生该反应。1538℃时,N2的转化率随时间变化如图所示,请 补充完成1760℃、2404℃时N2的转化率随时间变化的示意图。

(3)2404℃时,在容积为1.0L的密闭容器中通入2.6mol N2和2.6mol O2,计算反应N2(g)+O2(g)
 2NO(g)达到平衡时NO的浓度和O2的转化率。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
2NO(g)达到平衡时NO的浓度和O2的转化率。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】Ⅰ.用如图所示的装置测定中和反应反应热。实验药品: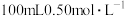 盐酸、
盐酸、 溶液、
溶液、 氨水。
氨水。
实验步骤:略。
已知:弱碱电离时吸热。

回答下列问题。
(1)从实验装置上看,还缺少_________ 。
(2)装置中隔热层的作用是__________________ 。
(3)将浓度为 的酸溶液和
的酸溶液和 的碱溶液各
的碱溶液各 混合(溶液密度均为
混合(溶液密度均为 ),生成的溶液的比热容
),生成的溶液的比热容 ,测得温度如下:
,测得温度如下:
①两组实验结果存在差异的原因是__________________ 。
② 的
的
_________ (保留一位小数)。
③某同学利用上述装置重新做甲组实验,测得反应热 偏大,可能的原因是
偏大,可能的原因是_________ (填序号)
A.测完盐酸的温度直接测NaOH溶液温度
B.做该实验时室温较高
C.杯盖未盖严
D.NaOH溶液一次性迅速倒入
Ⅱ.传统的定量化学实验受到计量手段的制约而研究范围狭窄、精确度不高,DS数字化信息系统(由传感器、数据采集器和计算机组成)因为可以准确测量气压、浓度、pH、温度等而在化学实验研究中应用越来越广泛深入。将打磨后的镁条放入锥形瓶中,再将注射器中某浓度的盐酸压入锥形瓶中,通过数字传感器测定实验中密闭容器(气密性良好)内压强与时间的关系如图2所示。

(4)镁条与盐酸的反应为_________ (填“吸热”或“放热反应。
(5)图2中a、b、c、d四个点中,产生氢气最快的为_________ 点。
(6)图中c点镁条已完全溶解,cd段容器内压强逐渐减小的原因可能是_________ 。
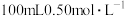 盐酸、
盐酸、 溶液、
溶液、 氨水。
氨水。实验步骤:略。
已知:弱碱电离时吸热。

回答下列问题。
(1)从实验装置上看,还缺少
(2)装置中隔热层的作用是
(3)将浓度为
 的酸溶液和
的酸溶液和 的碱溶液各
的碱溶液各 混合(溶液密度均为
混合(溶液密度均为 ),生成的溶液的比热容
),生成的溶液的比热容 ,测得温度如下:
,测得温度如下:| 反应物 | 起始温度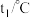 | 最高温度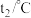 |
甲组 | 20.0 | 23.3 |
乙组 | 20.0 | 23.1 |
②
 的
的
③某同学利用上述装置重新做甲组实验,测得反应热
 偏大,可能的原因是
偏大,可能的原因是A.测完盐酸的温度直接测NaOH溶液温度
B.做该实验时室温较高
C.杯盖未盖严
D.NaOH溶液一次性迅速倒入
Ⅱ.传统的定量化学实验受到计量手段的制约而研究范围狭窄、精确度不高,DS数字化信息系统(由传感器、数据采集器和计算机组成)因为可以准确测量气压、浓度、pH、温度等而在化学实验研究中应用越来越广泛深入。将打磨后的镁条放入锥形瓶中,再将注射器中某浓度的盐酸压入锥形瓶中,通过数字传感器测定实验中密闭容器(气密性良好)内压强与时间的关系如图2所示。

(4)镁条与盐酸的反应为
(5)图2中a、b、c、d四个点中,产生氢气最快的为
(6)图中c点镁条已完全溶解,cd段容器内压强逐渐减小的原因可能是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】江西稀土资源丰富。硫酸铵作为一种重要的化工原料,可用于稀土的提取。初始投料比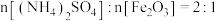 的混合物,其热分解过程如图所示:
的混合物,其热分解过程如图所示:
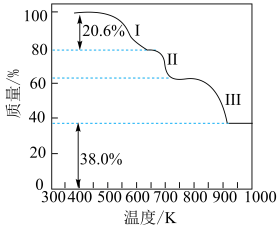
已知该过程主要分为三个阶段,其中:
阶段Ⅱ反应: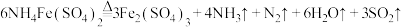
阶段Ⅲ反应: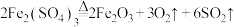
回答下列问题:
(1) 中,
中, 的空间结构为
的空间结构为_______ , 中心原子的杂化类型为
中心原子的杂化类型为______ 。
(2)阶段Ⅰ不发生氧化还原反应,对应的化学方程式为_________ ;图中阶段Ⅰ多次重复实验的实际失重均比理论值偏大,此误差属于______ (填“偶然误差”或“系统误差”)。
(3)阶段Ⅱ和Ⅲ都是吸热过程,且Ⅱ反应速率更快,下列示意图中能体现上述两反应能量变化的是______ (填标号),判断的理由是______ 。
A.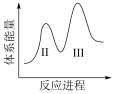 B.
B. 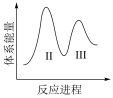 C.
C. 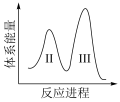 D.
D.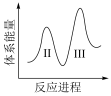
(4)该热分解过程中, 的作用为
的作用为_______ 。
(5)一定温度下,在真空刚性容器中, 的分解过程会发生下列反应:
的分解过程会发生下列反应:
主反应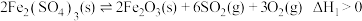
副反应
两个反应的平衡常数比值 随反应温度升高而
随反应温度升高而______ (填“增大”,“减小”或“不变”);若平衡时总压为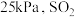 的体积分数为0.4,主反应的平衡常数
的体积分数为0.4,主反应的平衡常数
_____ 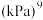 。
。
(6) 在高温下可以自发分解,原因是
在高温下可以自发分解,原因是______ 。
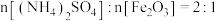 的混合物,其热分解过程如图所示:
的混合物,其热分解过程如图所示:
已知该过程主要分为三个阶段,其中:
阶段Ⅱ反应:
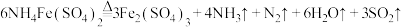
阶段Ⅲ反应:
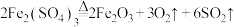
回答下列问题:
(1)
 中,
中, 的空间结构为
的空间结构为 中心原子的杂化类型为
中心原子的杂化类型为(2)阶段Ⅰ不发生氧化还原反应,对应的化学方程式为
(3)阶段Ⅱ和Ⅲ都是吸热过程,且Ⅱ反应速率更快,下列示意图中能体现上述两反应能量变化的是
A.
 B.
B.  C.
C.  D.
D.
(4)该热分解过程中,
 的作用为
的作用为(5)一定温度下,在真空刚性容器中,
 的分解过程会发生下列反应:
的分解过程会发生下列反应:主反应
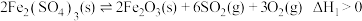
副反应

两个反应的平衡常数比值
 随反应温度升高而
随反应温度升高而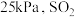 的体积分数为0.4,主反应的平衡常数
的体积分数为0.4,主反应的平衡常数
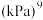 。
。(6)
 在高温下可以自发分解,原因是
在高温下可以自发分解,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】煤是一种重要能源,工业上常把煤进行气化和液化处理,变为清洁能源。由水蒸气和炽热的无烟煤反应可得水煤气,水煤气是混合气体,主要由两种无色无味气体组成,是重要的工业原料。
(1)工业上生产水煤气时,燃料层的温度会下降,这说明_______ 。
(2)提出猜想:水煤气的成分可能是①CO和氢气,②_______ (填化学式)和氢气。提出以上猜想的依据是_______ 。
设计实验:请从下列装置中选择一种,设计简单的实验证明猜想。
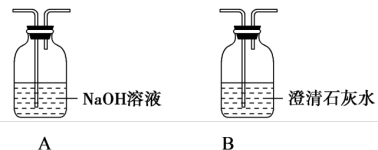
(3)你选择的装置是_______ (填字母代号)。
(4)实验结论:如果_______,那么猜想_______(填序号)合理_______ 。
(1)工业上生产水煤气时,燃料层的温度会下降,这说明
(2)提出猜想:水煤气的成分可能是①CO和氢气,②
设计实验:请从下列装置中选择一种,设计简单的实验证明猜想。

(3)你选择的装置是
(4)实验结论:如果_______,那么猜想_______(填序号)合理
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】富马酸亚铁[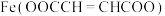 ,
,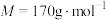 ]是一种治疗贫血的药物。实验制备富马酸亚铁并测定其纯度。
]是一种治疗贫血的药物。实验制备富马酸亚铁并测定其纯度。
Ⅰ.制备富马酸亚铁
步骤1:将4.64g富马酸(HOOCCH=CHCOOH)固体置于100mL烧杯中,加水20mL,在加热搅拌下加入 溶液10mL,使其pH为6.5~6.7,
溶液10mL,使其pH为6.5~6.7,
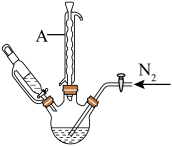
步骤2:将上述溶液转移至如图所示装置中(省略加热、搅拌和夹持装置),通 并加热一段时间后,缓慢滴加40mL
并加热一段时间后,缓慢滴加40mL 的
的 溶液,维持温度100℃,搅拌充分反应1.5h;
溶液,维持温度100℃,搅拌充分反应1.5h;
步骤3:将反应混合液冷却后,通过一系列操作,得到粗产品3.06g。
Ⅱ.纯度分析
取mg样品配制成100mL溶液,取25mL置于250mL锥形瓶中,加入煮沸过的 硫酸溶液15.00mL,待样品完全溶解后,加入煮沸过的蒸馏水50.00mL和2滴邻二氮菲指示剂(邻二氮菲遇
硫酸溶液15.00mL,待样品完全溶解后,加入煮沸过的蒸馏水50.00mL和2滴邻二氮菲指示剂(邻二氮菲遇 呈红色,遇
呈红色,遇 呈无色);立即用
呈无色);立即用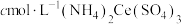 标准溶液滴定至终点(反应的离子方程式为
标准溶液滴定至终点(反应的离子方程式为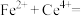
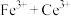 )。平行测定三次,消耗标准溶液的平均体积为VmL。
)。平行测定三次,消耗标准溶液的平均体积为VmL。
(1)仪器A的名称是______ 。
(2)“步骤1”中发生反应的方程式为______ ,pH调节不能过高,其原因是______ 。
(3)“步骤2”中持续通入 的目的是
的目的是______ 。
(4)“步骤3”一系列操作是指减压过滤,______ ,干燥等过程。证明富马酸亚铁产品已洗涤干净的实验操作及现象是______ 。
(5)纯度分析实验中判断达到滴定终点的现象是______ 。
(6)测得产品的纯度为______ 。(用含m、c、V的代数式表示)
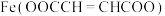 ,
,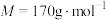 ]是一种治疗贫血的药物。实验制备富马酸亚铁并测定其纯度。
]是一种治疗贫血的药物。实验制备富马酸亚铁并测定其纯度。Ⅰ.制备富马酸亚铁
步骤1:将4.64g富马酸(HOOCCH=CHCOOH)固体置于100mL烧杯中,加水20mL,在加热搅拌下加入
 溶液10mL,使其pH为6.5~6.7,
溶液10mL,使其pH为6.5~6.7,步骤2:将上述溶液转移至如图所示装置中(省略加热、搅拌和夹持装置),通
 并加热一段时间后,缓慢滴加40mL
并加热一段时间后,缓慢滴加40mL 的
的 溶液,维持温度100℃,搅拌充分反应1.5h;
溶液,维持温度100℃,搅拌充分反应1.5h;
步骤3:将反应混合液冷却后,通过一系列操作,得到粗产品3.06g。
Ⅱ.纯度分析
取mg样品配制成100mL溶液,取25mL置于250mL锥形瓶中,加入煮沸过的
 硫酸溶液15.00mL,待样品完全溶解后,加入煮沸过的蒸馏水50.00mL和2滴邻二氮菲指示剂(邻二氮菲遇
硫酸溶液15.00mL,待样品完全溶解后,加入煮沸过的蒸馏水50.00mL和2滴邻二氮菲指示剂(邻二氮菲遇 呈红色,遇
呈红色,遇 呈无色);立即用
呈无色);立即用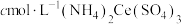 标准溶液滴定至终点(反应的离子方程式为
标准溶液滴定至终点(反应的离子方程式为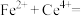
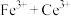 )。平行测定三次,消耗标准溶液的平均体积为VmL。
)。平行测定三次,消耗标准溶液的平均体积为VmL。(1)仪器A的名称是
(2)“步骤1”中发生反应的方程式为
(3)“步骤2”中持续通入
 的目的是
的目的是(4)“步骤3”一系列操作是指减压过滤,
(5)纯度分析实验中判断达到滴定终点的现象是
(6)测得产品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】磁性四氧化三铁是一种多功能磁性材料,在各个领域都有着十分广泛的应用。化学共沉淀法制备磁性四氧化三铁具有工艺简单,操作方便和反应时间短的优点。
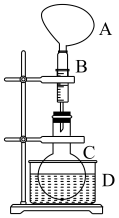
具体操作为:准确称取一定摩尔比质量的FeCl3·6H2O和FeCl2·4H2O于烧瓶中,加入10mL超声除气的蒸馏水,在一定温度下超声溶解后,向烧瓶中快速滴加25%NH3·H2O,控制反应终止的pH为10~11,盖上反口胶塞,组装好装置如图所示,气球中充入N2,在一定温度下进行超声反应,一段时间后,转移至恒温水浴锅,在一定温度下晶化至反应完成。
(1)采用化学共沉淀法制备磁性四氧化三铁颗粒的反应离子方程式为___ 。
(2)气球中充入N2的作用是___ 。
(3)利用恒温水浴锅,在一定温度下剧烈搅拌进行晶化的原因是___ 。
(4)磁性四氧化三铁颗粒用蒸馏水洗涤至中性后,再用乙醇洗涤2遍,用乙醇洗涤的优点是___ 。
(5)向提取磁性四氧化三铁颗粒后的溶液中加入___ ,可制得___ 进行循环使用,其反应生成气体的离子方程式为___ 。
(6)若Fe3+与Fe2+的物质的量分别为0.8mol、0.6mol,反应时间为0.5h,反应温度为80℃,晶化时间为1h、晶化温度为70℃为最佳条件,最终获得的磁性四氧化三铁颗粒质量为33.7g,则产率为___ %(保留至小数点后一位)。
具体操作为:准确称取一定摩尔比质量的FeCl3·6H2O和FeCl2·4H2O于烧瓶中,加入10mL超声除气的蒸馏水,在一定温度下超声溶解后,向烧瓶中快速滴加25%NH3·H2O,控制反应终止的pH为10~11,盖上反口胶塞,组装好装置如图所示,气球中充入N2,在一定温度下进行超声反应,一段时间后,转移至恒温水浴锅,在一定温度下晶化至反应完成。

(1)采用化学共沉淀法制备磁性四氧化三铁颗粒的反应离子方程式为
(2)气球中充入N2的作用是
(3)利用恒温水浴锅,在一定温度下剧烈搅拌进行晶化的原因是
(4)磁性四氧化三铁颗粒用蒸馏水洗涤至中性后,再用乙醇洗涤2遍,用乙醇洗涤的优点是
(5)向提取磁性四氧化三铁颗粒后的溶液中加入
(6)若Fe3+与Fe2+的物质的量分别为0.8mol、0.6mol,反应时间为0.5h,反应温度为80℃,晶化时间为1h、晶化温度为70℃为最佳条件,最终获得的磁性四氧化三铁颗粒质量为33.7g,则产率为
您最近一年使用:0次



