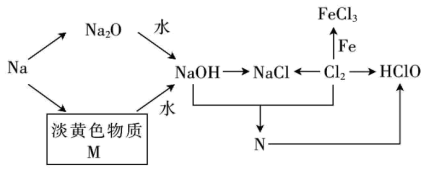
按要求书写方程式
(1)NaHSO4在熔融状态的电离方程式___________
(2)碳酸钙溶解在醋酸中的离子反应方程式___________
(3)将“ ”改写为对应的化学方程式
”改写为对应的化学方程式___________
(4)除去Na2CO3粉末中混有少量NaHCO3的化学方程式___________
(5)氯气与烧碱溶液反应的化学方程式为___________
(6)“84”消毒液与除垢剂(有效成分是盐酸)混合使用会产生黄绿色、有刺激性气味的气体,该反应的离子方程式是___________
(7)衣服上不小心沾到了蓝色墨水,可以先涂上酸性高锰酸钾溶液,即可除去蓝墨水中的鞣酸亚铁,再用乙二酸的稀溶液擦洗,可以迅速除去过量的 ,配平该反应的离子方程式:
,配平该反应的离子方程式:___________
_______MnO +_______H2C2O4+_______H+=_______CO2↑+_______Mn2++______H2O
+_______H2C2O4+_______H+=_______CO2↑+_______Mn2++______H2O
(1)NaHSO4在熔融状态的电离方程式
(2)碳酸钙溶解在醋酸中的离子反应方程式
(3)将“
 ”改写为对应的化学方程式
”改写为对应的化学方程式(4)除去Na2CO3粉末中混有少量NaHCO3的化学方程式
(5)氯气与烧碱溶液反应的化学方程式为
(6)“84”消毒液与除垢剂(有效成分是盐酸)混合使用会产生黄绿色、有刺激性气味的气体,该反应的离子方程式是
(7)衣服上不小心沾到了蓝色墨水,可以先涂上酸性高锰酸钾溶液,即可除去蓝墨水中的鞣酸亚铁,再用乙二酸的稀溶液擦洗,可以迅速除去过量的
 ,配平该反应的离子方程式:
,配平该反应的离子方程式:_______MnO
 +_______H2C2O4+_______H+=_______CO2↑+_______Mn2++______H2O
+_______H2C2O4+_______H+=_______CO2↑+_______Mn2++______H2O
更新时间:2021-11-16 20:39:15
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】现有下列物质:①氢氧化钠固体 ②铜丝 ③氯化氢气体 ④稀硫酸 ⑤二氧化碳气体 ⑥氨水 ⑦碳酸氢钠固体 ⑧蔗糖晶体 ⑨碳酸钙固体 ⑩胆矾(CuSO4·5H2O)晶体
(1)上述物质相应状态下可导电的是_______ ;
(2)属于电解质的是_______ ;
(3)属于非电解质的是_______ ;
(4)⑦溶于水后的电离方程式是_______ ;
(5)①和⑦混合溶于水的离子方程式是_______ ;
(6)③溶于水形成的溶液与⑨反应的离子方程式是_________ 。
(1)上述物质相应状态下可导电的是
(2)属于电解质的是
(3)属于非电解质的是
(4)⑦溶于水后的电离方程式是
(5)①和⑦混合溶于水的离子方程式是
(6)③溶于水形成的溶液与⑨反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在酸性条件下,许多氧化剂可使KI溶液中的I-氧化,例如KIO3(IO3-→I2)、H2O2(H2O2→H2O)、FeCl3(Fe3+→Fe2+)、K2Cr2O7(Cr2O72-→Cr3+)。请根据题目要求填空:
(1)写出在醋酸存在的条件下KIO3溶液与KI溶液反应的离子方程式___________ ;
(2)在酸性条件下(足量),各取1 L浓度为1 mol·L-1的KI溶液分别与上述列举四种溶液进行完全反应,则需要溶质的物质的量之比为n(KIO3)∶n(H2O2)∶n(FeCl3)∶n(K2Cr2O7)=____________ 。
(1)写出在醋酸存在的条件下KIO3溶液与KI溶液反应的离子方程式
(2)在酸性条件下(足量),各取1 L浓度为1 mol·L-1的KI溶液分别与上述列举四种溶液进行完全反应,则需要溶质的物质的量之比为n(KIO3)∶n(H2O2)∶n(FeCl3)∶n(K2Cr2O7)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知反应:①SO3+H2O=H2SO4 ②Cl2+H2O=HCl+HClO(弱酸)
③2F2+2H2O=4HF+O2 ④2Na+2H2O=2NaOH+H2↑
⑤2Na2O2+2H2O=4NaOH+O2↑ ⑥SiO2+2NaOH=Na2SiO3+H2O
(1)上述反应中属于氧化还原反应的是_______ (填序号,下同)。H2O被氧化的是_______ ,H2O被还原的是_______ 。属于氧化还原反应,反应物中的H2O既不被氧化,又不被还原的是_______ 。
(2)写出化学方程式②的离子方程式:_______ 。
③2F2+2H2O=4HF+O2 ④2Na+2H2O=2NaOH+H2↑
⑤2Na2O2+2H2O=4NaOH+O2↑ ⑥SiO2+2NaOH=Na2SiO3+H2O
(1)上述反应中属于氧化还原反应的是
(2)写出化学方程式②的离子方程式:
您最近一年使用:0次
【推荐1】已知:锂钴电池总反应: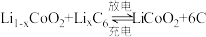 ,过程如图:
,过程如图:
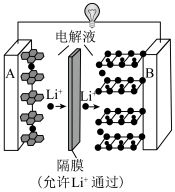
(1) 中,Co元素的化合价为
中,Co元素的化合价为___________ ;锂电池发生火灾时,和氧气发生反应的主要物质是___________ (填“正”或“负”)极材料;充电时阳极的反应方程式是___________ 。
(2)锂电池成本高昂,废弃后需回收其中的锂和钴元素,先将上述锂电池进行放电处理,拆卸后,再将正极材料 涂覆在铝箔上,进行电解,浸出
涂覆在铝箔上,进行电解,浸出 和
和 ,装置如图所示,该条件下副反应忽略不计。
,装置如图所示,该条件下副反应忽略不计。
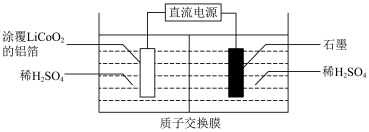
①拆卸前,将锂电池放电处理有利于锂在正极的回收,其原因是___________ 。
②石墨电极连接电源的___________ 极(填“正”或“负”)。
③结合电极反应,指出阴极室的pH变化并解释原因:___________ 。
(3)当前,三元正极材料——镍钴锰酸锂应用广泛,其化学式可写作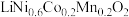 。可用
。可用 、
、 、
、 、
、 与空气混合加热烧结制得,写出制备的化学方程式:
与空气混合加热烧结制得,写出制备的化学方程式:___________ (设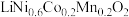 的计量系数为1)。
的计量系数为1)。
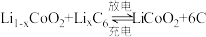 ,过程如图:
,过程如图:
(1)
 中,Co元素的化合价为
中,Co元素的化合价为(2)锂电池成本高昂,废弃后需回收其中的锂和钴元素,先将上述锂电池进行放电处理,拆卸后,再将正极材料
 涂覆在铝箔上,进行电解,浸出
涂覆在铝箔上,进行电解,浸出 和
和 ,装置如图所示,该条件下副反应忽略不计。
,装置如图所示,该条件下副反应忽略不计。
①拆卸前,将锂电池放电处理有利于锂在正极的回收,其原因是
②石墨电极连接电源的
③结合电极反应,指出阴极室的pH变化并解释原因:
(3)当前,三元正极材料——镍钴锰酸锂应用广泛,其化学式可写作
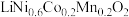 。可用
。可用 、
、 、
、 、
、 与空气混合加热烧结制得,写出制备的化学方程式:
与空气混合加热烧结制得,写出制备的化学方程式: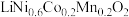 的计量系数为1)。
的计量系数为1)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】一定条件下,含氮元素的物质可发生如图所示的循环转化。
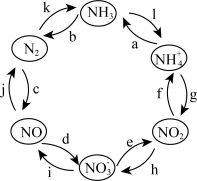
回答下列问题:
(1)氮的原子结构示意图为_________ 。
(2)图中属于“氮的固定”的是_________ (填字母,下同);转化过程中发生非氧化还原反应的是_________ 。
(3)若“反应h”是在NO2与H2O的作用下实现,则该反应中氧化产物与还原产物的物质的量之比为_________ 。
(4)若“反应i”是在酸性条件下由NO3-与Zn的作用实现,则该反应的离子方程式为_____ 。

回答下列问题:
(1)氮的原子结构示意图为
(2)图中属于“氮的固定”的是
(3)若“反应h”是在NO2与H2O的作用下实现,则该反应中氧化产物与还原产物的物质的量之比为
(4)若“反应i”是在酸性条件下由NO3-与Zn的作用实现,则该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)有以下几种物质①干燥的食盐晶体 ②液态氯化氢 ③Cu ④蔗糖 ⑤NH3 ⑥KNO3溶液 ⑦CO2 ⑧熔融的KCl ⑨石墨。填空回答(填序号):以上物质中能导电的是______________ ;属于电解质的是__________ ;属于非电解质的是______________ ;
(2)用“双线桥”表示出反应中电子转移的方向和数目:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O_______
(3)铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐为重要化合物。高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为________________ 。
(2)用“双线桥”表示出反应中电子转移的方向和数目:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
(3)铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐为重要化合物。高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物有重要用途,下图为氯元素的“价类二维图”的部分信息。请回答下列问题:
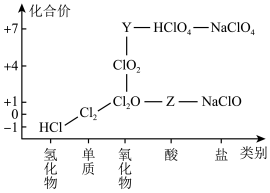
(1)根据图中信息写出Y、Z的化学式_______ 、_______ 。
(2)84消毒液能有效杀灭新冠病毒。某品牌84消毒液瓶体的部分标签如图所示。
回答下列问题:
①某使用说明中特别提醒84消毒液不可与洁厕灵(主要成分盐酸)混合使用,否则会产生 ,请用离子方程式表示其原因
,请用离子方程式表示其原因_______ 。
②如图所示,该品牌84消毒液的物质的量浓度为_______ ,84消毒液使用时需要稀释,某化学实验小组用上述84消毒液配制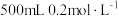 的稀溶液,需要用量筒量取该84消毒液
的稀溶液,需要用量筒量取该84消毒液_______  。
。
③配制过程中,下列操作会造成新配制的稀溶液浓度偏低的是_______ 。
A.量取浓84消毒液的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
B.容量瓶使用时未干燥
C.定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
D.定容时俯视刻度线
(3)①二氧化氯是一种高效消毒剂。实验室可用亚氯酸钠( )溶液与氯气反应制
)溶液与氯气反应制 ,同时生成氯化钠,此反应的化学方程式为
,同时生成氯化钠,此反应的化学方程式为_______ 。
② 可将废水中的
可将废水中的 转化为
转化为 而除去,本身被还原为
而除去,本身被还原为 ,该反应过程中氧化剂与还原剂的物质的量之比为
,该反应过程中氧化剂与还原剂的物质的量之比为_______ 。

(1)根据图中信息写出Y、Z的化学式
(2)84消毒液能有效杀灭新冠病毒。某品牌84消毒液瓶体的部分标签如图所示。
| 84消毒液 有效成分  规格  质量分数 25% 密度 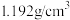 |
①某使用说明中特别提醒84消毒液不可与洁厕灵(主要成分盐酸)混合使用,否则会产生
 ,请用离子方程式表示其原因
,请用离子方程式表示其原因②如图所示,该品牌84消毒液的物质的量浓度为
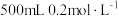 的稀溶液,需要用量筒量取该84消毒液
的稀溶液,需要用量筒量取该84消毒液 。
。③配制过程中,下列操作会造成新配制的稀溶液浓度偏低的是
A.量取浓84消毒液的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
B.容量瓶使用时未干燥
C.定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
D.定容时俯视刻度线
(3)①二氧化氯是一种高效消毒剂。实验室可用亚氯酸钠(
 )溶液与氯气反应制
)溶液与氯气反应制 ,同时生成氯化钠,此反应的化学方程式为
,同时生成氯化钠,此反应的化学方程式为②
 可将废水中的
可将废水中的 转化为
转化为 而除去,本身被还原为
而除去,本身被还原为 ,该反应过程中氧化剂与还原剂的物质的量之比为
,该反应过程中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氯气极其相关产品在生产生活中应用广泛。
(1)氯气属于有毒气体,贮氯罐意外泄漏时,消防员会喷洒稀氢氧化钠溶液,其作用是__________ 。(用化学方程式表示)。
实验室常用NaOH溶液吸收多余的氯气,下列也可用于吸收氯气的是_________ (填字母)。
a.NaCl溶液 b.FeSO4溶液 c.KMnO4溶液
(2)家庭中常用消毒液(主要成分NaClO)、洁厕灵(主要成分盐酸)等清洁卫生。某品牌消毒液包装上的说明如下图。
①分析“对金属制品有腐蚀作用”的原因:_______________ 。
②需“密闭保存”的原因:______________ 。
③“与洁厕灵同时使用”会产生有毒的氯气,请写出反应的离子方程式_____________ 。
(3)已知空气中氯气含量超过0.1mg/m3就会引起中毒。某液氯生产车间在一次测定空气中氯气的含量时,测得消耗0.001ml/L Kl溶液100mL,为了判断空气中氯气的含量是否超标,还需要获得的数据是_______ 。
(1)氯气属于有毒气体,贮氯罐意外泄漏时,消防员会喷洒稀氢氧化钠溶液,其作用是
实验室常用NaOH溶液吸收多余的氯气,下列也可用于吸收氯气的是
a.NaCl溶液 b.FeSO4溶液 c.KMnO4溶液
(2)家庭中常用消毒液(主要成分NaClO)、洁厕灵(主要成分盐酸)等清洁卫生。某品牌消毒液包装上的说明如下图。

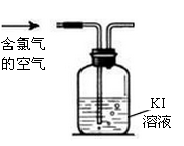
①分析“对金属制品有腐蚀作用”的原因:
②需“密闭保存”的原因:
③“与洁厕灵同时使用”会产生有毒的氯气,请写出反应的离子方程式
(3)已知空气中氯气含量超过0.1mg/m3就会引起中毒。某液氯生产车间在一次测定空气中氯气的含量时,测得消耗0.001ml/L Kl溶液100mL,为了判断空气中氯气的含量是否超标,还需要获得的数据是
您最近一年使用:0次