按要求回答下列问题:
(1)可用___________ 效应区别FeCl3溶液和Fe(OH)3胶体。
(2)新制氯水在阳光照射下产生的无色气体是___________ (填名称)。
(3)用四氯化碳萃取溴水后,分液时水层从分液漏斗的___________ (填“下口放出”或“上口倒出”)。
(4)工业上制漂白粉的化学方程式为___________ 。
(5)等质量的NH3和H2S中,氢原子的个数比是___________ 。
(6)将100 mL 2.50 mol/L BaCl2溶液加水稀释至500 mL,所得溶液中Cl-物质的量浓度为___________ 。
(7)10.8 g R2O5中氧原子的数目为3.01×1023,则R的摩尔质量为___________ 。
(8)某光卤石(KCl·MgCl2·6H2O)中含5.3250 g Cl-,则该光卤石的物质的量为___________ 。
(1)可用
(2)新制氯水在阳光照射下产生的无色气体是
(3)用四氯化碳萃取溴水后,分液时水层从分液漏斗的
(4)工业上制漂白粉的化学方程式为
(5)等质量的NH3和H2S中,氢原子的个数比是
(6)将100 mL 2.50 mol/L BaCl2溶液加水稀释至500 mL,所得溶液中Cl-物质的量浓度为
(7)10.8 g R2O5中氧原子的数目为3.01×1023,则R的摩尔质量为
(8)某光卤石(KCl·MgCl2·6H2O)中含5.3250 g Cl-,则该光卤石的物质的量为
更新时间:2021-11-19 20:12:17
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某化学小组围绕 开展主题学习。
开展主题学习。
Ⅰ.分类和性质
(1)墨粉中含有 (可表示为
(可表示为 ),
),
___________ (填“是”或“不是”)碱性氧化物,原因为___________ (用化学反应方程式说明)。
Ⅱ.制备
方法一:

方法二:

(2)方法二中A的化学式是___________ ,操作Ⅰ和操作Ⅱ相同,为___________ 。
(3)与方法二比较,方法一的不足之处有___________ (答1点即可)。
(4)氢氧化氧铁(FeOOH)中铁元素的化合价是___________ ,当A溶液①和A溶液②的质量之比为___________ 时,铁元素全部转化到 中。
中。
Ⅲ.应用
(5)纳米高性能 (平均直径为
(平均直径为 )可以实现高效催化分解水,其反应历程如下图所示。
)可以实现高效催化分解水,其反应历程如下图所示。

①该过程中的能量转化形式为___________ 转化为化学能,在加热的条件下反应b的化学方程式为___________ 。
②纳米高性能 均匀分散在水中,具有丁达尔现象,请设计实验方案证明
均匀分散在水中,具有丁达尔现象,请设计实验方案证明___________ 。
 开展主题学习。
开展主题学习。Ⅰ.分类和性质
(1)墨粉中含有
 (可表示为
(可表示为 ),
),
Ⅱ.制备
方法一:

方法二:

(2)方法二中A的化学式是
(3)与方法二比较,方法一的不足之处有
(4)氢氧化氧铁(FeOOH)中铁元素的化合价是
 中。
中。Ⅲ.应用
(5)纳米高性能
 (平均直径为
(平均直径为 )可以实现高效催化分解水,其反应历程如下图所示。
)可以实现高效催化分解水,其反应历程如下图所示。
①该过程中的能量转化形式为
②纳米高性能
 均匀分散在水中,具有丁达尔现象,请设计实验方案证明
均匀分散在水中,具有丁达尔现象,请设计实验方案证明
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.现有下列物质:①蔗糖、②Na2CO3溶液、③稀硫酸、④CO2、⑤CuSO4·5H2O固体、⑥石墨棒、⑦含泥沙的氯化钠溶液、⑧淀粉溶液
(1)属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
(2)除去⑦中的泥沙杂质的实验操作方法是___________ 。
(3)将气体④通入②会发生化学反应,其化学方程式为___________ 。
Ⅱ.央视《每周质量报告》曝光了一些明胶企业将皮革废料熬制成工业明胶,出售给某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(4)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是___________ 价。Fe(CrO2)2属于___________ (填“酸”、“碱”、“盐”或“氧化物”)。
(5)明胶的水溶液和K2SO4溶液共同具备的性质是___________(填序号)。
(1)属于电解质的是
(2)除去⑦中的泥沙杂质的实验操作方法是
(3)将气体④通入②会发生化学反应,其化学方程式为
Ⅱ.央视《每周质量报告》曝光了一些明胶企业将皮革废料熬制成工业明胶,出售给某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(4)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是
(5)明胶的水溶液和K2SO4溶液共同具备的性质是___________(填序号)。
| A.都不稳定,密封放置会产生沉淀 | B.分散质粒子可通过滤纸 |
| C.分散质粒子可通过半透膜 | D.二者均有丁达尔效应 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】把10 mL淀粉胶体和5 mL NaCl溶液混合,后加入用半透膜制成的袋内,将此袋浸入烧杯内的蒸馏水中,2 min后,用两支试管各取5 mL烧杯中的液体,并做如下实验(淀粉遇碘水变蓝色):
(1)向其中一支试管里滴加少量AgNO3溶液,其现象是___________ ;
(2)向另一支试管中滴加少量碘水,其现象___________ ;
(3)由上述实验得出的结论是___________ ;
(4)证明淀粉与NaCl溶液已分离完全的实验方法是___________ 。
(1)向其中一支试管里滴加少量AgNO3溶液,其现象是
(2)向另一支试管中滴加少量碘水,其现象
(3)由上述实验得出的结论是
(4)证明淀粉与NaCl溶液已分离完全的实验方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知硫酸钠晶体(Na2SO4·10H2O)为1mol,请计算填空:
(1)钠离子的物质的量是_______ ,硫酸钠晶体的物质的量是_______ ;
(2)所含硫酸根离子的物质的量是_______ ,硫酸根离子的数目是_______ ;
(3)所含结晶水的物质的量是_______ ,所含氧原子的物质的量是_______ 。
(1)钠离子的物质的量是
(2)所含硫酸根离子的物质的量是
(3)所含结晶水的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列填空
(1)①0.3molNH3分子中所含原子数与___________ 个 分子中所含原子数相等。
分子中所含原子数相等。
②在一定的温度和压强下,1体积气体X2跟3体积气体Y2刚好化合生成2体积气体A,则A的化学式可表示为___________ 。
③在同温同压同体积的条件下, 与气体B的质量之比是1:8,则B的摩尔质量为
与气体B的质量之比是1:8,则B的摩尔质量为___________ 。
④在 、101kPa的条件下,同质量的
、101kPa的条件下,同质量的 和气体C的体积之比是15:8,则C的摩尔质量为
和气体C的体积之比是15:8,则C的摩尔质量为___________ 。
⑤相同温度下在两个相同容积的密闭容器D、E中,分别充入相同质量的X气体和CO气体,D和E中的压强之比是7:16,则X的摩尔质量为___________ 。
(2)按下列要求回答:①Cu;②Al2O3;③CH3COOH(醋酸);④干冰;⑤Ba(OH)2;⑥C2H5OH(酒精);⑦KClO3;⑧CaCO3;⑨氨水;⑩液态硫酸
a.上述各物质属于电解质的是___________ (填物质编号,下同);属于非电解质的是___________ ;能导电的物质是___________ 。
b.⑤在水中的电离方程式为___________ 。⑦在水中的电离方程式为___________
(1)①0.3molNH3分子中所含原子数与
 分子中所含原子数相等。
分子中所含原子数相等。②在一定的温度和压强下,1体积气体X2跟3体积气体Y2刚好化合生成2体积气体A,则A的化学式可表示为
③在同温同压同体积的条件下,
 与气体B的质量之比是1:8,则B的摩尔质量为
与气体B的质量之比是1:8,则B的摩尔质量为④在
 、101kPa的条件下,同质量的
、101kPa的条件下,同质量的 和气体C的体积之比是15:8,则C的摩尔质量为
和气体C的体积之比是15:8,则C的摩尔质量为⑤相同温度下在两个相同容积的密闭容器D、E中,分别充入相同质量的X气体和CO气体,D和E中的压强之比是7:16,则X的摩尔质量为
(2)按下列要求回答:①Cu;②Al2O3;③CH3COOH(醋酸);④干冰;⑤Ba(OH)2;⑥C2H5OH(酒精);⑦KClO3;⑧CaCO3;⑨氨水;⑩液态硫酸
a.上述各物质属于电解质的是
b.⑤在水中的电离方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据所学知识回答下列问题:
(1)下列物质中:①SO2;②液态氯化氢;③CH4;④熔融NaOH;⑤NH4Cl固体;⑥氨水。能导电的是___________ (填序号)。
(2)实验室制备氢氧化铁胶体,反应的离子方程式为___________ 。
(3)1.204×1024个H2SO4分子的质量为___________ g,共含___________ 个氢原子。
(4)在标准状况下,CO和CO2混合气体共33.6L,质量为51.6g,则两种气体的物质的量之和为___________ mol,CO与CO2物质的量之比为___________ 。
(5)某反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O,试写出该反应的化学方程式___________ 。
(1)下列物质中:①SO2;②液态氯化氢;③CH4;④熔融NaOH;⑤NH4Cl固体;⑥氨水。能导电的是
(2)实验室制备氢氧化铁胶体,反应的离子方程式为
(3)1.204×1024个H2SO4分子的质量为
(4)在标准状况下,CO和CO2混合气体共33.6L,质量为51.6g,则两种气体的物质的量之和为
(5)某反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O,试写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)0.05 mol的硫酸钠中含有______ 个氧原子,与______ g NaCl中所含有的Na+数目相同。
(2)质量都是 50 g 的HCl、NH3、CO2、O2四种气体中,在相同温度和相同压强条件下,体积最大的是______ (填分子式)。
(3)0. 5 L 0.5 mol • L-1FeCl3溶液中的 Cl-的物质的量浓度为________ 。
(4)O2、SO2、SO3的质量之比为1:2:5,则它们的氧原子数之比为________ 。
(2)质量都是 50 g 的HCl、NH3、CO2、O2四种气体中,在相同温度和相同压强条件下,体积最大的是
(3)0. 5 L 0.5 mol • L-1FeCl3溶液中的 Cl-的物质的量浓度为
(4)O2、SO2、SO3的质量之比为1:2:5,则它们的氧原子数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氧化还原反应是一类重要的化学反应,广泛存在于生产和生活中。对我们的生产和生活中可能同时具有正负两方面的影响,如果我们能够掌握化学变化的规律,就有可能做到趋利避害,使之更好地为社会的发展服务。下面我们逐一分析:
(1)黑火药是我国古代的四大发明之一、黑火药着火时,发生如下氧化还原反应:
 。在此反应中,被还原的元素为
。在此反应中,被还原的元素为___________ (填元素符号),氧化产物是___________ (填化学式),4.8gS参加反应时,产生气体的体积为___________ L(标况下)。
(2)硝酸是一种具有强氧化性的无机酸,是六大无机强酸之一,也是一种重要的化工原料,常用于制造氮肥、硝酸盐、硝化甘油等。某硝酸溶液的密度为 ,质量分数为63%,请计算其物质的量浓度为
,质量分数为63%,请计算其物质的量浓度为___________ mol/L。另有一容器中发生某化学反应,反应过程中存在 、
、 、
、 、
、 、
、 和
和 六种粒子,在反应过程中测得
六种粒子,在反应过程中测得 、
、 的物质的量随时间变化的曲线如下图所示,请你写出此离子反应方程式:
的物质的量随时间变化的曲线如下图所示,请你写出此离子反应方程式:___________ 。

(3)汽车剧烈碰撞时,安全气囊中发生反应: 。若反应得到的氧化产物比还原产物多0.7mol,则此过程中转移电子的物质的量为
。若反应得到的氧化产物比还原产物多0.7mol,则此过程中转移电子的物质的量为___________ mol。
(4) 与一定浓度的
与一定浓度的 反应,生成
反应,生成 、
、 、
、 、NO和
、NO和 ,当
,当 和NO的个数之比为2:1时,实际参加反应的
和NO的个数之比为2:1时,实际参加反应的 与表现氧化性的
与表现氧化性的 的个数之比为
的个数之比为_______ 。
(5)一定量的某磁黄铁矿(主要成分 ,S为-2价)与100mL盐酸恰好完全反应(矿石中其他成分不与盐酸反应),生成3.2g硫单质、
,S为-2价)与100mL盐酸恰好完全反应(矿石中其他成分不与盐酸反应),生成3.2g硫单质、 和一定量
和一定量 气体,且溶液中无
气体,且溶液中无 ,该磁黄铁矿中
,该磁黄铁矿中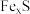 的x=
的x=___________ 。
(1)黑火药是我国古代的四大发明之一、黑火药着火时,发生如下氧化还原反应:
 。在此反应中,被还原的元素为
。在此反应中,被还原的元素为(2)硝酸是一种具有强氧化性的无机酸,是六大无机强酸之一,也是一种重要的化工原料,常用于制造氮肥、硝酸盐、硝化甘油等。某硝酸溶液的密度为
 ,质量分数为63%,请计算其物质的量浓度为
,质量分数为63%,请计算其物质的量浓度为 、
、 、
、 、
、 、
、 和
和 六种粒子,在反应过程中测得
六种粒子,在反应过程中测得 、
、 的物质的量随时间变化的曲线如下图所示,请你写出此离子反应方程式:
的物质的量随时间变化的曲线如下图所示,请你写出此离子反应方程式:
(3)汽车剧烈碰撞时,安全气囊中发生反应:
 。若反应得到的氧化产物比还原产物多0.7mol,则此过程中转移电子的物质的量为
。若反应得到的氧化产物比还原产物多0.7mol,则此过程中转移电子的物质的量为(4)
 与一定浓度的
与一定浓度的 反应,生成
反应,生成 、
、 、
、 、NO和
、NO和 ,当
,当 和NO的个数之比为2:1时,实际参加反应的
和NO的个数之比为2:1时,实际参加反应的 与表现氧化性的
与表现氧化性的 的个数之比为
的个数之比为(5)一定量的某磁黄铁矿(主要成分
 ,S为-2价)与100mL盐酸恰好完全反应(矿石中其他成分不与盐酸反应),生成3.2g硫单质、
,S为-2价)与100mL盐酸恰好完全反应(矿石中其他成分不与盐酸反应),生成3.2g硫单质、 和一定量
和一定量 气体,且溶液中无
气体,且溶液中无 ,该磁黄铁矿中
,该磁黄铁矿中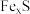 的x=
的x=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】高锰酸钾是一种典型的强氧化剂。完成下列填空:
I:在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
① MnO +Cu2S+H+
+Cu2S+H+ Cu2++SO2↑+Mn2++H2O(未配平)
Cu2++SO2↑+Mn2++H2O(未配平)
② MnO +CuS +H+
+CuS +H+ Cu2++SO2↑+Mn2++H2O(未配平)
Cu2++SO2↑+Mn2++H2O(未配平)
(1)下列关于反应①的说法中错误的是___________(填字母序号)。
II:在稀硫酸中,KMnO4与 (NH4)2Fe(SO4)2也能发生氧化还原反应。
(2)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:_ ___MnO +______Fe2++______H+=_____Mn2+_____Fe3++ ____ H2O
+______Fe2++______H+=_____Mn2+_____Fe3++ ____ H2O
(3)欲配制480mL 0.1mol/L Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392g/mol)的质量为___________ g,需要的玻璃仪器有___________
I:在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
① MnO
 +Cu2S+H+
+Cu2S+H+ Cu2++SO2↑+Mn2++H2O(未配平)
Cu2++SO2↑+Mn2++H2O(未配平)② MnO
 +CuS +H+
+CuS +H+ Cu2++SO2↑+Mn2++H2O(未配平)
Cu2++SO2↑+Mn2++H2O(未配平)(1)下列关于反应①的说法中错误的是___________(填字母序号)。
| A.被氧化的元素是Cu和S |
| B.氧化剂与还原剂的物质的量之比为8∶5 |
| C.生成2.24 L(标况下)SO2,转移电子的物质的量是0.8 mol |
| D.还原性的强弱关系是:Mn2+>Cu2S |
II:在稀硫酸中,KMnO4与 (NH4)2Fe(SO4)2也能发生氧化还原反应。
(2)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
 +______Fe2++______H+=_____Mn2+_____Fe3++ ____ H2O
+______Fe2++______H+=_____Mn2+_____Fe3++ ____ H2O(3)欲配制480mL 0.1mol/L Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392g/mol)的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某化学课外小组用海带为原料制取了少量碘水。现用CCl4从碘水中萃取碘,并用分液漏斗分离两种溶液。其实验操作可分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把10mL碘水和4mLCCl4加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转分液漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层水溶液;
G.将分液漏斗上口的玻璃塞打开或使塞上的凹槽(或小孔)对准分液漏斗口上的小孔;
H.静置,分层。
就此实验,完成下列填空:
(1)正确操作步骤的顺序是:___________ (用上述各操作的编号字母填写)______→______→_______→A→_______→G→E→F。
(2)上述E步骤的操作中应注意________ ;上述G步骤操作的目的是________ 。
(3)选用CCl4从碘水中萃取碘的原因:________ 。
(4)已知碘在酒精中的溶解度比在水中大得多,_______ (填“能”或“不能”)用酒精来萃取碘水中的碘,其理由是________ 。
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把10mL碘水和4mLCCl4加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转分液漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层水溶液;
G.将分液漏斗上口的玻璃塞打开或使塞上的凹槽(或小孔)对准分液漏斗口上的小孔;
H.静置,分层。
就此实验,完成下列填空:
(1)正确操作步骤的顺序是:
(2)上述E步骤的操作中应注意
(3)选用CCl4从碘水中萃取碘的原因:
(4)已知碘在酒精中的溶解度比在水中大得多,
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.某研究性学习小组为了验证臭氧的氧化性强于氧气 ,设计了实验。
(1)a溶液是一种显色剂,用来检验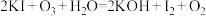 反应确有发生,a物质是
反应确有发生,a物质是___________ 。
(2)已知碘在酒精中的溶解度比在水中大得多,能否用酒精来萃取碘水中的碘___________ (填“能”或“不能”),其理由是___________ 。
(3)向碘水中加入适量的四氯化碳,充分振荡后,观察到的现象是___________。
(4)写出在臭氧消毒柜放电条件下产生 的化学方程式:
的化学方程式:___________ 。这是一个___________ (填“氧化还原”或“非氧化还原”)反应。
(5)在 氧化KI的反应中
氧化KI的反应中
①用单线桥法标出上述反应电子转移的方向和数目_________ 。
②若有9.6g 发生反应,则转移电子的物质的量为
发生反应,则转移电子的物质的量为___________ ,发生氧化反应的元素是___________ ;还原产物为___________ 。
Ⅱ.海水是巨大的资源宝库,可以进行综合利用。从海水中提取淡水、食盐和溴的过程如下:
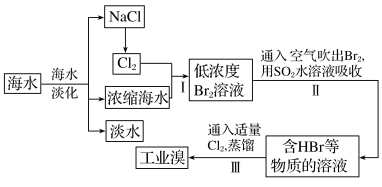
(6)步骤I获得 的反应的离子方程式为
的反应的离子方程式为___________
(7)步骤II用 水溶液吸收
水溶液吸收 ,使溴蒸气转化为氢溴酸以达到富集的目的,其反应的化学方程式为
,使溴蒸气转化为氢溴酸以达到富集的目的,其反应的化学方程式为___________ (若反应中生成2molHBr,则消耗lmol )。
)。
(8)根据上述反应可判断出 、
、 、
、 三种物质氧化性由强到弱的顺序是
三种物质氧化性由强到弱的顺序是___________ 。
(1)a溶液是一种显色剂,用来检验
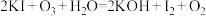 反应确有发生,a物质是
反应确有发生,a物质是(2)已知碘在酒精中的溶解度比在水中大得多,能否用酒精来萃取碘水中的碘
(3)向碘水中加入适量的四氯化碳,充分振荡后,观察到的现象是___________。
| A.溶液分层,上层紫红色,下层接近无色 |
| B.溶液不分层,溶液紫红色 |
| C.溶液分层,上层接近无色,下层紫红色 |
| D.溶液不分层,溶液黄色 |
(4)写出在臭氧消毒柜放电条件下产生
 的化学方程式:
的化学方程式:(5)在
 氧化KI的反应中
氧化KI的反应中
①用单线桥法标出上述反应电子转移的方向和数目
②若有9.6g
 发生反应,则转移电子的物质的量为
发生反应,则转移电子的物质的量为Ⅱ.海水是巨大的资源宝库,可以进行综合利用。从海水中提取淡水、食盐和溴的过程如下:

(6)步骤I获得
 的反应的离子方程式为
的反应的离子方程式为(7)步骤II用
 水溶液吸收
水溶液吸收 ,使溴蒸气转化为氢溴酸以达到富集的目的,其反应的化学方程式为
,使溴蒸气转化为氢溴酸以达到富集的目的,其反应的化学方程式为 )。
)。(8)根据上述反应可判断出
 、
、 、
、 三种物质氧化性由强到弱的顺序是
三种物质氧化性由强到弱的顺序是
您最近一年使用:0次



