在一定温度下,冰醋酸稀释过程中溶液的导电能力变化如图所示,请填写下列空白。
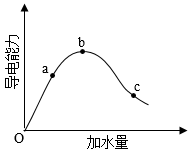
(1)加水前导电能力约为零的原因是___________ 。
(2)a、b、c三点对应的溶液中, 由小到大的顺序是
由小到大的顺序是___________ 。
(3)a、b、c三点对应的溶液中, 电离程度最大的是
电离程度最大的是___________ 。
(4)若使b点对应的溶液中 增大、
增大、 减小,可采用的方法是
减小,可采用的方法是___________ (填序号)。
①加入
②加入NaOH固体
③加入浓硫酸
④加入 固体
固体

(1)加水前导电能力约为零的原因是
(2)a、b、c三点对应的溶液中,
 由小到大的顺序是
由小到大的顺序是(3)a、b、c三点对应的溶液中,
 电离程度最大的是
电离程度最大的是(4)若使b点对应的溶液中
 增大、
增大、 减小,可采用的方法是
减小,可采用的方法是①加入

②加入NaOH固体
③加入浓硫酸
④加入
 固体
固体
更新时间:2021-12-01 23:57:53
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】有下列物质:①液态氯化氢,②氯化铁溶液,③盐酸,④氯化铵晶体,⑤蔗糖溶液,⑥酒精,⑦硫酸钡固体,⑧淀粉溶液,⑨熔融氢氧化钠,⑩铜。回答下面问题:
(1)上述物质中能够导电的是____ (填序号,下同),属于电解质的是____ ,属于非电解质是____ 。
(2)写出④在溶液中的电离方程式:____ 。
(3)证明⑧是胶体的方法是____ 。
(1)上述物质中能够导电的是
(2)写出④在溶液中的电离方程式:
(3)证明⑧是胶体的方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】分门别类地研究物质的组成、性质、用途,可以找到有关规律,发现同类物质之间的内在联系。下图是按树状分类法对一组物质进行的分类,回答下列问题。

已知:纳米颗粒是指颗粒直径在1~100nm之间的微粒。
(1)类别1是_________ ,分类标准2为_________ 。
(2)按照上述分类图示,物质③应填入图中_________ 、_________ 处(填“A”“B”“C”或“D”),将③均匀分散在乙醇中(已知碳酸钙不溶于乙醇)得到的分散系为_________ 。
(3)上述物质间发生的化学反应,能用 表示的是
表示的是_________ (填化学方程式)。
(4)电解质溶液中离子导电能力的强弱可用离子的摩尔电导率来衡量,摩尔电导率数值越大,离子在溶液中的导电能力越强。已知 、
、 、
、 、
、 、
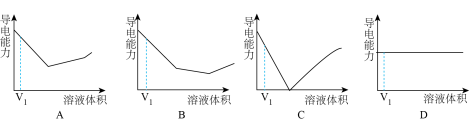
、 的摩尔电导率数值分别为34.98、19.8、7.98、6.36、5.01。据此判断,向②的溶液中滴加等物质的量浓度的①溶液,溶液导电能力变化趋势正确的是
的摩尔电导率数值分别为34.98、19.8、7.98、6.36、5.01。据此判断,向②的溶液中滴加等物质的量浓度的①溶液,溶液导电能力变化趋势正确的是_________ (填标号),滴加①的溶液体积为 时,发生反应的离子方程式为
时,发生反应的离子方程式为_________ 。

已知:纳米颗粒是指颗粒直径在1~100nm之间的微粒。
(1)类别1是
(2)按照上述分类图示,物质③应填入图中
(3)上述物质间发生的化学反应,能用
 表示的是
表示的是(4)电解质溶液中离子导电能力的强弱可用离子的摩尔电导率来衡量,摩尔电导率数值越大,离子在溶液中的导电能力越强。已知
 、
、 、
、 、
、 、
、 的摩尔电导率数值分别为34.98、19.8、7.98、6.36、5.01。据此判断,向②的溶液中滴加等物质的量浓度的①溶液,溶液导电能力变化趋势正确的是
的摩尔电导率数值分别为34.98、19.8、7.98、6.36、5.01。据此判断,向②的溶液中滴加等物质的量浓度的①溶液,溶液导电能力变化趋势正确的是 时,发生反应的离子方程式为
时,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】在一定温度下,对冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答下列问题:
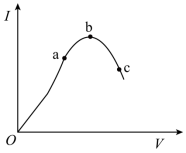
(1)在一定温度下,向上述醋酸溶液中,加入加水稀释,按要求填空。
①电离平衡将________ (填“向电离方向”、“向生成醋酸分子方向”或“不”)移动;
②醋酸的平衡常数Ka将__________ (填“增大”、“减小”或“不变”)
(2)a、b、c三点对应的溶液中,c(H+)最小为___________ 。
(3)a、b、c三点对应的溶液中,CH3COOH的电离程度最大的是___________ 。
(4)若使c点对应的溶液中的c(CH3COO-)增大,则下列措施中,可行的是 (填字母,下同)。
(5)部分弱酸的电离平衡常数如下表:
①依据表格中三种酸的电离常数,判断三种酸酸性强弱的顺序为_____________________ 。
②向NaCN溶液中通入CO2气体,反应的化学方程式为__________________ 。

(1)在一定温度下,向上述醋酸溶液中,加入加水稀释,按要求填空。
①电离平衡将
②醋酸的平衡常数Ka将
(2)a、b、c三点对应的溶液中,c(H+)最小为
(3)a、b、c三点对应的溶液中,CH3COOH的电离程度最大的是
(4)若使c点对应的溶液中的c(CH3COO-)增大,则下列措施中,可行的是 (填字母,下同)。
| A.加热 | B.加入NaOH稀溶液 | C.加入K2CO3固体 | D.加水 |
| 弱酸 |  |  |  |
| 电离平衡常数 (25℃) | 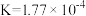 | 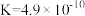 |  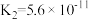 |
②向NaCN溶液中通入CO2气体,反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如图。____________ 。
(2)a、b、c三点酸性由大到小的顺序为______________ 。
(3)若使c点溶液中的c(CH3COO-)提高,在如下措施中,可选_____________ 。
A.加热
B.加很稀的NaOH溶液
C.加固体KOH
D.加水
E.加固体CH3COONa
F.加Zn粒
(4)在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是__________ 。
A.c(H+) B.H+个数
C.CH3COOH分子数D.c(H+)/c(CH3COOH)

(2)a、b、c三点酸性由大到小的顺序为
(3)若使c点溶液中的c(CH3COO-)提高,在如下措施中,可选
A.加热
B.加很稀的NaOH溶液
C.加固体KOH
D.加水
E.加固体CH3COONa
F.加Zn粒
(4)在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是
A.c(H+) B.H+个数
C.CH3COOH分子数D.c(H+)/c(CH3COOH)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】回答下列问题:
(1)为了证明醋酸是弱电解质,某同学分别取pH=3醋酸和盐酸各1mL,分别用蒸馏水稀释到100mL,然后用pH试纸分别测定两溶液的pH,则可认定醋酸是弱电解质,判断的依据是_______ 。
(2)已知室温时,0.1 mol∙L−1某一元酸HA在水中有0.1%发生电离,回答下列问题:
①该溶液中c(H+)=_______ mol∙L−1。
②HA的电离平衡常数K=_______ 。
③由HA电离出的c(H+)约为水电离出的c(H+)的_______ 倍。
(3)部分弱酸的电离平衡常数如下表:
①在相同浓度的HCOOH和HClO的溶液中,用“>”“<”或“=”填空。
溶液导电能力:HCOOH_______ HClO。
② 的电离平衡常数表达式为
的电离平衡常数表达式为_______
③将少量CO2气体通入NaClO溶液中,写出该反应离子方程式_______ 。
(4)某浓度的氨水中存在平衡:NH3·H2O
 +OH-,如想增大
+OH-,如想增大 的浓度而不增大OH-的浓度,应采取的措施是
的浓度而不增大OH-的浓度,应采取的措施是_______ (填字母)。
a.适当升高温度 b.加入NH4Cl固体 c.通入NH3 d.加入少量浓盐酸
(1)为了证明醋酸是弱电解质,某同学分别取pH=3醋酸和盐酸各1mL,分别用蒸馏水稀释到100mL,然后用pH试纸分别测定两溶液的pH,则可认定醋酸是弱电解质,判断的依据是
(2)已知室温时,0.1 mol∙L−1某一元酸HA在水中有0.1%发生电离,回答下列问题:
①该溶液中c(H+)=
②HA的电离平衡常数K=
③由HA电离出的c(H+)约为水电离出的c(H+)的
(3)部分弱酸的电离平衡常数如下表:
弱酸 | HCOOH | H2CO3 | HClO |
电离平衡常数/25 ℃ | K=1.77×10-4 | K1=4.4×10-7 K2=4.7×10-11 | 3.0×10-8 |
溶液导电能力:HCOOH
②
 的电离平衡常数表达式为
的电离平衡常数表达式为③将少量CO2气体通入NaClO溶液中,写出该反应离子方程式
(4)某浓度的氨水中存在平衡:NH3·H2O

 +OH-,如想增大
+OH-,如想增大 的浓度而不增大OH-的浓度,应采取的措施是
的浓度而不增大OH-的浓度,应采取的措施是a.适当升高温度 b.加入NH4Cl固体 c.通入NH3 d.加入少量浓盐酸
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】人类食用醋的历史已有10000多年,有关醋的文字记载也至少有3000年,醋和食盐一样属于最古老的调味品。
Ⅰ.某兴趣小组为确定 是弱电解质并分析其中的变化,设计如下实验方案。
是弱电解质并分析其中的变化,设计如下实验方案。
方案一:如图所示,取纯度、质量、大小相同的锌粒于两只相同气球中,同时将锌粒分别加入盛有10mL 溶液和稀盐酸的试管中,充分反应。
溶液和稀盐酸的试管中,充分反应。
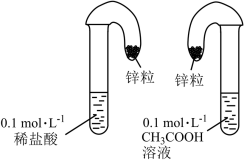
方案二:用pH计测定浓度为0.1 的
的 溶液的pH。
溶液的pH。
方案三:配制pH=3的 溶液250mL,取5mL稀释至500mL,再用pH计测其pH。
溶液250mL,取5mL稀释至500mL,再用pH计测其pH。
回答下列问题:
(1)方案一中,说明 是弱电解质的实验现象是
是弱电解质的实验现象是___________ (填字母)。
a.两个试管上方的气球同时鼓起,且体积一样大
b.装有盐酸的试管上方的气球鼓起慢
c.装有 的试管上方的气球鼓起慢
的试管上方的气球鼓起慢
d.装有 的试管上方的气球鼓起体积小
的试管上方的气球鼓起体积小
(2)方案二中,测得0.1 的
的 溶液的pH
溶液的pH___________ 1(填“>”“<”或“=”)。
(3)方案三中,所得醋酸溶液与pH=5的盐酸溶液,比较c(CH3COO-)___________ c(Cl-)(填“>”“<”或“=”)。
Ⅱ.完成下列问题
(4)根据 在溶液中的电离平衡移动的原理分析,为使
在溶液中的电离平衡移动的原理分析,为使 的电离程度和
的电离程度和 都减小,
都减小,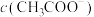 增加,可向0.1
增加,可向0.1 的
的 溶液中,选择加入的试剂是
溶液中,选择加入的试剂是___________ (填化学式)。
(5)常温下0.1mol•L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是___________ (填选项字母,下同)。
A.c(H+) B.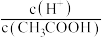 C.c(H+)∙c(OH-) D.
C.c(H+)∙c(OH-) D. E.
E.
若该溶液升高温度,上述5种表达式的数据一定增大的是___________ 。
(6)25℃时,将amolL-1的醋酸溶液与bmolL-1氢氧化钠溶液等体积混合,反应后溶液恰好显中性,则溶液中c(Na+)___________ c(CH3COO-)(填写“>”、“=”或“<”)。
Ⅰ.某兴趣小组为确定
 是弱电解质并分析其中的变化,设计如下实验方案。
是弱电解质并分析其中的变化,设计如下实验方案。方案一:如图所示,取纯度、质量、大小相同的锌粒于两只相同气球中,同时将锌粒分别加入盛有10mL
 溶液和稀盐酸的试管中,充分反应。
溶液和稀盐酸的试管中,充分反应。
方案二:用pH计测定浓度为0.1
 的
的 溶液的pH。
溶液的pH。方案三:配制pH=3的
 溶液250mL,取5mL稀释至500mL,再用pH计测其pH。
溶液250mL,取5mL稀释至500mL,再用pH计测其pH。回答下列问题:
(1)方案一中,说明
 是弱电解质的实验现象是
是弱电解质的实验现象是a.两个试管上方的气球同时鼓起,且体积一样大
b.装有盐酸的试管上方的气球鼓起慢
c.装有
 的试管上方的气球鼓起慢
的试管上方的气球鼓起慢d.装有
 的试管上方的气球鼓起体积小
的试管上方的气球鼓起体积小(2)方案二中,测得0.1
 的
的 溶液的pH
溶液的pH(3)方案三中,所得醋酸溶液与pH=5的盐酸溶液,比较c(CH3COO-)
Ⅱ.完成下列问题
(4)根据
 在溶液中的电离平衡移动的原理分析,为使
在溶液中的电离平衡移动的原理分析,为使 的电离程度和
的电离程度和 都减小,
都减小,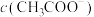 增加,可向0.1
增加,可向0.1 的
的 溶液中,选择加入的试剂是
溶液中,选择加入的试剂是(5)常温下0.1mol•L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是
A.c(H+) B.
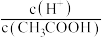 C.c(H+)∙c(OH-) D.
C.c(H+)∙c(OH-) D. E.
E.
若该溶液升高温度,上述5种表达式的数据一定增大的是
(6)25℃时,将amolL-1的醋酸溶液与bmolL-1氢氧化钠溶液等体积混合,反应后溶液恰好显中性,则溶液中c(Na+)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】Ⅰ.现有下列物质:
①盐酸 ②蔗糖 ③氨水 ④Fe(OH)3 ⑤CH3COOH ⑥Cu ⑦氯水 ⑧CaCO3 ⑨H2CO3 ⑩HNO3
(1)上述物质中属于强电解质的有_______ (填序号,下同),属于弱电解质的有_______
(2)写出下列物质的电离方程式:④_______ ;⑧_______ 。
Ⅱ.已知室温时,0.1mol/L醋酸溶液在水中电离度为0.02%,回答下列各问题:
(3)该溶液中c(H+)=_______ ;该溶液的电离平衡常数K=_______ 。
(4)写出醋酸的电离方程式:_______ ;
(5)向0.1mol/L醋酸溶液中加入少量水,电离平衡向_______ 移动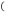 填“左”或“右”
填“左”或“右”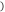 ;n(CH3COOH)
;n(CH3COOH)_______ 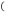 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变”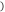 ;c(CH3COO-)/c(CH3COOH)
;c(CH3COO-)/c(CH3COOH) _______ 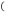 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。
(6)已知25℃时部分弱电解质的电离平衡常数数据如表所示:
以下说法不正确的是_______。 填选项
填选项
①盐酸 ②蔗糖 ③氨水 ④Fe(OH)3 ⑤CH3COOH ⑥Cu ⑦氯水 ⑧CaCO3 ⑨H2CO3 ⑩HNO3
(1)上述物质中属于强电解质的有
(2)写出下列物质的电离方程式:④
Ⅱ.已知室温时,0.1mol/L醋酸溶液在水中电离度为0.02%,回答下列各问题:
(3)该溶液中c(H+)=
(4)写出醋酸的电离方程式:
(5)向0.1mol/L醋酸溶液中加入少量水,电离平衡向
 填“左”或“右”
填“左”或“右” ;n(CH3COOH)
;n(CH3COOH) 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” ;c(CH3COO-)/c(CH3COOH)
;c(CH3COO-)/c(CH3COOH)  填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。(6)已知25℃时部分弱电解质的电离平衡常数数据如表所示:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7、Ka2=5.6×10-11 | Ka=3.0×10-8 |
以下说法不正确的是_______。
 填选项
填选项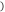
| A.向弱酸溶液中加入少量NaOH溶液,电离平衡常数变大 |
| B.多元弱酸的酸性主要由第一步电离决定 |
| C.表中三种酸,酸性最强的是CH3COOH |
| D.向NaClO溶液中通入CO2气体,可以生成HClO |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如图。____________ 。
(2)a、b、c三点酸性由大到小的顺序为______________ 。
(3)若使c点溶液中的c(CH3COO-)提高,在如下措施中,可选_____________ 。
A.加热
B.加很稀的NaOH溶液
C.加固体KOH
D.加水
E.加固体CH3COONa
F.加Zn粒
(4)在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是__________ 。
A.c(H+) B.H+个数
C.CH3COOH分子数D.c(H+)/c(CH3COOH)

(2)a、b、c三点酸性由大到小的顺序为
(3)若使c点溶液中的c(CH3COO-)提高,在如下措施中,可选
A.加热
B.加很稀的NaOH溶液
C.加固体KOH
D.加水
E.加固体CH3COONa
F.加Zn粒
(4)在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是
A.c(H+) B.H+个数
C.CH3COOH分子数D.c(H+)/c(CH3COOH)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】25℃时,50mL0.1mol/L醋酸中存在下述平衡:____________________________
若分别作如下改变,对上述平衡有何影响?
⑴加入少量冰醋酸,平衡将_________ ,溶液中c(H+)将________ (增大、减小、不变);
⑵加入一定量蒸馏水,平衡将_________ ,溶液中c(H+)将________ (增大、减小、不变)
⑶加入少量0.1mol/L盐酸,平衡将_________ ,溶液中c(H+)将________ (增大、减小、不变)
⑷加入20mL0.10mol/LNaCl,平衡将_________ ,溶液中c(H+)将________ (增大、减小、不变)
若分别作如下改变,对上述平衡有何影响?
⑴加入少量冰醋酸,平衡将
⑵加入一定量蒸馏水,平衡将
⑶加入少量0.1mol/L盐酸,平衡将
⑷加入20mL0.10mol/LNaCl,平衡将
您最近一年使用:0次

 溶液是实验室中的常用试剂。
溶液是实验室中的常用试剂。
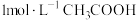 溶液的
溶液的 ,由此确定
,由此确定

