下列有关物质性质的叙述正确的是
| A.Al和Mg均为第三周期金属元素,常用电解熔融AlCl3的方法制备Al |
| B.紫色石蕊遇浓硝酸先变红色,后红色褪色,该现象说明浓硝酸具有酸性和氧化性 |
| C.向淀粉一KI溶液中通入过量的氯气,溶液先变蓝色,后蓝色褪去,该现象说明Cl2具有漂白性 |
| D.Li和Na均为I A金属元素,二者在氧气中燃烧分别生成Li2O2和Na2O2 |
更新时间:2021-12-03 09:29:44
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】常温常压下, 为棕黄色气体(沸点为3.8℃),42℃以上会分解生成
为棕黄色气体(沸点为3.8℃),42℃以上会分解生成 和
和 ,
, 易溶于水并与水反应生成
易溶于水并与水反应生成 。现将氯气和空气(不参与反应)按体积比
。现将氯气和空气(不参与反应)按体积比 混合通入含水8%的碳酸钠中制备
混合通入含水8%的碳酸钠中制备 ,并用水吸收后得次氯酸溶液。
,并用水吸收后得次氯酸溶液。
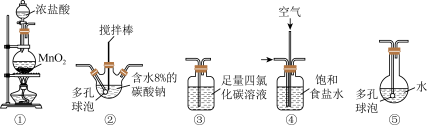
下列说法不正确的是
 为棕黄色气体(沸点为3.8℃),42℃以上会分解生成
为棕黄色气体(沸点为3.8℃),42℃以上会分解生成 和
和 ,
, 易溶于水并与水反应生成
易溶于水并与水反应生成 。现将氯气和空气(不参与反应)按体积比
。现将氯气和空气(不参与反应)按体积比 混合通入含水8%的碳酸钠中制备
混合通入含水8%的碳酸钠中制备 ,并用水吸收后得次氯酸溶液。
,并用水吸收后得次氯酸溶液。
下列说法不正确的是
| A.装置的连接顺序为①→④→②→③→⑤ |
B.装置②应采用水控温,防止反应放热引起 分解 分解 |
| C.氯气直接溶于水制备次氯酸溶液的方法,比本题目的方法简便且次氯酸更纯浓度更高 |
| D.两处多孔球泡的作用均是为了加快反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列离子方程式书写正确的是
| A.铁与稀盐酸反应:Fe+6H+=Fe3++3H2↑ |
| B.氯气与氯化亚铁溶液反应:Cl2+Fe2+=Fe3++2Cl- |
| C.氯化铁溶液与铜反应:3Cu+2Fe3+=2Fe+3Cu2+ |
| D.氯化铁溶液与硫化氢反应:2Fe3++H2S=2Fe2++S↓+2H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关实验操作、现象和解释或结论都正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 已知H3BO3=5.8×10-10,H2CO3K2=4.7×10-11,向饱和硼酸溶液中滴加碳酸钠溶液 | 无明显现象 | 硼酸不与碳酸钠反应 |
| B | AgI沉淀中滴入稀KCl | 有白色沉淀出现 | AgCl比AgI更难溶 |
| C | Al箔插入稀HNO3中 | 无现象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
| D | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | 析出了NaHCO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】以下指定反应中,浓硝酸既表现氧化性又表现酸性的是
| A.浓硝酸中滴入紫色石蕊试液(先变红后褪色) | B.氧化铁与浓硝酸反应 |
| C.氢氧化铜与浓硝酸反应 | D.碳与浓硝酸反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】将一块新切开的钠放在玻璃片上,可观察到发生的一系列的变化:表面迅速变暗→“出汗” →变成白色粉末,下列有关叙述正确的是
| A.表面迅速变暗是因为钠与空气中的氧气反应生成了过氧化钠 |
| B.“出汗” 是因为生成的氢氧化钠吸收空气中的水蒸气在表面形成溶液 |
| C.最后生成的白色粉末主要成分是碳酸氢钠 |
| D.该过程的所有变化均为物理变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列关于Na2O和Na2O2的说法中,不正确 的是
| A.Na2O与Na2O2中的阴阳离子比均为1:2 |
| B.Na2O2可在呼吸面具或潜水艇中作为氧气的来源 |
| C.钠放置在空气中,会迅速被氧化而生成白色的氧化钠 |
| D.Na2O2与Na2O都能与水反应生成碱,都属于碱性氧化物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】用无机矿物资源生产部分材料,其产品流程示意图如下。下列有关说法错误的是


| A.制取玻璃和粗硅时生成的气体产物均为CO2 |
| B.生产铝、铜及高纯硅的过程中都涉及氧化还原反应 |
| C.粗硅制高纯硅时,提纯四氯化硅可用多次蒸馏的方法 |
| D.黄铜矿冶炼铜时产生的SO2可用于生产硫酸,FeO可用作冶炼铁的原料 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】工业上用铝土矿(主要成分为Al2O3,含Fe2O3等杂质)为原料冶炼铝的工艺流程如下:
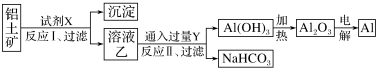
下列分析判断正确的是( )

下列分析判断正确的是( )
| A.试剂X为稀硫酸 |
| B.反应Ⅱ中生成Al(OH)3的反应为CO2+AlO2-+2H2O===Al(OH)3↓+HCO3- |
| C.Al2O3熔点很高,工业上还可采用电解熔融AlCl3的方法冶炼金属A1 |
| D.工业上可用冶炼出的金属铝来还原Fe2O3而冶炼出金属铁 |
您最近一年使用:0次

 )可能为
)可能为 NO
NO HNO3
HNO3 + H2O
+ H2O 、
、
 溶液
溶液
 的速率加快
的速率加快

