写出下列离子的电子式
Mg2+___________ 、O2-___________ 、F-___________ 、Al3+___________ 、S2-___________ 。
Mg2+
21-22高一·全国·课时练习 查看更多[1]
(已下线)5.2.1 离子键-2021-2022学年高一化学10分钟课前预习练(苏教版2019必修第一册)
更新时间:2021-12-06 17:22:08
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】I.填空。
(1)人体的胃液中含有适量的盐酸,可以帮助消化。如果胃酸过多则需要服用药物,这些药物的主要成分可以是___________ (填字母序号)。
A.NaOH B. C.碳酸氢钠
C.碳酸氢钠
(2)人体体液中含有的最常见的电解质之一是氯化钠,目前我们食用的食盐中常常加入碘酸钾( ),其目的是防止人体缺碘。写出碘酸钾在水溶液中的电离方程式:
),其目的是防止人体缺碘。写出碘酸钾在水溶液中的电离方程式:___________ 。
(3)人体血液中含有下列物质,其中不属于电解质的是___________(填字母序号)。
II.有A、B、C、D四种化合物,分别由 、
、 、
、 、
、 、
、 中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(4)推断A、B、C、D的化学式。
A___________ ,B___________ ,C___________ ,D___________ 。
(5)写出下列反应的离子方程式。
B与盐酸反应:___________ ,
C与硫酸反应:___________ ,
E(少量)与澄清石灰水反应:___________ 。
(1)人体的胃液中含有适量的盐酸,可以帮助消化。如果胃酸过多则需要服用药物,这些药物的主要成分可以是
A.NaOH B.
 C.碳酸氢钠
C.碳酸氢钠(2)人体体液中含有的最常见的电解质之一是氯化钠,目前我们食用的食盐中常常加入碘酸钾(
 ),其目的是防止人体缺碘。写出碘酸钾在水溶液中的电离方程式:
),其目的是防止人体缺碘。写出碘酸钾在水溶液中的电离方程式:(3)人体血液中含有下列物质,其中不属于电解质的是___________(填字母序号)。
A. | B.水 | C.碳酸氢钠 | D.葡萄糖 |
II.有A、B、C、D四种化合物,分别由
 、
、 、
、 、
、 、
、 中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。(4)推断A、B、C、D的化学式。
A
(5)写出下列反应的离子方程式。
B与盐酸反应:
C与硫酸反应:
E(少量)与澄清石灰水反应:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按要求回答下列问题:
(1)写出漂白粉的有效成分的化学式_______ 。
(2)写出CaCl2的电子式_______ 。
(3)写出CO2的结构式_______ 。
(4)写出红热的铁与水蒸气反应的化学方程式_______ 。
(1)写出漂白粉的有效成分的化学式
(2)写出CaCl2的电子式
(3)写出CO2的结构式
(4)写出红热的铁与水蒸气反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的化学符号:________ 。
(2)周期表中位于第8纵行的铁元素属于第________ 族。
(3)下列几种物质:①Ca(OH)2②H2O2③He④H2S ⑤MgCl2 ,只含有离子键的是(选填序号,下同)_________ ;只含有极性共价键的化合物是________ ;
(4)HClO的结构式______ ,I2的电子式______ 。
(5)下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④蔗糖溶液水⑤硫酸溶于水;未破坏化学键的是_____ ;
(6)下列不能说明氯元素原子得电子能力比硫元素原子得电子能力强的是_____________
①HCl的溶解度比H2S的大 ②HCl的酸性比H2S的强 ③HCl的稳定性比H2S的强④Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑤HClO4的酸性比H2SO4的强 ⑥Cl2能与H2S反应生成S
(1)写出表示含有8个质子、10个中子的原子的化学符号:
(2)周期表中位于第8纵行的铁元素属于第
(3)下列几种物质:①Ca(OH)2②H2O2③He④H2S ⑤MgCl2 ,只含有离子键的是(选填序号,下同)
(4)HClO的结构式
(5)下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④蔗糖溶液水⑤硫酸溶于水;未破坏化学键的是
(6)下列不能说明氯元素原子得电子能力比硫元素原子得电子能力强的是
①HCl的溶解度比H2S的大 ②HCl的酸性比H2S的强 ③HCl的稳定性比H2S的强④Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑤HClO4的酸性比H2SO4的强 ⑥Cl2能与H2S反应生成S
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】按要求填空:
(1)甲烷分子的电子式:___________ ;
(2)乙烯分子的结构式:___________ ;
(3)葡萄糖的分子式:___________ ;
(4)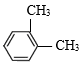 的名称:
的名称:___________ ;
(5)—OH的名称:___________ ;
(6)乙酸分子的结构简式___________ 。
(1)甲烷分子的电子式:
(2)乙烯分子的结构式:
(3)葡萄糖的分子式:
(4)
 的名称:
的名称:(5)—OH的名称:
(6)乙酸分子的结构简式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】画出下列微粒的结构示意图和电子式。
氧离子______________ ,______________
氯离子______________ ,______________
碳原子______________ ,______________
钙离子______________ ,______________
氧离子
氯离子
碳原子
钙离子
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】下图是元素周期表的一部分,用化学用语回答下列问题:

(1)元素Fe在周期表中的位置为________ 。
(2)⑦与⑧形成的化合物中各原子均满足8电子稳定结构的是_____ 。(用化学式表示)
(3)④、⑦、⑧三种元素的非金属性由强到弱的顺序是________ 。(用元素符号表示)
(4)用电子式表示含元素⑥的10电子二元化合物的形成过程________ 。
(5)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为_________ 。

(1)元素Fe在周期表中的位置为
(2)⑦与⑧形成的化合物中各原子均满足8电子稳定结构的是
(3)④、⑦、⑧三种元素的非金属性由强到弱的顺序是
(4)用电子式表示含元素⑥的10电子二元化合物的形成过程
(5)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】请回答下列问题
(1)①NaOH的电子式___________ ;②NH3的电子式:___________ ;③CO2的结构式___________ 。
(2)用离子方程式表示覆铜板制作印刷电路板:___________ 。
(3)已知氧化性:Br2>Fe3+,向FeBr2溶液中通入等物质的量的Cl2,写出离子方程式___________ 。
(1)①NaOH的电子式
(2)用离子方程式表示覆铜板制作印刷电路板:
(3)已知氧化性:Br2>Fe3+,向FeBr2溶液中通入等物质的量的Cl2,写出离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】阅读分析下列两个材料:
材料一
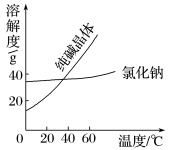
材料二
(1)用微粒符号表示下列微粒。
根据上述材料,将下列混合物分离的方法填在横线上(选填编号):
A.蒸馏法 B.萃取法 C.冷却结晶法 D.分液法
(2)从含氯化钠杂质的纯碱中分离出纯碱,最好选用________ ;
(3)将乙二醇和丙三醇分离的最佳方法是________ 。
材料三:
溴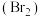 与碘
与碘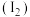 溶解性相似,其稀的水溶液呈黄色。
溶解性相似,其稀的水溶液呈黄色。
(4)从溴水中提取溴的方法是________ ,将溴水移入________ (填仪器名称)中,加入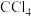 充分振荡并静置,
充分振荡并静置,________ (选填“上层”或“下层”)液体的颜色较深。
(5)若观察发现提取溴以后的水还有颜色,解决该问题的方法是________ 。
材料一

材料二
| 物质 | 熔点/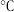 | 沸点/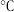 | 密度/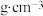 | 溶解性 |
乙二醇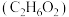 | 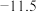 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇 | 17.9 | 290 | 1.26 | 与水、乙醇以任意比互溶 |
| 结构示意图 | 电子式 | |
| 钠离子 | ||
| 氯原子 |
根据上述材料,将下列混合物分离的方法填在横线上(选填编号):
A.蒸馏法 B.萃取法 C.冷却结晶法 D.分液法
(2)从含氯化钠杂质的纯碱中分离出纯碱,最好选用
(3)将乙二醇和丙三醇分离的最佳方法是
材料三:
溴
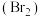 与碘
与碘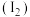 溶解性相似,其稀的水溶液呈黄色。
溶解性相似,其稀的水溶液呈黄色。(4)从溴水中提取溴的方法是
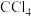 充分振荡并静置,
充分振荡并静置,(5)若观察发现提取溴以后的水还有颜色,解决该问题的方法是
您最近一年使用:0次



