某强酸性溶液X中可能含有Fe2+、Fe3+、Al3+、Ba2+、 、
、 、
、 、
、 、
、 中的若干种,现取X溶液进行连续实验,实验过程及产物如图所示。实验过程中有一种气体为红棕色。
中的若干种,现取X溶液进行连续实验,实验过程及产物如图所示。实验过程中有一种气体为红棕色。
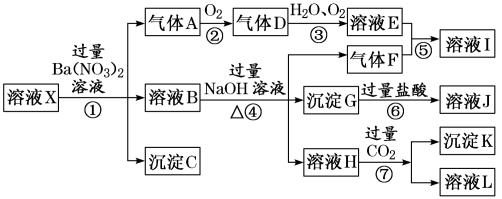
根据以上信息,回答下列问题:
(1)由强酸性条件即可判断X溶液中肯定不存在的离子有___________ 。
(2)溶液X中关于硝酸根离子的判断,正确的是___________ (填编号,下同)。
a.一定含有 b.一定不含有 c.可能含有
(3)转化①的离子方程式为___________ 。转化⑦的离子方程式为___________ 。
(4)在溶液J中通入二氧化硫气体,请写出反应的离子方程式___________ 。
 、
、 、
、 、
、 、
、 中的若干种,现取X溶液进行连续实验,实验过程及产物如图所示。实验过程中有一种气体为红棕色。
中的若干种,现取X溶液进行连续实验,实验过程及产物如图所示。实验过程中有一种气体为红棕色。
根据以上信息,回答下列问题:
(1)由强酸性条件即可判断X溶液中肯定不存在的离子有
(2)溶液X中关于硝酸根离子的判断,正确的是
a.一定含有 b.一定不含有 c.可能含有
(3)转化①的离子方程式为
(4)在溶液J中通入二氧化硫气体,请写出反应的离子方程式
更新时间:2021-11-05 08:57:06
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】有一瓶无色澄清的溶液,可能由以下离子中的几种组成:SO32-、I-、CO32-、Cl-、SO42-、Fe2+、Na+、MnO4-,请根据以下实验步骤及现象回答问题:
步骤一:取适量待测液,加入足量稀盐酸,产生有刺激性气味的气体A和溶液B。
步骤二:往B中加入足量BaCl2溶液,得白色沉淀和溶液C。
步骤三:往C溶液中通入足量Cl2,得黄褐色溶液D。
(1)该溶液中一定存在的离子是:_______ 。
(2)该溶液中可能存在的阴离子是:_______ 。
(3)步骤三中溶液变黄褐色是因为生成了某种物质,确认该物质的实验操作与现象是:取适量D溶液于试管中,_______ 。
步骤一:取适量待测液,加入足量稀盐酸,产生有刺激性气味的气体A和溶液B。
步骤二:往B中加入足量BaCl2溶液,得白色沉淀和溶液C。
步骤三:往C溶液中通入足量Cl2,得黄褐色溶液D。
(1)该溶液中一定存在的离子是:
(2)该溶液中可能存在的阴离子是:
(3)步骤三中溶液变黄褐色是因为生成了某种物质,确认该物质的实验操作与现象是:取适量D溶液于试管中,
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某河道两旁有甲乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、C1-、OH-、NO3-六种离子。
(1)甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子_________ 、________ 、_________ 。
(2)乙厂的废水中含有另外三种离子。对于该两厂的废水,可采取下列两种方法来处理。如果在乙厂废水中加一定量_________ (选填:活性炭或铁粉),离子方程式是________ ,并且能够回收其中的金属____________ (填写金属元素符号)。
(1)甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子
(2)乙厂的废水中含有另外三种离子。对于该两厂的废水,可采取下列两种方法来处理。如果在乙厂废水中加一定量
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】I.离子反应是中学化学中重要的反应类型,回答下列问题:
(1)将两种化合物一起溶于水得到一种无色透明溶液,溶液中含有下列离子中的某些离子:K+、Mg2+、Fe3+、Ba2+、SO 、OH-、CO
、OH-、CO 和Cl-,取该溶液进行如下实验:
和Cl-,取该溶液进行如下实验:
I.取少量溶液滴入紫色石蕊试液,溶液呈蓝色。
II.取少许溶液滴入BaCl2溶液,无白色沉淀产生。
III.取少许溶液先滴加硝酸再加AgNO3溶液,产生白色沉淀。
IV.再取少许原溶液滴入少量H2SO4溶液,有白色沉淀产生。
①根据以上现象判断,原溶液中肯定不存在的离子是_______ 。
②如溶液中各种离子数相等,确定溶液中_______ (填有或无)K+。判断依据是_______ 。
II.当温度和压强一定时,向KOH、Ba(OH)2混合溶液中通入足量的CO2气体,随CO2的通入生成的沉淀质量如图所示:
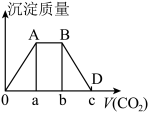
(2)实验室制取二氧化碳的离子方程式:________ 。
(3)根据图像可知,随着CO2通入KOH、Ba(OH)2混合溶液,反应分多个阶段,AB阶段的离子反应方程式:_______ 。
(4)随着CO2的通入,(不考虑CO2在溶液中的溶解,忽略溶液体积的微小变化)混合溶液的导电性会发生一些变化,导电性:0点_______ D点(填“大于”、“等于”或“小于”)。
(5)0A段和BD段消耗CO2用量的关系:_________ (用a、b和c表示)。
(6)原溶液中Ba2+和OH-的个数之比:_______ (用a、b和c表示)。
(1)将两种化合物一起溶于水得到一种无色透明溶液,溶液中含有下列离子中的某些离子:K+、Mg2+、Fe3+、Ba2+、SO
 、OH-、CO
、OH-、CO 和Cl-,取该溶液进行如下实验:
和Cl-,取该溶液进行如下实验:I.取少量溶液滴入紫色石蕊试液,溶液呈蓝色。
II.取少许溶液滴入BaCl2溶液,无白色沉淀产生。
III.取少许溶液先滴加硝酸再加AgNO3溶液,产生白色沉淀。
IV.再取少许原溶液滴入少量H2SO4溶液,有白色沉淀产生。
①根据以上现象判断,原溶液中肯定不存在的离子是
②如溶液中各种离子数相等,确定溶液中
II.当温度和压强一定时,向KOH、Ba(OH)2混合溶液中通入足量的CO2气体,随CO2的通入生成的沉淀质量如图所示:

(2)实验室制取二氧化碳的离子方程式:
(3)根据图像可知,随着CO2通入KOH、Ba(OH)2混合溶液,反应分多个阶段,AB阶段的离子反应方程式:
(4)随着CO2的通入,(不考虑CO2在溶液中的溶解,忽略溶液体积的微小变化)混合溶液的导电性会发生一些变化,导电性:0点
(5)0A段和BD段消耗CO2用量的关系:
(6)原溶液中Ba2+和OH-的个数之比:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】一包白色粉末中可能含有NaCl、Ba(NO3)2、CuSO4、Na2CO3,现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,滤液呈无色
②向①中的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生
试根据上述实验现象判断,原白色粉末中:
(1)一定含有的物质是___________ ,
(2)一定不含的物质是___________ ,
(3)可能含有的物质是___________ (以上物质均写化学式)
(4)第②步反应中离子方程式为:___________
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,滤液呈无色
②向①中的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生
试根据上述实验现象判断,原白色粉末中:
(1)一定含有的物质是
(2)一定不含的物质是
(3)可能含有的物质是
(4)第②步反应中离子方程式为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】食盐中含有一定量的镁、铁等杂质,加碘盐可能含有K+、IO3-、I-、Mg2+.加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热引起的。
已知:IO3-+5I-+6H+→3I2+3H2O,2Fe3++2I-→2Fe2++I2,KI+I2⇌KI3;氧化性:IO3->Fe3+>I2。
(1)学生甲对某加碘盐进行如下实验,以确定该加碘盐中碘元素的存在形式。取一定量加碘盐,用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3份。第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,加入CCl4,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。
①第一份试液中,加KSCN溶液显红色,该红色物质是______ (用化学式表示)。
②第二份试液中“加入CCl4”的实验操作名称为______ ,CCl4中显紫红色的物质是______ (用化学式表示)。
③根据这三次实验,学生甲得出以下结论:
在加碘盐中,除了Na+、Cl-以外,一定存在的离子是______ ,可能存在的离子是______ ,一定不存在的离子是______ 。由此可确定,该加碘盐中碘元素是______ 价(填化合价)的碘。
(2)将I2溶于KI溶液,在低温条件下,可制得KI3•H2O.该物质作为食盐加碘剂是否合适?______ (填“是”或“否”),并说明理由______ 。
(3)已知:I2+2S2O32-→2I-+S4O62-.学生乙用上述反应方程式测定食用精制盐的碘含量(假设不含Fe3+),其步骤为:
a.准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为2.0×10-3mol/L的Na2S2O3溶液10.0mL,恰好反应完全。
根据以上实验,学生乙所测精制盐的碘含量(以I元素计)是______ mg/kg(以含w的代数式表示)。
已知:IO3-+5I-+6H+→3I2+3H2O,2Fe3++2I-→2Fe2++I2,KI+I2⇌KI3;氧化性:IO3->Fe3+>I2。
(1)学生甲对某加碘盐进行如下实验,以确定该加碘盐中碘元素的存在形式。取一定量加碘盐,用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3份。第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,加入CCl4,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。
①第一份试液中,加KSCN溶液显红色,该红色物质是
②第二份试液中“加入CCl4”的实验操作名称为
③根据这三次实验,学生甲得出以下结论:
在加碘盐中,除了Na+、Cl-以外,一定存在的离子是
(2)将I2溶于KI溶液,在低温条件下,可制得KI3•H2O.该物质作为食盐加碘剂是否合适?
(3)已知:I2+2S2O32-→2I-+S4O62-.学生乙用上述反应方程式测定食用精制盐的碘含量(假设不含Fe3+),其步骤为:
a.准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为2.0×10-3mol/L的Na2S2O3溶液10.0mL,恰好反应完全。
根据以上实验,学生乙所测精制盐的碘含量(以I元素计)是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D 四种可溶性物质,它们的阳离子可能分别是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子可能分别是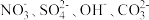 中的某一种。
中的某一种。
①若把4种物质分别溶解于盛有蒸馏水的4支试管中,均得澄清溶液,只有C溶液呈蓝色。
②若向①的4支试管中分别加盐酸,B溶液中有沉淀产生,D溶液中有无色无味气体逸出。
(1)根据①②的事实推断B的化学式为_______ ;
(2)C溶液中阴离子的检验方法:__________ ;
(3)将A溶液与D溶液混合使之恰好完全反应,将反应后混合物中两种物质分离的方法是___ ,在所得溶液中加入铝片,发生的离子反应方程式为:____________ ;有一块铝铁合金,将其溶于足量的盐酸中,再用过量的NaOH溶液处理,将产生的沉淀过滤、洗涤、干燥、灼烧,完全变成红色粉末后,经称量,红色粉末的质量恰好与合金的质量相等,则合金中铝的质量分数为__ ;
(4)D与稀硫酸反应生成的气体x用排空气法收集,测得体积为8.96 L(标准状况下),质量为15.2 g,该混合气体平均摩尔质量为_____ ,混合气体中x气体的体积分数为____ 。
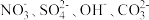 中的某一种。
中的某一种。①若把4种物质分别溶解于盛有蒸馏水的4支试管中,均得澄清溶液,只有C溶液呈蓝色。
②若向①的4支试管中分别加盐酸,B溶液中有沉淀产生,D溶液中有无色无味气体逸出。
(1)根据①②的事实推断B的化学式为
(2)C溶液中阴离子的检验方法:
(3)将A溶液与D溶液混合使之恰好完全反应,将反应后混合物中两种物质分离的方法是
(4)D与稀硫酸反应生成的气体x用排空气法收集,测得体积为8.96 L(标准状况下),质量为15.2 g,该混合气体平均摩尔质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某小组研究Cu和Fe(NO3)3溶液的反应原理。
(1)配制100mL 0.600mol·L-1 Fe(NO3)3溶液,需使用的仪器有_______(填标号)。
(2)提出假设
假设i:Fe(NO3)3溶液中的Fe3+将Cu氧化,反应的离子方程式为_______ ;
假设ii:Fe(NO3)3溶液中的NO 将Cu氧化,反应的离子方程式为3Cu+2NO
将Cu氧化,反应的离子方程式为3Cu+2NO +8H+=3Cu2++2NO↑+4H2O。
+8H+=3Cu2++2NO↑+4H2O。
(3)实验探究
实验Ⅰ:向0.600mol·L-1 Fe(NO3)3溶液中加入稍过量铜粉并不断振荡,溶液变成深棕色,无气泡产生。向上层清液中滴加2滴K3Fe(CN)6溶液,出现_______ ,说明有Fe2+生成。
实验Ⅱ:向0.200mol·L-1 HNO3溶液中加入稍过量铜粉并不断振荡,未见到明显淡蓝色。
已知:常温下,0.600mol·L-1 Fe(NO3)3溶液中的c(H+ )<0.200mol·L-1。
综合“实验Ⅰ”和“实验Ⅱ”,假设_______ (填 “i” 或 “ii” )一定成立。
(4)为探究“实验Ⅰ”中溶液变成深棕色的原因,设计了以下方案。请完成下表中的内容。
经分析推测,“实验I”中还存在以下反应:①3Fe2+ +NO +4H+=3Fe3+ +NO↑+2H2O;
+4H+=3Fe3+ +NO↑+2H2O;
②Fe2++NO=[Fe(NO)]2+(深棕色)。无气泡产生的原因是反应_______ (填“①”或“②”)的速率较快。
(1)配制100mL 0.600mol·L-1 Fe(NO3)3溶液,需使用的仪器有_______(填标号)。
A. | B. | C.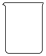 | D.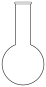 |
假设i:Fe(NO3)3溶液中的Fe3+将Cu氧化,反应的离子方程式为
假设ii:Fe(NO3)3溶液中的NO
 将Cu氧化,反应的离子方程式为3Cu+2NO
将Cu氧化,反应的离子方程式为3Cu+2NO +8H+=3Cu2++2NO↑+4H2O。
+8H+=3Cu2++2NO↑+4H2O。(3)实验探究
实验Ⅰ:向0.600mol·L-1 Fe(NO3)3溶液中加入稍过量铜粉并不断振荡,溶液变成深棕色,无气泡产生。向上层清液中滴加2滴K3Fe(CN)6溶液,出现
实验Ⅱ:向0.200mol·L-1 HNO3溶液中加入稍过量铜粉并不断振荡,未见到明显淡蓝色。
已知:常温下,0.600mol·L-1 Fe(NO3)3溶液中的c(H+ )<0.200mol·L-1。
综合“实验Ⅰ”和“实验Ⅱ”,假设
(4)为探究“实验Ⅰ”中溶液变成深棕色的原因,设计了以下方案。请完成下表中的内容。
| 序号 | 操作 | 现象 | 结论 |
| 实验Ⅲ | 向 | 溶液变成蓝色 | |
| 实验Ⅳ | 向0.600mol·L-1 Fe(NO3)3溶液中加入稍过量铜粉并不断振荡,用传感器检测反应过程中c(NO )的变化情况 )的变化情况 | 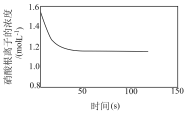 |
 +4H+=3Fe3+ +NO↑+2H2O;
+4H+=3Fe3+ +NO↑+2H2O;②Fe2++NO=[Fe(NO)]2+(深棕色)。无气泡产生的原因是反应
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】各物质间的转化关系如下图所示,请回答下列问题:
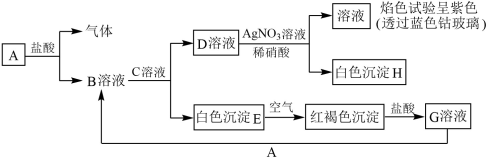
(1)写出B和D的化学式:B___________ ;D___________ 。
(2)写出E转变为F的化学方程式:___________ 。
(3)用KSCN鉴别G溶液的现象:___________ 。
(4)向G溶液中加入A,写出反应的离子方程式:___________ 。

(1)写出B和D的化学式:B
(2)写出E转变为F的化学方程式:
(3)用KSCN鉴别G溶液的现象:
(4)向G溶液中加入A,写出反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某实验小组对FeCl3溶液与Na2SO3溶液的反应进行探究。
已知:铁氰化钾的化学式为K3[Fe(CN)6],用于检验Fe2+,遇Fe2+离子产生蓝色沉淀
【实验1】
(1)配制FeCl3溶液时,先将FeCl3溶于浓盐酸,再稀释至指定浓度。从化学平衡角度说明浓盐酸的作用:__________ 。
【探究现象i产生的原因】
(2)甲同学认为发生反应:2Fe3++3 +6H2O
+6H2O 2Fe(OH)3(胶体)+3H2SO3;他取少量红褐色溶液于试管中,继续滴加1mol/LNa2SO3溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是
2Fe(OH)3(胶体)+3H2SO3;他取少量红褐色溶液于试管中,继续滴加1mol/LNa2SO3溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是_______ (填化学式)。
(3)乙同学认为还发生了氧化还原反应。他取少许红褐色溶液于试管中,加入______ ,有白色沉淀产生,证明产物中含有 。
。
丙同学认为乙同学的实验不严谨,因为在上述过程中 可能被其它物质氧化。为了进一步确认
可能被其它物质氧化。为了进一步确认 被氧化的原因,丙同学设计了实验2。
被氧化的原因,丙同学设计了实验2。
【实验2】用如图装置(a、b均为石墨电极)进行实验。闭合开关后灵敏电流计指针偏转。
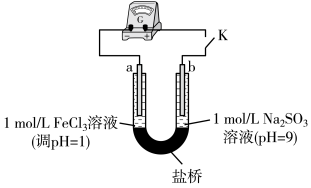
(4)实验2中正极的电极反应式为______ 。丙同学又用铁氰化钾溶液检验正极的产物,观察到有蓝色沉淀产生。他得出的结论是___________ 。
【解释现象ii产生的原因】
(5)综合上述结果,请从平衡移动角度解释,现象ii产生的原因为___________________ 。
已知:铁氰化钾的化学式为K3[Fe(CN)6],用于检验Fe2+,遇Fe2+离子产生蓝色沉淀
【实验1】
| 装置 | 实验现象 |
 | 现象i:一开始溶液颜色加深,由棕黄色变为红褐色。 现象ii:一段时间后溶液颜色变浅,变为浅黄色。 |
【探究现象i产生的原因】
(2)甲同学认为发生反应:2Fe3++3
 +6H2O
+6H2O 2Fe(OH)3(胶体)+3H2SO3;他取少量红褐色溶液于试管中,继续滴加1mol/LNa2SO3溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是
2Fe(OH)3(胶体)+3H2SO3;他取少量红褐色溶液于试管中,继续滴加1mol/LNa2SO3溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是(3)乙同学认为还发生了氧化还原反应。他取少许红褐色溶液于试管中,加入
 。
。丙同学认为乙同学的实验不严谨,因为在上述过程中
 可能被其它物质氧化。为了进一步确认
可能被其它物质氧化。为了进一步确认 被氧化的原因,丙同学设计了实验2。
被氧化的原因,丙同学设计了实验2。【实验2】用如图装置(a、b均为石墨电极)进行实验。闭合开关后灵敏电流计指针偏转。

(4)实验2中正极的电极反应式为
【解释现象ii产生的原因】
(5)综合上述结果,请从平衡移动角度解释,现象ii产生的原因为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、氯化钡溶液、碳酸钾溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,用小试管各盛少量多次进行两两混合反应,反应现象为:A与B、A与E均可产生白色沉淀,其中A与B反应所产生沉淀不溶于酸,A与E反应所生成的白色沉淀可以溶于C或D;B与D、B与E产生沉淀;E与C、E与D反应均可产生二氧化碳气体;而C与D由于属于同一类物质,混合时无反应现象。
由此,可判定各试剂瓶中所盛试剂为(用化学式表示)
A________ ;B________ ;C________ ;D________ ;E________ 。
另外,请写出下面要求的离子方程式:
(1)A与E:
________________________________________________________ 。
(2)A与B:
_________________________________________________________ 。
(3)C与E:
__________________________________________________________ 。
由此,可判定各试剂瓶中所盛试剂为(用化学式表示)
A
另外,请写出下面要求的离子方程式:
(1)A与E:
(2)A与B:
(3)C与E:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有一瓶澄清溶液,其中可能含有NH 、K+、Ba2+、Al3+、Fe3+、I-、NO
、K+、Ba2+、Al3+、Fe3+、I-、NO 、CO
、CO 、SO
、SO 、AlO
、AlO 。取该溶液进行以下实验:
。取该溶液进行以下实验:
①用pH试纸检验,溶液呈强酸性;
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色;
③另取溶液适量,逐滴加入NaOH溶液;
a.溶液从酸性变为中性;b.溶液逐渐产生沉淀;c.沉淀完全溶解;d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝;
④取适量③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题。
(1)由①可以排除_______ 的存在。
(2)由②可以证明_______ 的存在;同时排除_______ 的存在。
(3)由③可以证明_______ 的存在;写出c、d所涉及的化学方程式,是离子反应的用离子方程式表示:c_______ ;d_______ 。
(4)由④可以排除_______ 的存在。
 、K+、Ba2+、Al3+、Fe3+、I-、NO
、K+、Ba2+、Al3+、Fe3+、I-、NO 、CO
、CO 、SO
、SO 、AlO
、AlO 。取该溶液进行以下实验:
。取该溶液进行以下实验:①用pH试纸检验,溶液呈强酸性;
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色;
③另取溶液适量,逐滴加入NaOH溶液;
a.溶液从酸性变为中性;b.溶液逐渐产生沉淀;c.沉淀完全溶解;d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝;
④取适量③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题。
(1)由①可以排除
(2)由②可以证明
(3)由③可以证明
(4)由④可以排除
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有一包固体,可能含有NaCl、KNO3、K2CO3、BaCl2、CuSO4、K2SO4中的一种或几种,为确定其成分,进行如下实验:
(1)取少量固体溶于水,得白色沉淀和上层无色溶液;
(2)往沉淀中加足量稀硝酸,沉淀全部溶解;
(3)向(1)步得到的清液中加AgNO3,有白色沉淀产生,再加足量稀硝酸沉淀不溶解。
试推断,固体中一定含有_______ ,一定不含有_______ ,可能含有_______ 。(用物质的化学式表示)
(1)取少量固体溶于水,得白色沉淀和上层无色溶液;
(2)往沉淀中加足量稀硝酸,沉淀全部溶解;
(3)向(1)步得到的清液中加AgNO3,有白色沉淀产生,再加足量稀硝酸沉淀不溶解。
试推断,固体中一定含有
您最近一年使用:0次



