消毒剂在生产生活中有极其重要的作用,开发具有广谱、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
(1) 、
、 、
、 (还原产物为
(还原产物为 )、
)、 都可以做消毒剂,都具有
都可以做消毒剂,都具有___________ 性。
(2)将紫色石蕊试液滴入氯水中现象是___________ 。
(3)漂白剂亚氯酸钠( )在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为
)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为 (未配平)。在该反应中,被氧化的元素是
(未配平)。在该反应中,被氧化的元素是___________ ,13.7g 完全反应转移电子数是
完全反应转移电子数是___________ 。
(4)“84”消毒液(主要成分是NaClO),用氯气制取NaClO的离子方程式是___________ ,使用“84”消毒液时加入少量的稀硫酸效果更好,原理是___________ (用离子方程式表示)。
(1)
 、
、 、
、 (还原产物为
(还原产物为 )、
)、 都可以做消毒剂,都具有
都可以做消毒剂,都具有(2)将紫色石蕊试液滴入氯水中现象是
(3)漂白剂亚氯酸钠(
 )在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为
)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为 (未配平)。在该反应中,被氧化的元素是
(未配平)。在该反应中,被氧化的元素是 完全反应转移电子数是
完全反应转移电子数是(4)“84”消毒液(主要成分是NaClO),用氯气制取NaClO的离子方程式是
更新时间:2021-12-24 12:53:48
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】KClO3和浓盐酸在一定温度下反应,会生成橙黄色的易爆物二氧化氯(ClO2)气体,该反应的化学方程式为2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O。
(1)该反应的还原产物是_____________ (填化学式)。
(2)在反应中浓盐酸表现出来的性质是________ (填字母)。
A.只有还原性 B 只有氧化性 C.还原性和酸性 D.氧化性和酸性
(3)若该反应产生2.24 L(标准状况)ClO2,则转移电子的物质的量为_____________ 。
(4)当发生二氧化氯泄漏和爆炸事故,人们逃离爆炸现场时,可用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的物质是_________ (填字母)。
A.NaOH B.NaCl C.KCl D.Na2CO3
(5)某地生产的氧化钠井盐中含有少量的剧毒物质氰化钠(NaCN),用ClO2 可除去其中的氰化钠,从而得到纯净的食盐,同时产生两种无毒气体。写出该反应的化学方程式:_____________ 。
(1)该反应的还原产物是
(2)在反应中浓盐酸表现出来的性质是
A.只有还原性 B 只有氧化性 C.还原性和酸性 D.氧化性和酸性
(3)若该反应产生2.24 L(标准状况)ClO2,则转移电子的物质的量为
(4)当发生二氧化氯泄漏和爆炸事故,人们逃离爆炸现场时,可用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的物质是
A.NaOH B.NaCl C.KCl D.Na2CO3
(5)某地生产的氧化钠井盐中含有少量的剧毒物质氰化钠(NaCN),用ClO2 可除去其中的氰化钠,从而得到纯净的食盐,同时产生两种无毒气体。写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题。
Ⅰ.已知某容器中发生了一个化学反应,反应体系存在 、
、 、
、 、
、 、
、 、
、 六种粒子。在反应过程中,溶液紫红色逐渐褪去。
六种粒子。在反应过程中,溶液紫红色逐渐褪去。
(1)写出该反应的离子方程式:___________ 。
(2)该反应中,氧化剂与还原剂的粒子个数之比为___________ 。
Ⅱ.高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为: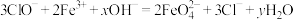 ,回答下列问题:
,回答下列问题:
(3)上述反应中的
___________ ,
___________ 。
(4)上述反应中氧化剂为___________ ;还原产物为___________ 。
(5)由上述反应可知,氧化性强弱:
___________  (填“>”或“<”,下同);还原性强弱:
(填“>”或“<”,下同);还原性强弱:
___________  。
。
(6)请用单线桥法表示该反应中电子的转移情况:___________ 。
Ⅰ.已知某容器中发生了一个化学反应,反应体系存在
 、
、 、
、 、
、 、
、 、
、 六种粒子。在反应过程中,溶液紫红色逐渐褪去。
六种粒子。在反应过程中,溶液紫红色逐渐褪去。(1)写出该反应的离子方程式:
(2)该反应中,氧化剂与还原剂的粒子个数之比为
Ⅱ.高铁酸钠
 是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为: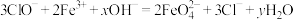 ,回答下列问题:
,回答下列问题:(3)上述反应中的


(4)上述反应中氧化剂为
(5)由上述反应可知,氧化性强弱:

 (填“>”或“<”,下同);还原性强弱:
(填“>”或“<”,下同);还原性强弱:
 。
。(6)请用单线桥法表示该反应中电子的转移情况:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学小魔术“魔棒点灯”的表演过程是:用玻璃棒蘸取固体高锰酸钾与浓硫酸的混合物,将混合物与酒精灯的灯芯接触,酒精即燃。其原理是:固体高锰酸钾与浓硫酸反应生成高锰酸(HMnO4)和硫酸钾,高锰酸立即分解生成一种棕色油状物——七氧化二锰和水,七氧化二锰遇酒精时,发生剧烈的氧化还原反应使酒精燃烧。七氧化二锰还能爆炸,分解生成二氧化锰、氧气和臭氧。氧气和臭氧的分子个数比为3:1。试写出生成高锰酸、七氧化二锰和它爆炸分解的化学方程式_______ 、_____ 、____ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】含氯化合物在日常生活中有多种用途,根据要求完成下列问题:
(1)漂白粉的有效成分是___________ ,家庭中使用漂白粉加水配置消毒液,与空气发生反应的化学方程式为___________ 。
(2)84消毒液的有效成分中NaClO中Cl的化合价为___________ ,请写出氯气与NaOH反应的化学方程式:___________ 。向NaOH溶液中通入11.2L(标准状况)氯气恰好完全反应生成三种含氯盐:0.7molNaCl、0.2molNaClO和X。则X是___________ 。
a.0.1molNaClO4 b.0.1molNaClO3 c.0.2molNaClO2 d.0.1molNaClO2
(3)日常生活中84消毒液若与洁厕灵(较浓的盐酸)混用,发生反应:NaClO+2HCl=NaCl+Cl2+H2O,该反应的氧化剂为___________ ,被氧化的物质为___________ 。若反应中电子转移为2mol,生成的氯气为___________ mol。
(1)漂白粉的有效成分是
(2)84消毒液的有效成分中NaClO中Cl的化合价为
a.0.1molNaClO4 b.0.1molNaClO3 c.0.2molNaClO2 d.0.1molNaClO2
(3)日常生活中84消毒液若与洁厕灵(较浓的盐酸)混用,发生反应:NaClO+2HCl=NaCl+Cl2+H2O,该反应的氧化剂为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据信息和要求书写相关反应的方程式
(1)用84消毒液对新冠病毒进行消杀。将 通入NaOH溶液制备84消毒液,写出反应的离子方程式
通入NaOH溶液制备84消毒液,写出反应的离子方程式___________ 。
(2) 与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:
与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:_____ 。

(3)以 为原料可在加热熔融条件下制取
为原料可在加热熔融条件下制取 。该反应中包含的所有物质有
。该反应中包含的所有物质有 、
、 、KCl、KOH、
、KCl、KOH、 、
、 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。
(4)向 溶液中逐滴加入
溶液中逐滴加入 溶液至沉淀完全,写出发生反应的离子方程式:
溶液至沉淀完全,写出发生反应的离子方程式:___________ 。
(1)用84消毒液对新冠病毒进行消杀。将
 通入NaOH溶液制备84消毒液,写出反应的离子方程式
通入NaOH溶液制备84消毒液,写出反应的离子方程式(2)
 与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:
与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:
(3)以
 为原料可在加热熔融条件下制取
为原料可在加热熔融条件下制取 。该反应中包含的所有物质有
。该反应中包含的所有物质有 、
、 、KCl、KOH、
、KCl、KOH、 、
、 ,写出该反应的化学方程式
,写出该反应的化学方程式(4)向
 溶液中逐滴加入
溶液中逐滴加入 溶液至沉淀完全,写出发生反应的离子方程式:
溶液至沉淀完全,写出发生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】A、B是两种常见的无机物,它们分别能与下图中周围4种物质在一定条件下反应:
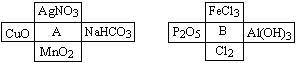
请回答下列问题:
(1)A溶液与B溶液反应的离子方程式_______________________ 。
(2)若A与其周围某物质在一定条件下反应,产物之一是B周围的一种,则此反应的离子方程式为________________
(3)请写出B溶液分别与Cl2、Al(OH)3反应的离子方程式:_________ ,____________
(4)在A、B周围的8种物质中,有些既能与A反应又能与B反应。则这些物质可能是:_______________

请回答下列问题:
(1)A溶液与B溶液反应的离子方程式
(2)若A与其周围某物质在一定条件下反应,产物之一是B周围的一种,则此反应的离子方程式为
(3)请写出B溶液分别与Cl2、Al(OH)3反应的离子方程式:
(4)在A、B周围的8种物质中,有些既能与A反应又能与B反应。则这些物质可能是:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氯及其化合物在生产、生活中都有重要的应用。
(1)已知HClO的杀菌能力比ClO-强。25℃时将氯气溶于水形成氯气—氯水体系,该体系中Cl2(aq)、HClO和ClO-的物质的量分数(α)随pH变化的关系如图所示。

由图分析,用氯气处理饮用水时,pH=7.5与pH=6时杀菌效果强的是___ ,当pH=7.5时,氯水中含氯元素的微粒有___ 。
(2)Ca(ClO)2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,NaClO2中Cl元素的化合价为___ ,写出工业上用氯气与石灰乳反应生产漂白粉的化学方程式:___ 。
(3)ClO2是国际上公认的高效、安全的杀菌消毒剂。
①工业制备ClO2的反应原理为:2KClO3+H2C2O4+H2SO4=K2SO4+2ClO2+2X +2H2O
X的化学式为___ ,每生成1molClO2,反应中转移电子___ mol。
②消毒能力可用单位质量消毒剂得电子多少来衡量。则ClO2与Cl2消毒能力比为___ (整数比)。
(1)已知HClO的杀菌能力比ClO-强。25℃时将氯气溶于水形成氯气—氯水体系,该体系中Cl2(aq)、HClO和ClO-的物质的量分数(α)随pH变化的关系如图所示。

由图分析,用氯气处理饮用水时,pH=7.5与pH=6时杀菌效果强的是
(2)Ca(ClO)2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,NaClO2中Cl元素的化合价为
(3)ClO2是国际上公认的高效、安全的杀菌消毒剂。
①工业制备ClO2的反应原理为:2KClO3+H2C2O4+H2SO4=K2SO4+2ClO2+2X +2H2O
X的化学式为
②消毒能力可用单位质量消毒剂得电子多少来衡量。则ClO2与Cl2消毒能力比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】含氧化合物具有广泛的应用,请回答下列问题。
(1) 中含有的电子数目为
中含有的电子数目为___________ 。
(2)将氯气持续通入紫色石蕊试液中,溶液颜色如图变化:

溶液中导致变色的微粒Ⅰ是___________ (填微粒符号,下同),Ⅱ是___________ ,Ⅲ是___________ 。
(3)氯气和氢氧化钠溶液反应可制备“84消毒液”,其化学方程式为___________ 。
(4)漂白粉漂白时,通入 可增加漂白效果,其化学方程式为
可增加漂白效果,其化学方程式为___________ 。
(5)用坩埚钳夹住一束铁丝,灼烧后立刻放入充满氯气的集气瓶中,反应的现象为___________ 。
(6) 是酸性氧化物,
是酸性氧化物, 和碱反应生成
和碱反应生成 的化学方程式为
的化学方程式为___________ 。
(1)
 中含有的电子数目为
中含有的电子数目为(2)将氯气持续通入紫色石蕊试液中,溶液颜色如图变化:

溶液中导致变色的微粒Ⅰ是
(3)氯气和氢氧化钠溶液反应可制备“84消毒液”,其化学方程式为
(4)漂白粉漂白时,通入
 可增加漂白效果,其化学方程式为
可增加漂白效果,其化学方程式为(5)用坩埚钳夹住一束铁丝,灼烧后立刻放入充满氯气的集气瓶中,反应的现象为
(6)
 是酸性氧化物,
是酸性氧化物, 和碱反应生成
和碱反应生成 的化学方程式为
的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氯气溶于水,形成氯水。
(1)氯水呈_______ 色,说明氯水中存在_______ 微粒;
(2)①取少量氯水,滴入硝酸银溶液,产生白色沉淀,说明氯水中存在_______ 微粒;另取少量氯水,滴入碘化钾淀粉溶液,看到溶液变_______ 色,这是因为_______ 。
②另取2mL碘化钾溶液,滴入少量氯水,少量四氯化碳,振荡静置。看到的现象是_______ 。
(3)请写出次氯酸电离方程式:_______ 。请写出次氯酸光照分解的化学方程式:_______ 。
(4)请写出次氯酸与氢氧化钠溶液反应的离子方程式:_______ 。
(1)氯水呈
(2)①取少量氯水,滴入硝酸银溶液,产生白色沉淀,说明氯水中存在
②另取2mL碘化钾溶液,滴入少量氯水,少量四氯化碳,振荡静置。看到的现象是
(3)请写出次氯酸电离方程式:
(4)请写出次氯酸与氢氧化钠溶液反应的离子方程式:
您最近一年使用:0次



