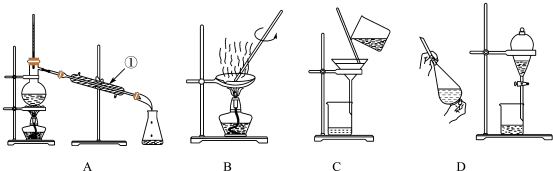
我国科学家屠呦呦因青蒿素研究获得诺贝尔奖,某实验小组拟提取青蒿素
【查阅资料】青蒿素为无色针状晶体,熔点156~157℃,易溶于丙酮、氯仿和乙醚,在水中几乎不溶。实验室用乙醚提取青蒿素的工艺流程如图所示:

(1)在操作I前要对青蒿进行粉碎,其目的是_______ 。
(2)操作II的名称是___________ 。
(3)操作III进行的是重结晶,其操作步骤为加热溶解→____ →____ →过滤、洗涤、干燥。
【查阅资料】青蒿素为无色针状晶体,熔点156~157℃,易溶于丙酮、氯仿和乙醚,在水中几乎不溶。实验室用乙醚提取青蒿素的工艺流程如图所示:

(1)在操作I前要对青蒿进行粉碎,其目的是
(2)操作II的名称是
(3)操作III进行的是重结晶,其操作步骤为加热溶解→
21-22高二·全国·课时练习 查看更多[2]
(已下线)1.2.1 有机化合物的分离、提纯-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修3)(已下线)1.2.1 分离提纯-2021-2022学年高二化学课后培优练(人教版2019选择性必修3)
更新时间:2021-12-25 09:17:50
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】掌握仪器的名称、组装及使用方法是中学化学实验的基础。如图为两套实验装置。
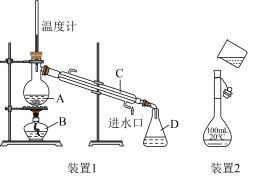
(1)写出下列实验仪器的名称A___ ;B___ ;C__ ;D___ 。
(2)用装置1分离四氯化碳和Br2的混合物,实验操作的名称为___ ,冷凝管的进水口是___ ;(填a或b);
(3)现需配制480mL 0.2mol/L KOH溶液,需要称量KOH___ g,配制过程中所用到的仪器有托盘天平、烧杯、___ 、___ 、胶头滴管。
(4)装置2是某同学转移溶液的示意图,图中的错误是___ 。
(5)下列操作会引起浓度偏高的是___ 。
A.溶液未冷却到室温就转移至容量瓶中 B.称量固体时将右边放药品与左边放砝码
C.定容时仰视读数 D.容量瓶中的水未除尽

(1)写出下列实验仪器的名称A
(2)用装置1分离四氯化碳和Br2的混合物,实验操作的名称为
(3)现需配制480mL 0.2mol/L KOH溶液,需要称量KOH
(4)装置2是某同学转移溶液的示意图,图中的错误是
(5)下列操作会引起浓度偏高的是
A.溶液未冷却到室温就转移至容量瓶中 B.称量固体时将右边放药品与左边放砝码
C.定容时仰视读数 D.容量瓶中的水未除尽
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】用于分离或提纯物质的方法有:
A .蒸馏 ( 分馏 ) B .萃取 C .过滤 D .重结晶 E .分液。
下列各组混合物的分离或提纯应选用上述哪一种方法最合适?(填方法的标号 )
(1)除去 Ca(OH) 2溶液中悬浮的CaCO3微粒_________
(2)分离四氯化碳与水的混合物_________
(3)分离碘水中的碘单质_________
(4)提纯氯化钠和硝酸钾混合物中的硝酸钾_________
A .蒸馏 ( 分馏 ) B .萃取 C .过滤 D .重结晶 E .分液。
下列各组混合物的分离或提纯应选用上述哪一种方法最合适?(填方法的标号 )
(1)除去 Ca(OH) 2溶液中悬浮的CaCO3微粒
(2)分离四氯化碳与水的混合物
(3)分离碘水中的碘单质
(4)提纯氯化钠和硝酸钾混合物中的硝酸钾
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.现有下列物质:①蔗糖、②Na2CO3溶液、③稀硫酸、④CO2、⑤CuSO4·5H2O固体、⑥石墨棒、⑦含泥沙的氯化钠溶液、⑧淀粉溶液
(1)属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
(2)除去⑦中的泥沙杂质的实验操作方法是___________ 。
(3)将气体④通入②会发生化学反应,其化学方程式为___________ 。
Ⅱ.央视《每周质量报告》曝光了一些明胶企业将皮革废料熬制成工业明胶,出售给某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(4)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是___________ 价。Fe(CrO2)2属于___________ (填“酸”、“碱”、“盐”或“氧化物”)。
(5)明胶的水溶液和K2SO4溶液共同具备的性质是___________(填序号)。
(1)属于电解质的是
(2)除去⑦中的泥沙杂质的实验操作方法是
(3)将气体④通入②会发生化学反应,其化学方程式为
Ⅱ.央视《每周质量报告》曝光了一些明胶企业将皮革废料熬制成工业明胶,出售给某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(4)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是
(5)明胶的水溶液和K2SO4溶液共同具备的性质是___________(填序号)。
| A.都不稳定,密封放置会产生沉淀 | B.分散质粒子可通过滤纸 |
| C.分散质粒子可通过半透膜 | D.二者均有丁达尔效应 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请按照要求回答下列各小题:
(1)被称为“水玻璃”的是溶液___ (填化学式),其电离方程式为___ 。
(2)随着生产力的发展,硫酸的生产工艺几经改进,目前工业上主要采用接触法制硫酸,其中产生SO2的设备的名称是___ 。
(3) 已知:2H++2CrO
 Cr2O
Cr2O +H2O,从Na2CrO4溶液中获得K2Cr2O7晶体,必须进行的操作步骤有:酸化→加KCl固体→蒸发浓缩→操作A→过滤→操作B→干燥,操作A的名称是
+H2O,从Na2CrO4溶液中获得K2Cr2O7晶体,必须进行的操作步骤有:酸化→加KCl固体→蒸发浓缩→操作A→过滤→操作B→干燥,操作A的名称是___ ;操作B的名称是___ 。
(1)被称为“水玻璃”的是溶液
(2)随着生产力的发展,硫酸的生产工艺几经改进,目前工业上主要采用接触法制硫酸,其中产生SO2的设备的名称是
(3) 已知:2H++2CrO

 Cr2O
Cr2O +H2O,从Na2CrO4溶液中获得K2Cr2O7晶体,必须进行的操作步骤有:酸化→加KCl固体→蒸发浓缩→操作A→过滤→操作B→干燥,操作A的名称是
+H2O,从Na2CrO4溶液中获得K2Cr2O7晶体,必须进行的操作步骤有:酸化→加KCl固体→蒸发浓缩→操作A→过滤→操作B→干燥,操作A的名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】选择下列实验方法分离物质,将分离方法的序号填在横线上.
A萃取分液 B升华 C结晶 D过滤 E蒸馏 F分液
(1)分离饱和食盐水与沙子的混合物___________
(2)从硝酸钾和氯化钠的混合液中获得硝酸钾___________
(3)从碘水中提取碘单质___________
(4)分离氯化钠固体和碘单质的混合物___________
(5)分离水和汽油的混合物___________
(6)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物___________
A萃取分液 B升华 C结晶 D过滤 E蒸馏 F分液
(1)分离饱和食盐水与沙子的混合物
(2)从硝酸钾和氯化钠的混合液中获得硝酸钾
(3)从碘水中提取碘单质
(4)分离氯化钠固体和碘单质的混合物
(5)分离水和汽油的混合物
(6)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】海水水资源的利用和海水化学资源的开发利用具有非常广阔的前景。
(1)列举海水淡化的两种方法:______________ 、______________ 。
(2)采用“空气吹出法”从浓海水吹出Br2,用SO2吸收,则发生反应的离子方程式为:____ 。
还可以用纯碱吸收,主要反应是Br2+Na2CO3+H2O → NaBr+NaBrO3+NaHCO3,当吸收1 mol Br2时,转移电子的物质的量为________ mol。
(3)按以下实验方案可从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
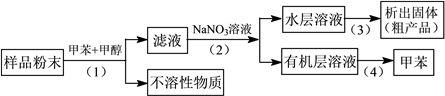
下列说法正确的是________ 。
A.步骤(1)需要过滤装置 B.步骤(2)需要用到分液漏斗
C.步骤(3)需要用到坩埚 D.步骤(4)需要蒸馏装置
(1)列举海水淡化的两种方法:
(2)采用“空气吹出法”从浓海水吹出Br2,用SO2吸收,则发生反应的离子方程式为:
还可以用纯碱吸收,主要反应是Br2+Na2CO3+H2O → NaBr+NaBrO3+NaHCO3,当吸收1 mol Br2时,转移电子的物质的量为
(3)按以下实验方案可从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
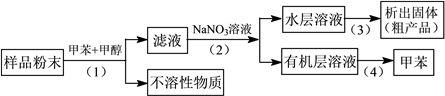
下列说法正确的是
A.步骤(1)需要过滤装置 B.步骤(2)需要用到分液漏斗
C.步骤(3)需要用到坩埚 D.步骤(4)需要蒸馏装置
您最近一年使用:0次
【推荐2】现拟分离乙酸乙酯、乙酸、乙醇的混合物,如图所示的分离操作步骤流程图.图中圆括号内为加入的适当试剂,中括号内为采取的适当分离方法,方框内字母代表分离得到的有关物质的名称.
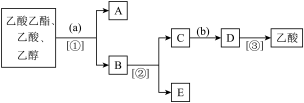
请填写:
(1)试剂:a._____________ ,b._____________ .
(2)操作:①_______ ;②_______ ;③_______ .
(3)分离所得物质的名称:
A_________ ,B__________ ,C_________ ,D________ ,E_______ .

请填写:
(1)试剂:a.
(2)操作:①
(3)分离所得物质的名称:
A
您最近一年使用:0次