某化学兴趣小组利用如图所示装置进行“铁与水反应”的实验,并检验产物的性质,且要对反应后硬质试管中固体物质的组成进行探究。请回答下列问题:
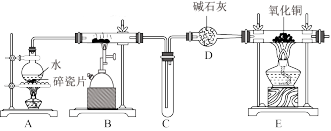
(1)A的作用是___________ ,B中反应的化学方程式为___________ 。
(2)D的作用是___________ 。
(3)E中的现象是______ 。
(4)A、B两个装置中应先点燃______ 处的酒精(喷)灯(填“A”或“E”),点燃E处酒精灯之前应进行的操作是______ 。
(5)该小组对反应后硬质试管中固体物质的组成提出了如下假设。
假设1:只有Fe;
假设2:只有____ (填化学式);
假设3:既有Fe也有Fe3O4。
(6)为了验证反应后硬质试管中固体物质的组成,该同学进行了定量研究:反应前固体物质的质量为5.6g,反应后固体物质的质量为6.6g.从数据分析,反应后硬质试管中固体物质的组成为_____ 。

(1)A的作用是
(2)D的作用是
(3)E中的现象是
(4)A、B两个装置中应先点燃
(5)该小组对反应后硬质试管中固体物质的组成提出了如下假设。
假设1:只有Fe;
假设2:只有
假设3:既有Fe也有Fe3O4。
(6)为了验证反应后硬质试管中固体物质的组成,该同学进行了定量研究:反应前固体物质的质量为5.6g,反应后固体物质的质量为6.6g.从数据分析,反应后硬质试管中固体物质的组成为
更新时间:2021-12-29 20:53:44
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】新型材料纳米α-Fe粉具有超强的磁性能,可用作高密度磁记录的介质以及高效催化剂等。
(1)甲同学用下左图所示装置进行α-Fe粉与水蒸气的反应。

Fe粉与水蒸气反应的化学反应方程式为__________________ ;
证明实验中有氢气产生的现象是_________________ 。
(2)已知不同温度下,α—Fe粉与水蒸气反应的固体产物不同:温度低于570℃时,生成FeO;高于570℃时,生成Fe3O4。乙同学用上右图所示装置进行α-Fe粉与水蒸气的反应并验证产物。
①试管a中的物质是__________________ 。
②乙同学为探究实验结束后试管内的 固体物质成分,进行了下列实验:
以上实验现象能否判断固体物质中Fe3O4的存在___________ ( 填“存在”或“不存在”或“不能确定”),主要原因 是_______________ (用离子方程式表示)。
(1)甲同学用下左图所示装置进行α-Fe粉与水蒸气的反应。

Fe粉与水蒸气反应的化学反应方程式为
证明实验中有氢气产生的现象是
(2)已知不同温度下,α—Fe粉与水蒸气反应的固体产物不同:温度低于570℃时,生成FeO;高于570℃时,生成Fe3O4。乙同学用上右图所示装置进行α-Fe粉与水蒸气的反应并验证产物。
①试管a中的物质是
②乙同学为探究实验结束后
实验步骤 | 实验操作 | 实验现象 |
Ⅰ | 将反应后得到黑色粉末X(假定为均匀的),取出少量放入另一试管中,加入适量盐酸,微热加速反应的进行 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
Ⅱ | 向实验I中得到的溶液滴加几滴KSCN溶液,振荡 | 溶液没有出现红色 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、E、H是中学化学常见的单质;B、D、F是中学化学常见的氧化物,其中D又是生命活动不可缺少的液态物质;G、I的焰色反应呈黄色,D与 E在高温条件下能发生反应。它们之间的转化关系如下图所示:
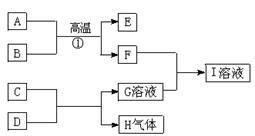
(1)C若为单质,其与D反应的离子方程式为_____ 。C若为氧化物,其电子式为:______ 。
(2)若B为铁的氧化物,8g B灼热后通入足量CO,将生成的气体通入过量石灰水,生成沉淀15g,则B的化学式______ ,写出①的化学方程式_____________ 。
(3)E与D反应的化学方程式_________________________________________ 。

(1)C若为单质,其与D反应的离子方程式为
(2)若B为铁的氧化物,8g B灼热后通入足量CO,将生成的气体通入过量石灰水,生成沉淀15g,则B的化学式
(3)E与D反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某小组设计如下实验探究铁与水蒸气的反应.
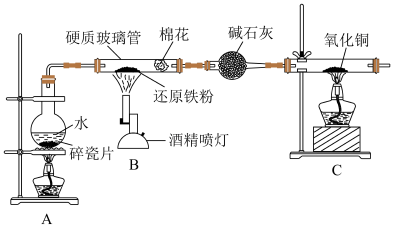
回答下列问题:
(1)写出铁和水蒸气反应的化学方程式,并用双线桥表示电子转移的方向和数目:_________________ .
(2)圆底烧瓶中碎瓷片的作用是防止暴沸,若加热一段时间后发现忘记加碎瓷片,需要补加碎瓷片的操作是___________________ .
(3)检验反应后的固体是否存在 ,引起小组成员争论:
,引起小组成员争论:
①甲同学认为可以使用化学方法,先用足量硫酸溶解,再分别检验 和
和 .
.
a.先检测 是否存在:从下列试剂中选择
是否存在:从下列试剂中选择________ 来检验 是否存在.然后再检测
是否存在.然后再检测 是否存在.
是否存在.
A. 溶液 B.新制氯水、KSCN溶液 C.酸性
溶液 B.新制氯水、KSCN溶液 C.酸性 溶液
溶液
b.多数同学认为该方法检验是否存在 不合理,请写出一条理由:
不合理,请写出一条理由:__________________
②乙同学认为可以利用 的物理性质进行快速检验.用铁片接触样品后再移开,若观察到
的物理性质进行快速检验.用铁片接触样品后再移开,若观察到_________ 现象,证明了反应后的固体中含有 。
。

回答下列问题:
(1)写出铁和水蒸气反应的化学方程式,并用双线桥表示电子转移的方向和数目:
(2)圆底烧瓶中碎瓷片的作用是防止暴沸,若加热一段时间后发现忘记加碎瓷片,需要补加碎瓷片的操作是
(3)检验反应后的固体是否存在
 ,引起小组成员争论:
,引起小组成员争论:①甲同学认为可以使用化学方法,先用足量硫酸溶解,再分别检验
 和
和 .
.a.先检测
 是否存在:从下列试剂中选择
是否存在:从下列试剂中选择 是否存在.然后再检测
是否存在.然后再检测 是否存在.
是否存在.A.
 溶液 B.新制氯水、KSCN溶液 C.酸性
溶液 B.新制氯水、KSCN溶液 C.酸性 溶液
溶液b.多数同学认为该方法检验是否存在
 不合理,请写出一条理由:
不合理,请写出一条理由:②乙同学认为可以利用
 的物理性质进行快速检验.用铁片接触样品后再移开,若观察到
的物理性质进行快速检验.用铁片接触样品后再移开,若观察到 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】如图是实验室研究潜水艇中供氧体系反应机理的装置图(夹持仪器略)。
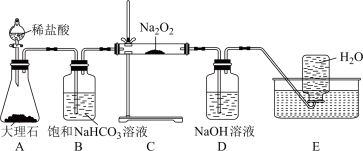
(1)B装置可除去A装置中可能挥发出的_______ ,反应的离子方程式为_______ 。
(2)C装置为O2的发生装置,发生反应的化学方程式有_______ 、_______ 。
(3)D装置可除去C装置中未发生反应的_______ ,反应的离子方程式为_______ 。
(4)C装置中固体由淡黄色完全变为白色,检验固体成分的实验方案为取少量C装置中反应后的固体溶于水,向溶液中滴入过量_______ 溶液,若有白色沉淀生成,则证明固体中含有_______ ;过滤,向滤液中滴入几滴酚酞试液,若_______ 且不褪色,则证明固体中含有_______ 。

(1)B装置可除去A装置中可能挥发出的
(2)C装置为O2的发生装置,发生反应的化学方程式有
(3)D装置可除去C装置中未发生反应的
(4)C装置中固体由淡黄色完全变为白色,检验固体成分的实验方案为取少量C装置中反应后的固体溶于水,向溶液中滴入过量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】亚硝酸钠(NaNO2)是一种常见的食品添加剂,在使用过程中必须严格控制用量,否则会导致中毒。为此某兴趣小组制备 并对其性质进行探究。
并对其性质进行探究。
已知: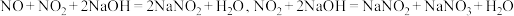
回答下列问题:
Ⅰ.制备
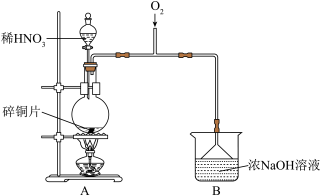
(1)为检验B中制得 ,甲进行以下实验,请将实验补充完整。
,甲进行以下实验,请将实验补充完整。
(2)乙认为上述3组实验无法证明B中一定含 ,还需补充实验,理由是
,还需补充实验,理由是________
Ⅱ.探究 的性质
的性质
资料:ⅰ.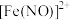 在溶液中呈棕色。
在溶液中呈棕色。
ⅱ. 在溶液中不稳定,易分解产生
在溶液中不稳定,易分解产生 和
和 气体。
气体。
(3)溶液迅速变为棕色的原因是_______ 。
(4)已知棕色溶液变浅是由于生成了 ,反应的离子方程式是
,反应的离子方程式是_______ 。
(5)最终棕褐色溶液的成分是 ,乙认为其中铁元素可能为
,乙认为其中铁元素可能为 ,也可能为
,也可能为 ,或既有
,或既有 也有
也有 ,因此设计以下实验探究,请补齐实验方案。
,因此设计以下实验探究,请补齐实验方案。
 并对其性质进行探究。
并对其性质进行探究。已知:
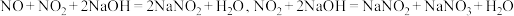
回答下列问题:
Ⅰ.制备


(1)为检验B中制得
 ,甲进行以下实验,请将实验补充完整。
,甲进行以下实验,请将实验补充完整。| 序号 | 试管 | 操作 | 现象 |
| ① | 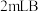 中溶液 中溶液 | 加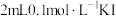 溶液,滴加几滴淀粉溶液 溶液,滴加几滴淀粉溶液 | 不变蓝 |
| ② | 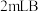 中溶液 中溶液 | 滴加几滴 至 至 ,加 ,加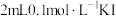 溶液,滴加几滴淀粉溶液 溶液,滴加几滴淀粉溶液 | 变蓝 |
| ③ | 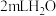 | 滴加几滴 至 至 ,加 ,加 | 不变蓝 |
 ,还需补充实验,理由是
,还需补充实验,理由是Ⅱ.探究
 的性质
的性质| 装置 | 操作 | 现象 |
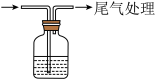 | 取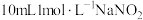 溶液于试剂瓶中,加入几滴 溶液于试剂瓶中,加入几滴 酸化,再加入 酸化,再加入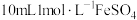 溶液,迅速塞上橡胶塞,缓缓通入足量 溶液,迅速塞上橡胶塞,缓缓通入足量 | ⅰ.溶液迅速变为棕色; ⅱ.溶液逐渐变浅,有无色气泡产生,溶液上方为浅红棕色; iii.最终形成棕褐色溶液。 |
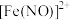 在溶液中呈棕色。
在溶液中呈棕色。ⅱ.
 在溶液中不稳定,易分解产生
在溶液中不稳定,易分解产生 和
和 气体。
气体。(3)溶液迅速变为棕色的原因是
(4)已知棕色溶液变浅是由于生成了
 ,反应的离子方程式是
,反应的离子方程式是(5)最终棕褐色溶液的成分是
 ,乙认为其中铁元素可能为
,乙认为其中铁元素可能为 ,也可能为
,也可能为 ,或既有
,或既有 也有
也有 ,因此设计以下实验探究,请补齐实验方案。
,因此设计以下实验探究,请补齐实验方案。| 实验操作 | 预期现象与结论 |
步骤1:加入过量稀 于 于 ,溶液中 ,溶液中 | |
| 步骤2:① | ② |
| 步骤3:③ | 若溶液变为红色,则含有Fe3+ |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】一氧化二氯( )是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸。
)是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸。 的熔点是-120.6℃,沸点是2.0℃。利用反应
的熔点是-120.6℃,沸点是2.0℃。利用反应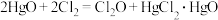 可制备
可制备 ,某同学利用如图所示装置制备
,某同学利用如图所示装置制备 。
。
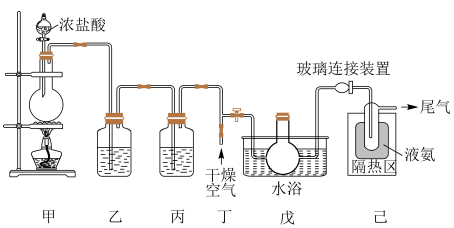
回答下列问题:
(1)装置甲的作用是为该制备反应提供 ,写出该装置中制备
,写出该装置中制备 的离子方程式为
的离子方程式为_______ 。
(2)装置乙的洗气瓶中盛放的试剂是_______ ;装置丙的作用是_______ 。
(3)反应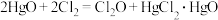 中,每生成1 mol
中,每生成1 mol  转移电子的物质的量为
转移电子的物质的量为_______ mol。若实验开始前称量装置戊中的玻璃丝与HgO的混合物的质量为48.0g,实验结束后玻璃丝及其附着物的质量为53.5g,则制备的 为
为_______ mol。
(4)25℃下, 的
的 ,HClO的
,HClO的 ,则:
,则:
①温度、浓度相同的 和HClO溶液,水的电离程度:前者
和HClO溶液,水的电离程度:前者_______ 后者(填“>”“=”或“<”)。
②相同温度下,pH相同的NaClO和 两种溶液中,
两种溶液中,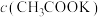
_______  (填“>”“=”或“<”,下同),
(填“>”“=”或“<”,下同),
_______ 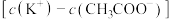 。
。
 )是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸。
)是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸。 的熔点是-120.6℃,沸点是2.0℃。利用反应
的熔点是-120.6℃,沸点是2.0℃。利用反应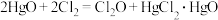 可制备
可制备 ,某同学利用如图所示装置制备
,某同学利用如图所示装置制备 。
。
回答下列问题:
(1)装置甲的作用是为该制备反应提供
 ,写出该装置中制备
,写出该装置中制备 的离子方程式为
的离子方程式为(2)装置乙的洗气瓶中盛放的试剂是
(3)反应
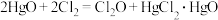 中,每生成1 mol
中,每生成1 mol  转移电子的物质的量为
转移电子的物质的量为 为
为(4)25℃下,
 的
的 ,HClO的
,HClO的 ,则:
,则:①温度、浓度相同的
 和HClO溶液,水的电离程度:前者
和HClO溶液,水的电离程度:前者②相同温度下,pH相同的NaClO和
 两种溶液中,
两种溶液中,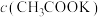
 (填“>”“=”或“<”,下同),
(填“>”“=”或“<”,下同),
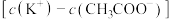 。
。
您最近一年使用:0次



