我国的环境空气质量标准中对空气中SO2的浓度限值规定如下表所示。
研究人员测定受污染空气中SO2含量的实验方法如下:用NaOH溶液吸收2m3空气,用0.1mo·L-1硫酸调节pH,然后用I2溶液将其氧化,测得恰好完全反应时消耗I22.54mg。下列推断中,不正确 的是
| 标准等级 | 一级标准 | 二级标准 | 三级标准 |
| 浓度限值(mg·m-3) | 0~0.15 | 0.15~0.50 | 0.50~0.70 |
| A.恰好完全反应时消耗I2的物质的量为1×10-5mol |
| B.反应中转移电子的物质的量为2×10-5mol |
| C.被吸收的空气中SO2的质量为0.64mg |
| D.被测空气样品中SO2的浓度达到了三级标准 |
更新时间:2022-01-14 12:10:55
|
相似题推荐
【推荐1】铜与一定量浓硝酸恰好完全反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与0.84 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,若向所得硝酸铜溶液中加入5 mol·L-1NaOH溶液至Cu2+恰好完全沉淀,消耗NaOH溶液的体积是
| A.60 mL | B.45 mL | C.30 mL | D.15 mL |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在120℃和101kPa的条件下,某气态烃和过量的氧气混和,点燃完全反应后再恢复到原状态时,气体体积不变,则该烃分子内的氢原子个数是
| A.小于4 | B.大于4 | C.等于4 | D.无法判断 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在标准状况下,0.672L H2S气体通入含有0.01mol X2O 离子的酸性溶液中,两者恰好完全反应,而且H2S全部被氧化成硫单质,则X元素在还原产物中的化合价为
离子的酸性溶液中,两者恰好完全反应,而且H2S全部被氧化成硫单质,则X元素在还原产物中的化合价为
 离子的酸性溶液中,两者恰好完全反应,而且H2S全部被氧化成硫单质,则X元素在还原产物中的化合价为
离子的酸性溶液中,两者恰好完全反应,而且H2S全部被氧化成硫单质,则X元素在还原产物中的化合价为| A.+4 | B.+3 | C.+2 | D.+1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】Fe和Fe2O3的混合物共13.6g,加入150mL稀H2SO4,在标准状况下收集到1.12LH2,Fe和Fe2O3均无剩余。为中和过量的H2SO4,并使FeSO4全部转化为Fe(OH)2沉淀,消耗了200mL 3mol/L的NaOH溶液,则该H2SO4的物质的量浓度为
| A.2.25mol/L | B.2mol/L | C.0.3mol/L | D.0.6mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】用CH4催化还原NOx可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
下列说法不正确的是
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
下列说法不正确的是
| A.由反应①、②可推知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH=-867kJ·mol-1 |
| B.等物质的量的甲烷分别参与反应①、②,则反应转移的电子数相等 |
| C.若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移的电子总数为3.2NA |
| D.若用标准状况下4.48 L CH4还原NO2至N2,放出的热量为173.4 kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】研究表明,易溶于水的 所形成的溶液中存在着下列平衡:
所形成的溶液中存在着下列平衡: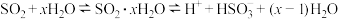 、
、 ,据此,下列说法正确的是
,据此,下列说法正确的是
 所形成的溶液中存在着下列平衡:
所形成的溶液中存在着下列平衡: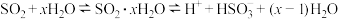 、
、 ,据此,下列说法正确的是
,据此,下列说法正确的是A.该溶液中存在着 分子 分子 |
B.该溶液中的微粒只有 、 、 、 、 、 、 、 、 |
C.向该溶液中加入足量的酸都能放出 气体 气体 |
D.向该溶液中加入过量NaOH可得到溶质为 、 、 和NaOH的溶液 和NaOH的溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】物质的转化具有重要应用。下列说法正确的是
A.在稀硫酸中加入铜粉,铜粉不溶解,若再加入 ,铜粉溶解 ,铜粉溶解 |
B.实验室检验 的漂白性:酸性 的漂白性:酸性 溶液 溶液 紫红色褪去 紫红色褪去 |
C.工业上通过 生产 生产 的物质转化:NH3 的物质转化:NH3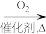 NO2 NO2 HNO3 HNO3 |
D.在实验室中向饱和 溶液中滴加少量稀氨水制备 溶液中滴加少量稀氨水制备 胶体 胶体 |
您最近一年使用:0次







