下表是元素周期表的一部分,表中所列的数字分别代表某一种元素。
针对元素①~⑩回答下列问题。
(1)元素①和②的单质化合形成的化合物NaH中H元素的化合价为_______ ;NaH能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,其化学方程式为_______ 。
(2)元素④是人体必不可缺少的一种元素,缺乏会出现骨质疏松、易骨折等症状,请写出其原子结构示意图_______ 。
(3)由元素①和⑥形成的一种物质是天然气的主要成分,其电子式为_______ ;元素⑥还可以和⑦形成一种三原子直线型分子,其结构式为_______ ;元素②的单质在元素⑦的单质中点燃生成的淡黄色固体将其投入硫酸亚铁溶液中,预测主要的反应现象是_______ 。
(4)元素③、⑧、⑨的简单离子中半径最大是_______ (填离子符号),元素②和⑤的最高价氧化物对应的水化物之间可以发生反应,其反应的离子方程式为_______ 。
(5)表中元素⑨和⑩的气态氢化物中更稳定的是_______ (填化学式)。
| 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ② | ⑤ | ⑧ | ⑨ | ||||
| 4 | ③ | ④ | ⑩ |
(1)元素①和②的单质化合形成的化合物NaH中H元素的化合价为
(2)元素④是人体必不可缺少的一种元素,缺乏会出现骨质疏松、易骨折等症状,请写出其原子结构示意图
(3)由元素①和⑥形成的一种物质是天然气的主要成分,其电子式为
(4)元素③、⑧、⑨的简单离子中半径最大是
(5)表中元素⑨和⑩的气态氢化物中更稳定的是
更新时间:2022-01-19 10:55:20
|
相似题推荐
【推荐1】含硫的物质与人们的生活密切相关。已知硫元素常见的化合价有-1、0、+4、+6四种,其不同价态的物质间可相互转化。完成下列填空:
(1)硫离子的结构示意图_____________ 。
(2)黑火药爆炸时,发生的反应之一为:S+2KNO3+3C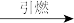 K2S+3CO2↑+N2↑该反应中1mol S能氧化C
K2S+3CO2↑+N2↑该反应中1mol S能氧化C_______ mol。
(3)将硫化氢气体与二氧化硫气体在集气瓶中混合发生反应,现象____________ 。二氧化硫呈现______________ (选填“氧化性”、“还原性”)。
(4)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是硫酸。
以下是二氧化硫形成酸雨的两种途径:

请分别写出(1)和(4)的化学方程式:________________ , ___________________ 。
(5)你认为减少酸雨产生的途径可采用的措施是_______________ 。
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A. ①②③ B. ②③④ C. ①③⑤ D. ①③④⑤
(6)硫酸盐的种类很多,且应用广泛,医疗上常用_______ (写化学式)作X射线透视肠胃的内服药剂,生活用水可以用_________ (写化学式)作净水剂。
(7)有化学反应2SO2(g)+O2(g)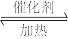 2SO3(g) △H=-190kJ/mol,450℃往2L密闭容器中充入2mol SO2和1mol O2,5分钟后的SO2物质的量为0.5mol,则在5min内,用消耗的O2表示的反应速率为
2SO3(g) △H=-190kJ/mol,450℃往2L密闭容器中充入2mol SO2和1mol O2,5分钟后的SO2物质的量为0.5mol,则在5min内,用消耗的O2表示的反应速率为_____________________ 。在其它条件不变时,扩大容器体积,v(正)_______ (选填“增大”或“减小”或“不变”),v(逆)______ (选填“增大”或“减小”或“不变”)。
(1)硫离子的结构示意图
(2)黑火药爆炸时,发生的反应之一为:S+2KNO3+3C
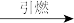 K2S+3CO2↑+N2↑该反应中1mol S能氧化C
K2S+3CO2↑+N2↑该反应中1mol S能氧化C(3)将硫化氢气体与二氧化硫气体在集气瓶中混合发生反应,现象
(4)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是硫酸。
以下是二氧化硫形成酸雨的两种途径:

请分别写出(1)和(4)的化学方程式:
(5)你认为减少酸雨产生的途径可采用的措施是
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A. ①②③ B. ②③④ C. ①③⑤ D. ①③④⑤
(6)硫酸盐的种类很多,且应用广泛,医疗上常用
(7)有化学反应2SO2(g)+O2(g)
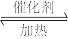 2SO3(g) △H=-190kJ/mol,450℃往2L密闭容器中充入2mol SO2和1mol O2,5分钟后的SO2物质的量为0.5mol,则在5min内,用消耗的O2表示的反应速率为
2SO3(g) △H=-190kJ/mol,450℃往2L密闭容器中充入2mol SO2和1mol O2,5分钟后的SO2物质的量为0.5mol,则在5min内,用消耗的O2表示的反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据要求回答下列问题:
(1) 的离子结构示意图为
的离子结构示意图为___________ 。
(2)Se与S同族,基态硒原子价层电子排布式为___________ 。
(3)基态F原子的价层电子排布图(轨道表示式)为___________ 。
(4)基态S原子的原子核外电子有___________ 种空间运动状态,其能量最高的电子电子云轮廓图为___________ 形。
(5)基态Ni原子的电子排布式为___________ ,在元素周期表中位置为___________ 。
(1)
 的离子结构示意图为
的离子结构示意图为(2)Se与S同族,基态硒原子价层电子排布式为
(3)基态F原子的价层电子排布图(轨道表示式)为
(4)基态S原子的原子核外电子有
(5)基态Ni原子的电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如表是元素周期表的一部分,回答下列有关问题。
(1)写出下列元素符号:①___________
(2)画出原子的结构示意图:④___________
(3)在①—⑫元素中,金属性最强的元素是___________ ,非金属性最强的元素是___________ ,最不活泼的元素是___________ 。(均填元素符号)
(4)第三周期中原子半径最大的元素是___________ (填序号),跟它同周期原子半径最小的元素是___________ (填序号),它们可以形成___________ (填“离子”或“共价”)化合物,用电子式表示其形成过程如下:___________ 。
(5)在①~⑩元素的最高价氧化物对应的水化物中,呈两性的是___________ 。写出其与另两种水溶液之间相互反应的离子方程式___________ ,___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)画出原子的结构示意图:④
(3)在①—⑫元素中,金属性最强的元素是
(4)第三周期中原子半径最大的元素是
(5)在①~⑩元素的最高价氧化物对应的水化物中,呈两性的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,针对表中①到⑩10种元素,填写下表空白:
(1)在最高价氧化物对应的水化物中,酸性最强的化合物的化学式是______ ,碱性最强的化合物的化学式是______ 。 均填化学式
均填化学式
(2)最高价氧化物对应的水化物是两性的元素是______  填元素符号
填元素符号 ,写出它的氢氧化物与⑤的氢氧化物反应的离子方程式
,写出它的氢氧化物与⑤的氢氧化物反应的离子方程式______ 。
(3)③⑤⑥三元素形成的简单离子具有相同的电子层结构,它们的离子半径由大到小顺序是 用离子符号表示
用离子符号表示
______ 。
列 周期 | 1 | 2 | 13 | 14 | 15 | 16 | 17 | 18 |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
4 | ⑩ |
(1)在最高价氧化物对应的水化物中,酸性最强的化合物的化学式是
 均填化学式
均填化学式
(2)最高价氧化物对应的水化物是两性的元素是
 填元素符号
填元素符号 ,写出它的氢氧化物与⑤的氢氧化物反应的离子方程式
,写出它的氢氧化物与⑤的氢氧化物反应的离子方程式(3)③⑤⑥三元素形成的简单离子具有相同的电子层结构,它们的离子半径由大到小顺序是
 用离子符号表示
用离子符号表示
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】右表为元素周期表的一部分。回答下列问题:
(1)Z的元素符号为_________________ 。
(2)X位于元素周期表第_______ 周期_______ 族。
(3)W与Y形成的化合物WY中,W的化合价是________ 。
(4)硫的最简单氢化物与硫的低价氧化物通入水中时,发生反应的化学方程式为_________________________ 。
| W | 氮 | Y | |
| X | 硫 | Z |
(1)Z的元素符号为
(2)X位于元素周期表第
(3)W与Y形成的化合物WY中,W的化合价是
(4)硫的最简单氢化物与硫的低价氧化物通入水中时,发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素周期表与元素周期律在化学学习研究中有很重要的作用。如表是元素周期表的一部分,回答下列问题(用相关化学用语回答)。
(1)⑤、⑥、⑨、⑩的简单离子半径由小到大的顺序____ ,写出⑥的原子结构示意图:____ 。
(2)元素①的一种同素异形体为天然存在的最硬的物质,它属于____ (填“晶体”或“非晶体”)。
(3)元素②、③、④的简单气态氢化物的稳定性最强的是____ (用化学式表示,下同),元素③、⑨简单氢化物沸点较高的是____ 。
(4)元素⑤、⑥最高价氧化物对应的水化物碱性更强的是____ ,元素⑪最高价氧化物对应的水化物的化学式是____ 。
(5)请用电子式表示元素⑤的氧化物的形成过程:____ ,该化合物属于____ (填“共价”或“离子”)化合物。
(6)⑤2⑨③3在加热条件下发生分解反应生成两种盐,其中一种产物为无氧酸盐,该反应的化学方程式:____ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
| 四 | ⑪ |
(2)元素①的一种同素异形体为天然存在的最硬的物质,它属于
(3)元素②、③、④的简单气态氢化物的稳定性最强的是
(4)元素⑤、⑥最高价氧化物对应的水化物碱性更强的是
(5)请用电子式表示元素⑤的氧化物的形成过程:
(6)⑤2⑨③3在加热条件下发生分解反应生成两种盐,其中一种产物为无氧酸盐,该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】硬铝(含少量铜、镁、锰和硅)有良好的机械性能,是制造飞机的理想材料。
(1)写出硅原子最外层电子排布式__________ ;短周期元素A与硅元素同主族,能与氧元素组成化合物AO2,写出AO2的电子式:__________ 。
(2)上述硬铝中所含的主族元素的原子半径由大到小的顺序为:__________ 。
(3)请阐述硬铝是制造飞机的理想材料的原因有:__________ 、__________ 。
(4)工业上可用镁真空炼铷,方程式为2RbCl+Mg MgCl2+2Rb(g),对于此反应能够进行正确的解释是
MgCl2+2Rb(g),对于此反应能够进行正确的解释是 __________ 。
a.Rb比Mg金属性强
b.MgCl2的热稳定性比RbCl 弱
c.高温下Mg2+得电子能力比Rb+弱
d.Rb的沸点比Mg低,当把Rb(g)抽走时,平衡向正反应方向移动
(1)写出硅原子最外层电子排布式
(2)上述硬铝中所含的主族元素的原子半径由大到小的顺序为:
(3)请阐述硬铝是制造飞机的理想材料的原因有:
(4)工业上可用镁真空炼铷,方程式为2RbCl+Mg
 MgCl2+2Rb(g),对于此反应能够进行正确的解释是
MgCl2+2Rb(g),对于此反应能够进行正确的解释是 a.Rb比Mg金属性强
b.MgCl2的热稳定性比RbCl 弱
c.高温下Mg2+得电子能力比Rb+弱
d.Rb的沸点比Mg低,当把Rb(g)抽走时,平衡向正反应方向移动
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】短周期元素A、B、C、D、E在元素周期表中的相对位置如图所示:

请回答下列问题:
(1)D在元素周期表中的位置为___ 。
(2)A和C形成的一种摩尔质量为41g·mol-1的化合物,该化合物与盐酸反应能生成两种盐,其化学方程式为___ 。
(3)M为A的简单气态氮化物,其水溶液可作刻蚀剂H2O2的清除剂,反应的产物不污染环境,其化学方程式为___ 。N为A的另一种氢化物,其相对分子质量比M大15,N为二元弱碱,在水中分步电离,并与M的电离方式相似,则N第一步电离的电离方程式为___ ,N与过量硫酸反应生成的酸式盐的化学式为___ 。
(4)下列事实能说明E元素的非金属性比D元素的非金属性强的是___ (填序号)。
①E的单质与D的气态氢化物的水溶液反应,生成淡黄色沉淀
②E与H2化合比D与H2化合更容易
③D与Fe化合时产物中Fe为+2价,E与Fe化合时产物中Fe为+3价
④等浓度的D和E的最高价含氧酸的水溶液中的c(H+):D>E
(5)D2E2分子中各原子最外层均满足8电子结构,则D2E2的电子式为___ 。

请回答下列问题:
(1)D在元素周期表中的位置为
(2)A和C形成的一种摩尔质量为41g·mol-1的化合物,该化合物与盐酸反应能生成两种盐,其化学方程式为
(3)M为A的简单气态氮化物,其水溶液可作刻蚀剂H2O2的清除剂,反应的产物不污染环境,其化学方程式为
(4)下列事实能说明E元素的非金属性比D元素的非金属性强的是
①E的单质与D的气态氢化物的水溶液反应,生成淡黄色沉淀
②E与H2化合比D与H2化合更容易
③D与Fe化合时产物中Fe为+2价,E与Fe化合时产物中Fe为+3价
④等浓度的D和E的最高价含氧酸的水溶液中的c(H+):D>E
(5)D2E2分子中各原子最外层均满足8电子结构,则D2E2的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据题意回答下列问题
(1)胃舒平的主要成分是氢氧化铝,同时含有三硅酸镁(Mg2Si3O8·nH2O)等化合物。三硅酸镁的氧化物形式为___________ 。
(2)Al2O3、MgO和SiO2都可以制耐火材料,其原因是___________ (填字母)。
a.Al2O3、MgO和SiO2都是白色固体
b.Al2O3、MgO和SiO2都是金属氧化物
c.Al2O3、MgO和SiO2都有很高的熔点
(3)用浓硫酸给竹筒“刻字”是利用浓硫酸的___________ 性。
(4)写出Cu与浓硫酸在加热条件下反应的化学方程式___________
(5)推测Si、N最简单氢化物的稳定性:___________ 强于___________ (填化学式)。
(1)胃舒平的主要成分是氢氧化铝,同时含有三硅酸镁(Mg2Si3O8·nH2O)等化合物。三硅酸镁的氧化物形式为
(2)Al2O3、MgO和SiO2都可以制耐火材料,其原因是
a.Al2O3、MgO和SiO2都是白色固体
b.Al2O3、MgO和SiO2都是金属氧化物
c.Al2O3、MgO和SiO2都有很高的熔点
(3)用浓硫酸给竹筒“刻字”是利用浓硫酸的
(4)写出Cu与浓硫酸在加热条件下反应的化学方程式
(5)推测Si、N最简单氢化物的稳定性:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题(书写相关符号)。
(1)上述8种元素中,写出④⑦⑧元素的符号___________ ,其中非金属性最强的是___________ 。
(2)元素③、⑤、⑥原子半径由大到小为___________ 。
(3)元素②的原子结构示意图为___________ 。
(4)元素②、③形成的气态氢化物热稳定性:___________ >___________ ;元素①、③、⑤的化合物,写出其电子式:___________ 。
(5)元素⑦的最高价氧化物对应的水化物与元素⑤最高价氧化物对应的水化物溶液反应的方程式为___________ 。
(6)从原子结构的角度解释元素③和⑦的非金属性强弱:___________ 。
| ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)上述8种元素中,写出④⑦⑧元素的符号
(2)元素③、⑤、⑥原子半径由大到小为
(3)元素②的原子结构示意图为
(4)元素②、③形成的气态氢化物热稳定性:
(5)元素⑦的最高价氧化物对应的水化物与元素⑤最高价氧化物对应的水化物溶液反应的方程式为
(6)从原子结构的角度解释元素③和⑦的非金属性强弱:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表的一部分,根据表中给出的10种元素,回答下列问题。
(1)单质的化学性质最不活沷的元素是__________ ;
(2)氧的原子结构示意图是__________ ;
(3)形成化合物种类最多的元素是__________ ;
(4)HF和H2O中,热稳定性较强的是__________ ;
(5)N和P中,原子半径较小的是__________ ;
(6)常温下,会在浓硫酸中发生钝化的金属是_________ ;
(7)元素最高价氧化物对应水化物中,碱性最强的是___ (填化学式),酸性最强的是_____ (填“H2SO4”或“ HClO4”);
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | C | N | O | F | Ne | |||
| 3 | Na | Al | P | S | Cl |
(1)单质的化学性质最不活沷的元素是
(2)氧的原子结构示意图是
(3)形成化合物种类最多的元素是
(4)HF和H2O中,热稳定性较强的是
(5)N和P中,原子半径较小的是
(6)常温下,会在浓硫酸中发生钝化的金属是
(7)元素最高价氧化物对应水化物中,碱性最强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】元素在周期表中的位置反映了元素的原子结构和性质。下图是元素周期表的一部分,请按要求回答下列问题:
(1)元素①在元素周期表的位置:第_______ 周期第_______ 族,它是形成化合物种类最多的元素。
(2)写出②的元素符号_______ 。
(3)画出元素④的原子结构示意图_______ 。
(4)元素③和⑤的最高价氧化物对应的水化物中碱性较强的是_______ (填化学式)。
(5)比较⑦和⑧的原子半径大小_______ >_______ (填原子符号)。
(6)元素⑧的单质是一种_______ 色、有刺激性气味的气体。
(7)写出元素⑧的单质与水反应的化学方程式:_______ 。
(8)写出实验室制取元素⑧的单质的离子方程式:_______ 。
族 周期 | IA | 0 | |||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | |||
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
(2)写出②的元素符号
(3)画出元素④的原子结构示意图
(4)元素③和⑤的最高价氧化物对应的水化物中碱性较强的是
(5)比较⑦和⑧的原子半径大小
(6)元素⑧的单质是一种
(7)写出元素⑧的单质与水反应的化学方程式:
(8)写出实验室制取元素⑧的单质的离子方程式:
您最近一年使用:0次



